研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2012年11月6日
タンパク質に応答して細胞の運命を制御するRNAスイッチを3Dデザイン法で作製
齊藤博英准教授、樫田俊一さん(CiRA初期化機構研究部門)らの研究グループは、井上丹教授(京都大学大学院生命科学研究科)との共同研究で、3D分子モデルを用いたRNA-タンパク質相互作用の分子設計により、細胞内の状態に応じてRNA干渉 (RNAi)注1)の効果を制御できる「RNAスイッチ」注2)を開発することに成功しました。本研究成果は、2012年10月18日に英国科学雑誌『Nucleic Acids Research』にTop 5% のクオリティーをもつFeatured Articlesとして掲載され、また同紙の表紙に取り上げられています。
本研究グループは、これまでに、ショートヘアピンRNA(shRNA)注3)を改変することで、特定のタンパク質を発現したターゲット細胞の生死を制御することができる「RNAスイッチ」の開発に成功しています(Saito H., et al. Nat. commun. 2:160, 2011)。このスイッチは、細胞内で特定のタンパク質が生産されるのに応答して、標的の遺伝子の発現を制御することができますが、その作動原理を明らかにし、ヒト由来の様々なタンパク質に応答するスイッチに発展させることが、iPS細胞による目的細胞への分化を含む医学・生物学への応用に向けての課題でした。
shRNAはDicer(RNA切断酵素)によって切断されることで標的の遺伝子の発現を抑制するRNA干渉(RNAi)という現象を起こします。そのため、Dicerによる切断部位に特定のタンパク質が邪魔する形で結合すると、RNA干渉を防ぐことが予想できます。本研究では、まず3D分子モデルソフトを用いてこのshRNAスイッチとDicerの立体構造および、切断時の位置関係をコンピュータ上で再現することを試み、shRNAの二重鎖部位の長さを変更することで、Dicerの切断部位に結合するタンパク質がDicerと衝突する方向に近接するように、その位置を調節することができる可能性があることを見出しました。
実際に、U1A(ヒト細胞中に存在するタンパク質)が結合することによって、Dicerによる切断を阻害するようなshRNAスイッチを細胞内に導入したところ、細胞内でU1Aの生産に応答してRNAiの働きを、抑制できることがわかりました(図1)。さらに、3D分子デザイン法の汎用性を確かめるため、種々のがん細胞で発現している転写因子(NF-kB)に結合するRNA配列をshRNAに組み込んだところ、期待通り細胞内でのこの転写因子の発現に応じてRNAiの効果を抑制できることがわかりました。
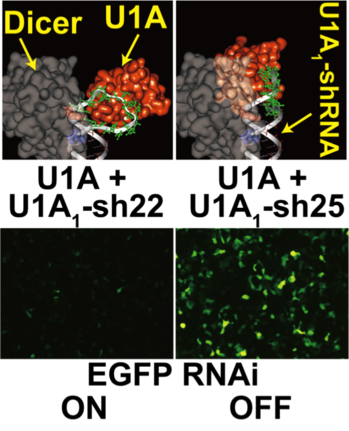
図1 3D分子モデルによるDicerとshRNAスイッチにつくタンパク質との立体障害予想(上)と細胞内でのshRNAスイッチの機能評価(下)
Dicerの働きを阻害しないと予想されたshRNA(左上)では、EGFP(蛍光蛋白質)に対するRNAiが抑制されず、EGFP(緑)の発現がみられなかった(左下)。Dicerによる切断を阻害すると予想されたshRNA(右上)では、RNAiが抑制されて、EGFPが発現した(右下)。
本研究では、3D分子モデルを用いたRNA-タンパク質相互作用の分子設計を利用し、ヒト培養細胞内の特定のタンパク質の有無に応じてRNA干渉 (RNAi)の効果を制御できる「RNAスイッチ」を開発することに成功しました。このデザイン法により、特定のタンパク質に応答するRNAスイッチの細胞内での機能を予測、最適化できます。また、今後、標的とする細胞の運命を細胞内状態に応じて制御する技術や、特定の細胞に分化した細胞だけを効率よく選別する技術などへの応用を通して、iPS細胞から標的細胞への分化誘導法の新たなツールとなることが期待できます。
この研究は、京都大学iPS細胞研究所、京都大学大学院生命科学研究科、京都大学白眉センターとの連携の元で実施されました。
【論文名】
【著者】
Shunnichi Kashida, Tan Inoue*, and Hirohide Saito*
(樫田俊一、井上丹*、齊藤博英*) * corresponding author
【本研究への支援】
本研究は、下記機関より資金的支援を受けて実施されました。
・ JST ICORP RNAシンセティックバイオロジープロジェクト
・ NEDO若手研究グラント
・ 文部科学省科学研究費補助金 若手研究A
・ 日本学術振興会特別研究員制度 (DC2)
・ 武田科学振興財団ライフサイエンス研究奨励
注1: RNA干渉(RNAi)
細胞内で形成される二本鎖RNAにより、任意の遺伝子の発現を抑制する手法であり、発見者であるアンドリュー・ファイアーとクレイグ・メローはRNAi発見の功績より2006年のノーベル生理学・医学賞を受賞した。最近では、RNAiを医薬品に応用する研究が進んでいる。
注2: RNAスイッチ
本研究では、RNAiを誘導するshRNAで生じるRNAとタンパク質の相互作用を利用して、細胞内で目的のタンパク質が発現しているときのみ、 RNAiの機構を働かなくさせる仕組みを利用する。すなわち、目的タンパク質Aが発現しない時は、RNAiの機構が働くのでターゲットmRNAが切断され、そのmRNAからのタンパク質合成Bはオフになるが、目的タンパク質Aが発現すると、RNAiの機構が阻害され、ターゲットmRNAが切断されなくなるため、タンパク質Bの合成は進行する。
注3: shRNA
short hairpin RNAの略で、ヘアピン型のRNAのこと。RNAiによる目的の遺伝子の働きを抑制するために使われる。