
研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2011年2月26日
マウス及びヒトiPS細胞の心筋細胞分化に及ぼすサイクロスポリンAの効果
山下潤 准教授(京都大学再生医科学研究所/iPS細胞研究所)研究グループと京都大学内分泌代謝内科(中尾一和教授)は、マウスiPS細胞やヒトiPS細胞からの心筋分化の際に、サイクロスポリンAを作用させると、効率良く心筋分化を誘導できることを明らかにしました。本論文は米国科学誌「PLoS ONE」6巻2号:e16734 (2011年2月発行)に掲載されました。
【ポイント】
【要旨】
iPS細胞(人工多能性幹細胞)注1は、マウスやヒトの線維芽細胞が初期化されることによって作製できる細胞です。これらのiPS細胞から心筋細胞を分化誘導する分子メカニズムや効率の良い誘導方法の開発は、心筋細胞モデルの構築や再生医療に貢献すると考えられます。これまでに我々は、マウスES細胞(胚性幹細胞)注2及びiPS細胞から誘導したFlk1を発現する前駆細胞注3を用いて心臓や血管が誘導できることや、Flk1陽性/ CXCR4陽性/ VE-cadherin陰性の細胞群(FCV細胞)注4が心筋の前駆細胞として高い心筋分化能を示すことを示してきました。また、サイクロスポリンA(CSA)注5が、マウスES細胞からFCV細胞や心筋細胞の誘導を劇的に促進することを明らかにしています。そこで本実験では、上記のES細胞を用いた研究から得られた知見をマウス及びヒトiPS細胞に対して用いて、それぞれの効果ついて検討しました。
その結果、OP9ストロマ細胞注6上でマウスiPS細胞由来Flk1陽性細胞を培養する際に、CSAを添加すると心筋細胞やFCV細胞が劇的に増加することが示されました。また、内胚葉様の支持細胞であるEND–2細胞との共培養によってヒトiPS細胞から自発的な拍動を示す心筋細胞のコロニーが得られましたが、この分化登場においてCSAを添加することにより、ヒトiPS細胞からの拍動コロニーの誘導効率は、約4.3倍に増加しました。
サイクロスポリンAを用いてヒトiPS細胞から誘導した心筋細胞は、種々の心筋特異的マーカー遺伝子を発現しているとともに、拍動に同調したカルシウムトランジェント注7、心筋様の活動電位、薬物反応や微細構造を示すことが示されました。
以上の結果から、本研究においてヒトiPS細胞から正常な機能を示す心筋細胞を得る基本的な技術が確立できたと考えています。
【研究の背景】
iPS細胞は、体細胞に4種の転写因子(Oct3/4, Sox2, Klf4, c–Myc)を導入して得られる多能性幹細胞です。成人組織の細胞から多能性細胞を作製できることから、再生医療や患者由来細胞を用いれば病態モデルを示す細胞の開発に利用することが期待されています。その中でも心筋細胞は再生医療への利用が期待される細胞の一つです。これまでに、幾つかの前駆細胞や成体の細胞から心筋細胞の分化が報告されていますが、機能的な心筋細胞の誘導効率は非常に低く、改善が求められていました。そのようなことからES細胞(胚性幹細胞)やiPS細胞などの多能性幹細胞は、体外で機能的な心筋細胞を誘導できる幹細胞として大きな期待を集めており、これまでに、マウスやヒトのES細胞を用いた様々な心筋誘導の研究が報告されています。これらの報告では、胚様体形成法やストロマ細胞との共培養、分化誘導の際の無血清培養、低酸素培養など、様々な方法が報告されています。しかしながら、ヒトES細胞からの心筋誘導は、マウスES細胞から誘導する方法と比較して、効率が低いのが現状です。iPS細胞はES細胞に性質が似ていることから、iPS細胞からの心筋誘導には、ES細胞で行ってきた知見を元にした研究が進められています。最近では、ヒトiPS細胞から胚様体注8形成を用いる方法で心筋誘導を行った結果が示されていますが、誘導効率の改善はみられておらず、効率の良い誘導方法が求められています。
これまでに山下研究室では、マウスES細胞及びiPS細胞から誘導したFlk1陽性細胞が心血管前駆細胞であることを示し、血管内皮細胞や心筋細胞などに分化誘導できることを示してきた。また、骨髄由来ストロマ細胞のOP9細胞上でFlk1陽性細胞を培養することで、自発的に拍動する心筋細胞が誘導できることを示してきました。さらに、Flk1陽性/ CXCR4陽性/ VE-cadherin陰性の細胞群(FCV細胞)が心筋の前駆細胞として高い心筋分化能を示すことなど、心筋や血管の分化研究を進めています。また、最近では、免疫抑制剤としても知られるサイクロスポリンAが、Flk1陽性の中胚葉系細胞から、FCV心筋前駆細胞や心筋細胞への誘導効率を高めることを示しています。つまりFlk1陽性細胞をOP9細胞と共培養中にサイクロスポリンAを添加すると、FCV心筋前駆細胞や心筋細胞への誘導効率を10–20倍高めることを示しています。本研究では、これまでに得られたマウスやヒトES細胞を用いた心筋誘導研究の知見をiPS細胞に適用し、マウス及び、ヒトiPS細胞から効率的な心筋細胞の誘導について詳細に検討しています。
【研究の成果】
(1)サイクロスポリンAは、マウスiPS細胞からの心筋及び心筋前駆細胞の誘導効率を向上する
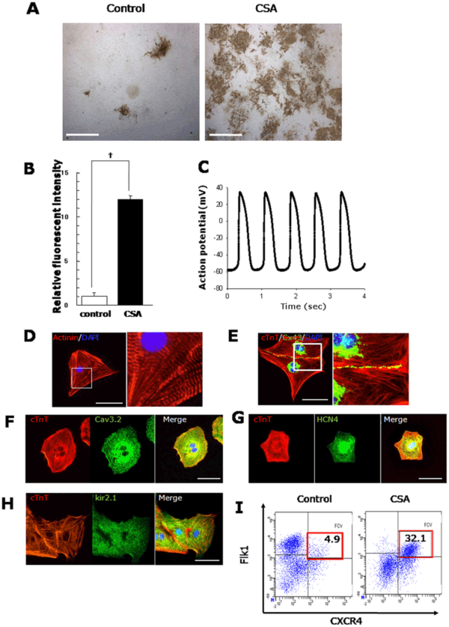
本研究では、まず初めにマウスiPS細胞からの心筋および心筋前駆細胞の分化に及ぼすサイクロスポリンAの影響を検討しました。その結果、Flk1陽性細胞から心筋誘導を行う際に、サイクロスポリンAを添加すると加えない場合と比べて約12倍多く、心筋トロポニン陽性(cTnT+)心筋細胞が得られました(図1A,B)。この結果は、これまでに得られていたマウスES細胞を用いた場合とほぼ同等の効率でした。
また、サイクロスポリンAを用いて誘導したマウスiPS細胞由来心筋細胞は、自発的な拍動をするとともに、活動電位も、正常の心筋と同様の結果を示しました(図1C)。さらに、誘導された心筋細胞には、サルコメア構造注9が確認でき、cTnT(心筋トロポニンT)注10や心筋細胞間のConnexin43注11といった、機能性を持つ心筋であることを示すマーカータンパクが存在することを確認しました。(図1D–H)
また、サイクロスポリンAがFCV心筋前駆細胞を約6.5倍増加させることを確認しました。以上の結果から、サイクロスポリンAは、マウスiPS細胞からの心筋及び心筋前駆細胞の誘導効率を向上することが示されました。
【図1】
A:マウスiPS細胞由来Flk1陽性細胞に及ぼすサイクロスポリンAの影響培養6日後。茶色の細胞は、cTnT染色された細胞で、心筋細胞であることを示す。
B:心筋細胞の誘導率
コントロールを1とした場合のcTnT染色された細胞の割合を示す。
C:誘導した心筋細胞の活動電位
D:誘導した心筋細胞のサルコメア構造
E:Connexin43タンパクの局在
F:T型Caチャンネル(Cav3.2)の局在
G:ペースメーカーイオンチャンネル(HCN4)の局在
H:心室イオンチャンネル(kir2.1)の局在
I:FACS分析による心筋前駆細胞の割合。赤枠がFCV心筋前駆細胞分画
(2)サイクロスポリンAは、ヒトiPS細胞からの心筋誘導においても誘導効率の向上に効果を示す
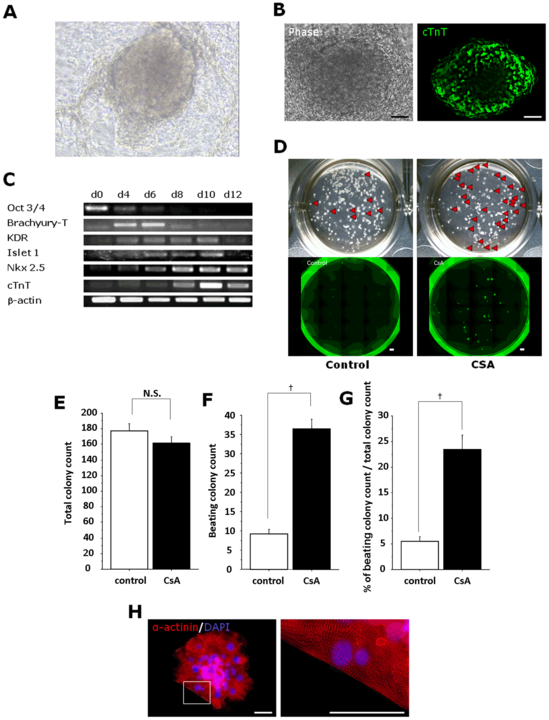
これまでに結果を得ていたヒトES細胞から心筋細胞に分化する実験系と同様の方法を用いて、ヒトiPSからの心筋分化を試みたところ、自発的な拍動を示す心筋を得ることができました(図2.A)。またこれらの心筋は、cTnTタンパク質が存在することが確認できました(図2.B)。さらに、幾つかの心筋に特異的な遺伝子の発現も見られました(図2.C)。以前のヒトES細胞を用いた実験では、細胞分化の培養を始めて約8日目に中胚葉系の細胞が見られましたが、この時期にサイクロスポリンAを添加して培養すると培養12日目の拍動心筋コロニーが有意に増加しました(図2.D)。すなわち、培養12日目の観察では、サイクロスポリンAの添加有無に関わらず、コロニーの総数に違いは見られませんでしたが(図2.E)、拍動しているコロニー数には、約4–4.3倍の違いが見られました(図2.F,G)。また、誘導した心筋細胞には、サルコメア構造も確認できました(図2.H)。以上の結果から、サイクロスポリンAは、ヒトiPS細胞からの心筋誘導においても誘導効率を向上させることが示されました。また、サイクロスポリンAの添加時期は、マウスのES細胞やiPS細胞の実験結果と同様に、中胚葉期に添加することで効果を示すことが示されました。
【図2】
A: ヒトiPS細胞由来の拍動する心筋細胞
B: 誘導した心筋コロニーのcTnTタンパクの局在。左が明視野、右が蛍光観察下の視野。
C: RT–PCRを用いた、心筋細胞特異的マーカー遺伝子の発現解析
D: 拍動心筋の誘導に及ぼすサイクロスポリンAの影響
E–G: コロニー数に対する拍動心筋の割合
H: 心筋細胞の免疫染色。サルコメア構造を確認する。
(3)ヒトiPS細胞から誘導した心筋細胞の機能評価
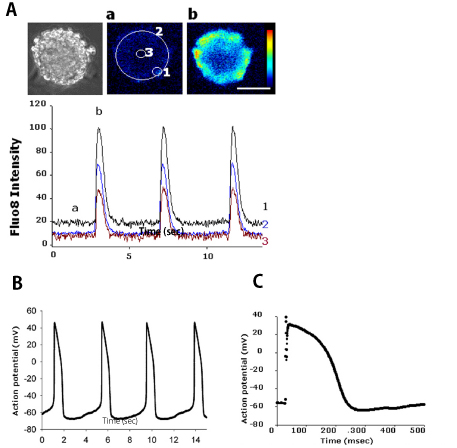
次に、サイクロスポリンAを用いてヒトiPS細胞から誘導した心筋細胞の機能評価を試みました。その結果、拍動する心筋細胞のコロニーにおいて、拍動に同調したカルシウムトランジェントが観察されました(図3.A)。活動電位を測定したところ、ペースメーカー能を持つ細胞を同定することができました(図3.B)。誘導した心筋コロニーは、10ヶ月以上も自発的な拍動を続けていました。約3ヶ月間拍動するコロニーから取り出した細胞は、心室の細胞のような活動電位パターンを示しました。これらの結果から、この培養システムによって、心臓を構成する種々の心筋細胞の作製ができることが示されました。
【図3】
A: 拍動心筋のカルシウムイオンの測定
B: 拍動する心筋細胞1個の活動電位
C: 自発的拍動を持たない心筋細胞の活動電位
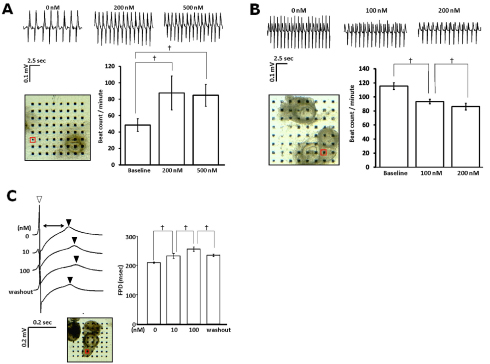
また、誘導した心筋の評価を行うために、薬剤反応検査についても実施しました。その結果、β刺激剤のイソプロテレノール注12を加えると、心筋細胞の拍動が早くなり(図4.A)、β阻害剤のプロプラノロール注13の添加により、拍動が遅くなりました(図4.B)。また、HERGチャンネル阻害剤注14のE4031に対しては、濃度依存的にQT延長を示す所見も確認できました(図4.C)。以上の結果からも、サイクロスポリンAを用いてヒトiPS細胞から誘導した心筋細胞は、有用なヒト心筋細胞モデルになりうると考えられます。
【図4】
誘導した心筋細胞の各薬剤に対する反応
A: イソプロテレノール
B: プロプラノロール
C: E–4031
(4)ヒトiPS細胞から誘導した心筋細胞の構造の評価
最後に、サイクロスポリンAを用いてヒトiPS細胞から誘導した心筋細胞を、電子顕微鏡を用いて細胞の微小構造についても観察しました。その結果、筋原繊維のZ帯構造注15やミトコンドリアを豊富に観察することができました(図5.A–D)。また、細胞間には、デスモソーム注16(図5.D)と呼ばれる細胞接着構造を伴った介在板や心房の分泌顆粒(図5.E)や糖原顆粒(図5.F)など心筋特異的構造を観察することができました。
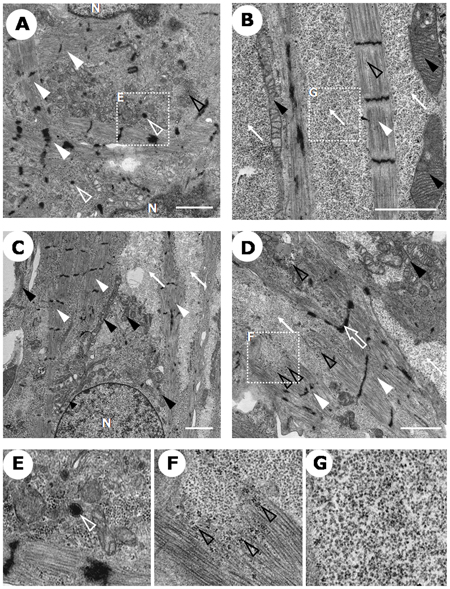
【図5 ヒトiPS細胞から誘導した心筋の微細構造の分析】
白の矢頭: 筋原繊維のZ帯構造(A–D)、 黒の矢頭: ミトコンドリア(B–D)白枠の矢印: デスモソーム(D)、 白枠の矢頭: 心房の分泌顆粒(A,E)黒枠の矢頭: 糖原顆粒(D,F)、 白の矢印: リボソーム顆粒(B–D,G)
【今後の展開】
本研究では、マウス及びヒトiPS細胞から心筋細胞を誘導する際に、サイクロスポリンAは効果的に作用することを明らかにしました。また、この方法で誘導した心筋細胞は、心筋特異的な機能や構造を有し、正常の心筋に近い電気生理学的反応や微細構造を示すことが確認できました。
ヒトiPS細胞から作製した心筋細胞は、創薬における毒性検査や心筋の再生医療への利用が期待されています。今回の心筋誘導法には、まだ改善すべき点があると考えられますが、さらに改良を進めることで、より生体内の心筋に近い細胞を作りだすことが可能になると考えられます。これらの技術の進展は、細胞移植治療などの再生医療や新薬開発の創薬研究に大きく貢献できると考えられます。
【論文名】
"Induction and enhancement of cardiac cell differentiation from mouse and human induced pluripotent stem cells with cyclosporin-A"
「マウス及びヒトiPS細胞の心筋細胞分化に及ぼすサイクロスポリンAの効果」
Masataka Fujiwara, Peishi Yan, Tomomi G. Otsuji, Genta Narazaki, Hideki Uosaki, Hiroyuki Fukushima, Hiroyuki Matsuda, Koichiro Kuwahara, Masaki Harada, Hiroyuki Matsuda, Satoshi Matsuoka Keisuke Okita, Kazutoshi Takahashi, Masato Nakagawa, Tadashi Ikeda, Ryuzo Sakata, Christine L. Mummery, Norio Nakatsuji, Shinya Yamanaka, Kazuwa Nakao, Jun K. Yamashita.
PLoS ONE. 2011 February Vol6 (2); e16734
【本研究への支援】
本研究は、下記機関より資金的支援を受け実施されました。
【用語説明】
(1) iPS細胞
人工多能性幹細胞(iPS細胞:induced pluripotent stem cell)のこと。皮膚細胞などの体細胞に特定因子を導入することにより樹立される。胚性幹細胞(ES細胞)のように無限に増え続ける能力と体のあらゆる組織細胞に分化する能力を有する多能性幹細胞である。
(2) ES細胞(胚性幹細胞)
胚性幹細胞(ES細胞:embryonic stem cell)のこと。ES細胞は受精後6、7日目の胚盤胞から細胞を取り出し、それを培養することによって作製される多能性幹細胞の一つで、あらゆる組織の細胞に分化することができる。しかし、受精卵を破壊する必要があり、患者自身の細胞から作製することが困難なため、免疫拒絶の問題が指摘されている。
(3) 前駆細胞
幹細胞から特定の機能をもつ細胞に分化する前の細胞のことを前駆細胞と呼ぶ。
(4) Flk1陽性/ CXCR4陽性/ VE-cadherin陰性の細胞群(FCV細胞)
Flk1とCXCR4という遺伝子の発現があり、かつ、VE-cadherin遺伝子の発現が見られない細胞群。遺伝子発現の状態を指標にして細胞を選ぶ。FCV細胞は、心筋の前駆細胞として高い心筋分化能を示す。
(5) サイクロスポリンA (Cyclosporin–A:CSA)
免疫抑制剤として良く知られる薬剤で、臓器移植の拒絶反応の抑制や自己免疫疾患の治療にも用いられる。
(6) OP9ストロマ細胞
OP9という骨髄に由来する間質細胞(ストロマ細胞)のこと。ES細胞やiPS細胞のような多能性幹細胞を様々な組織の細胞に分化する際、共培養して用いる。OP9ストロマ細胞はES細胞を血液系の細胞に分化させる作用をもつことが知られている。
(7) カルシウムトランジェント
活動電位に従って細胞質内全体のカルシウムイオン濃度が上昇する動きのことで、心筋収縮に対応して変化する。カルシウムイオン濃度を測定することで、心筋収縮の状態を観察する。
(8) 胚様体
EB(embryoid body)とも言われ、ES細胞やiPS細胞などを浮遊培養するとボール状の細胞塊を形成する。この状態で2 週間程度培養すると、様々な細胞種への分化が観察される。細胞の分化多能性を調べる一般的な方法の一つとして用いられている。
(9) サルコメア構造
骨格筋は筋繊維によって形成される。そして筋繊維は多数の筋原繊維が束になったものである。この筋原繊維はZ膜でしきられており、このZ膜に仕切られた単位をサルコメアと呼ぶ。
(10) cTnT(心筋トロポニンT)
トロポニン(Troponin)は骨格筋や心筋の収縮に不可欠な3つの蛋白質(TnC, TnI, TnT)の複合体のこと。アクチンフィラメントの間の溝に沿って点在している。cTnTは、3つのサブユニットの一つ。
(11) Connexin43
隣り合う細胞の細胞膜間で、水溶性の小さいイオンや分子を通過させる「ギャップ結合」を構成するタンパク質のひとつ。
(12) イソプロテレノール
アドレナリン作動薬のひとつで、β受容体に作用して心筋刺激作用を引き起こす薬剤。心停止の際に静脈内注射薬として使用される。
(13) プロプラノロール
β1受容体とβ2受容体を遮断し、アドレナリン作動性効果を遮断する薬剤。不整脈、高血圧、心筋梗塞、緑内障、偏頭痛の治療に使用される。
(14) HERGチャンネル阻害剤
HERG(human ether-a-go-go related gene:ヒト遅延整流性カリウムイオンチャネル遺伝子)チャネルの働きを阻害する薬剤。このチャンネルがブロックされるとQT延長が起こり不整脈、心室細動が引き起こされ、最悪の場合心臓停止に至る。
(15) Z帯構造
横紋筋の収縮単位のサルコメアを仕切る膜状の構造である。Z帯以外に、Z線、Z膜、Z板、などとも呼ばれる。
(16) デスモソーム
上皮細胞によくみられる細胞間接着装置のこと。接着班とも呼ばれる。






















