
研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2020年7月3日
筋ジストロフィーモデルマウスにおけるヒトiPS細胞由来骨格筋幹細胞の移植効果を確認
ポイント
- 筋肉の高い再生能をもつ骨格筋幹細胞注1)をヒトiPS細胞から分化させることに成功した。
- ヒトiPS細胞から分化させた骨格筋幹細胞をデュシェンヌ型筋ジストロフィーモデルマウスに移植したところ、筋張力注2)の改善がみられた。
趙明明研究員(京都大学CiRA臨床応用研究部門)、櫻井英俊准教授(京都大学CiRA同部門)らの研究グループは、ヒトiPS細胞から筋再生能のある骨格筋幹細胞を誘導する方法を確立しました。また、この細胞をデュシェンヌ型筋ジストロフィーモデルマウスに移植したところ、筋張力の改善効果があることがわかりました。これにより、将来の細胞移植療法の実現に貢献できると期待されます。
この研究成果は2020年7月3日午前1時(日本時間)に米国科学誌「Stem Cell Reports」でオンライン公開されました。
デュシェンヌ型筋ジストロフィー(DMD)は、筋肉にあるジストロフィンというタンパク質が欠損することによって発症する進行性の重篤な筋疾患で、根本的な治療法は開発されていません。
ジストロフィンを骨格筋に再生する方法として細胞移植治療が期待されていますが、生体由来の骨格筋幹細胞であるサテライト細胞注3)の他家移植による治療では、治療効果が認められていません。また、他のグループの研究によって、Pax7という遺伝子を強制的に発現させ続けることで骨格筋幹細胞を多能性幹細胞注4)から誘導する方法も開発されましたが、遺伝子導入を行った細胞を移植するには現状では安全面で課題があります。
そこで本研究グループは、ヒトiPS細胞を段階的に骨格筋の発生過程をたどりながら分化させ、筋肉の高い再生能を持つ骨格筋幹細胞の誘導を目指して研究を行いました。
(1) ヒトiPS細胞から骨格筋幹細胞を誘導
まず本研究グループは、段階的に発生過程をたどるためにPax3という遺伝子に注目し、初期の中胚葉発生過程をモニターすることで、ヒトiPS細胞から効率的に骨格筋前駆細胞注5)を得られる方法を開発しました。この方法は、他の研究グループによって報告された方法よりも誘導効率が上昇していることが分かりました。さらに骨格筋前駆細胞に特異的に発現する遺伝子の中でも、Myf5という遺伝子に着目したところ、発生過程初期(4週目)ではMyf5陽性細胞は円形の細胞で、発生初期の骨格筋前駆細胞と考えられるのに対し、発生過程後期(12週目)になると、融合して長く伸びた筋管細胞と同じ場所にMyf5陽性細胞が集まっていることがわかりました(図1)。
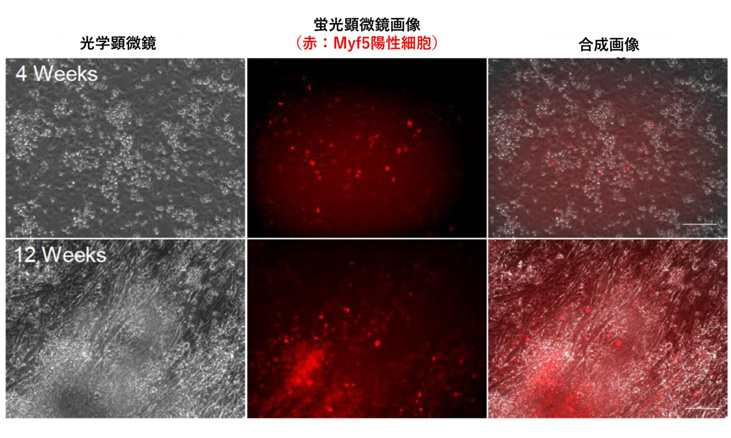
図1 ヒトiPS細胞から骨格筋前駆細胞への分化の様子
上段は分化開始後4週目、下段は12週目。Myf5陽性細胞は繊維状の骨格筋前駆細胞に分化している。スケールバーは50µm。
また、発生過程後期(12週目)には、Myf5陽性細胞がMyf5陰性細胞に比べて、Pax7など、サテライト細胞に特徴的な遺伝子も多く発現していることが分かりました。
これらの結果を踏まえ、ヒトiPS細胞由来のMyf5陽性細胞とMyf5陰性細胞を、それぞれ30万細胞ずつ免疫不全マウスのすねの筋肉(前脛骨筋)に移植すると、Myf5陰性細胞に比べてMyf5陽性細胞のほうが、移植後に筋線維を形成している度合いが高く、筋再生能が高いことが示唆されました(図2A、B)。また、発生過程初期(分化開始後6週目)と後期(12週目)の細胞を比べてみると、初期のMyf5陽性細胞に比べて、後期のMyf5陽性細胞のほうが移植後の筋再生能が高いことがわかりました(図2C)。そしてこの分化後期のMyf5陽性細胞は、
筋再生能の高い胎児型の骨格筋幹細胞注6)と似た遺伝子発現パターンを示していることがわかりました。
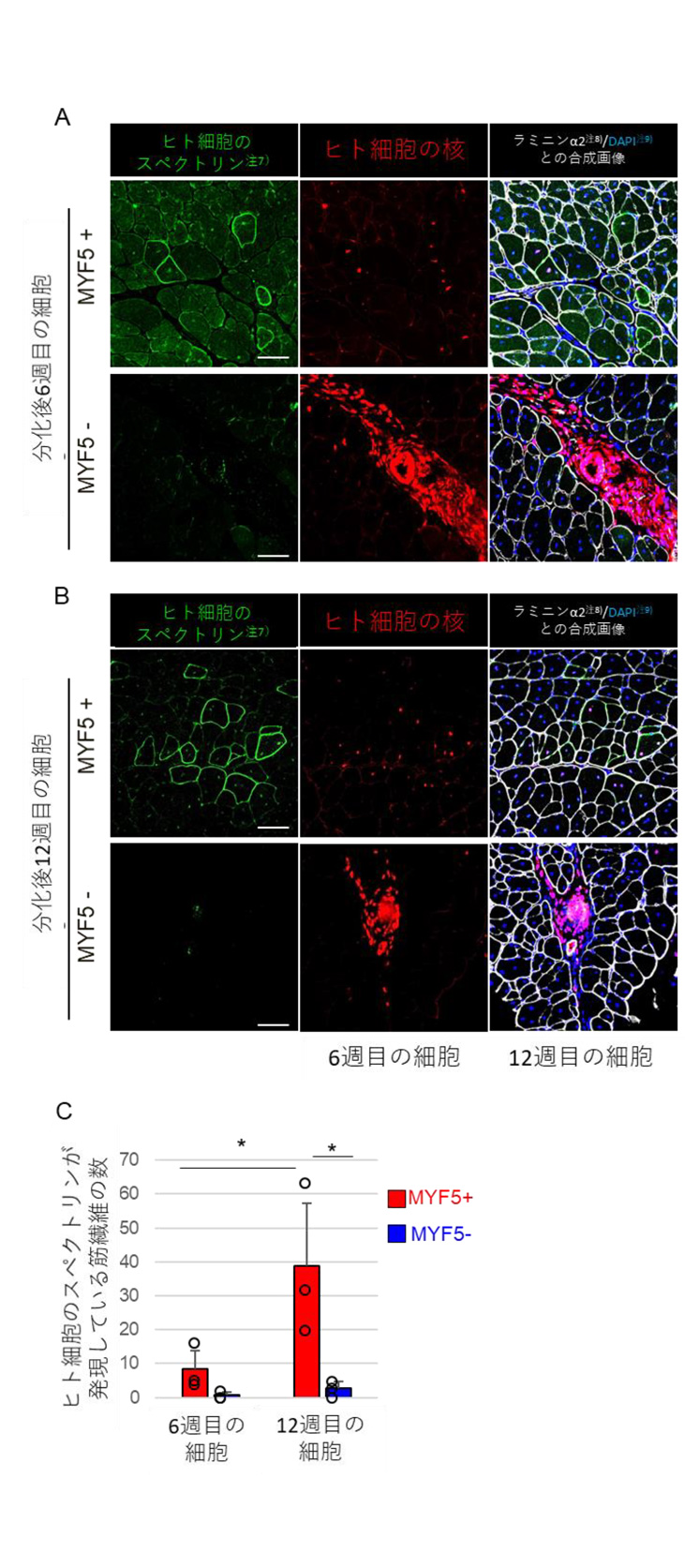
図2 ヒトiPS細胞由来のMyf5陽性細胞とMyf5陰性細胞による筋肉の再生能の違い
A:分化後6週目のMyf5陽性細胞(上段)および陰性細胞(下段)を移植した組織の蛍光顕微鏡画像。Myf5陰性細胞に比べて、Myf5陽性細胞のスペクトリン注7)発現量が多く、核が分散していることから、より筋細胞に分化しやすく、筋線維に分散して生着し、筋肉を再生していることがわかる。
B:分化後12週目のMyf5陽性細胞(上段)および陰性細胞(下段)を移植した組織の蛍光顕微鏡画像。図2Aと同様、Myf5陽性細胞のほうが筋細胞に分化しやすく、筋線維に分散して生着し、筋肉を再生していることがわかる。
C:分化後6週目および12週目のMyf5陽性細胞または陰性細胞を移植した後、ヒト細胞のスペクトリンを発現していた筋線維の数。12週目のMyf5陽性細胞の方が、筋肉の再生能が高いことが分かる。
スケールバーは50µm。
(2) DMDモデルマウスでの移植効果の確認
(1)の結果を踏まえ、発生過程後期(12週目)のMyf5陽性細胞の移植効果を確認するため、DMDモデルマウスのすねの筋肉(前脛骨筋)に30万個のMyf5陽性細胞を移植しました。すると、1匹あたり100本以上のジストロフィン陽性筋線維が再生されるのが確認されました(図3A、赤色)。また一部のMyf5陽性細胞は移植後にPax7陽性のサテライト細胞になっていると考えられます(図3B、矢頭)。
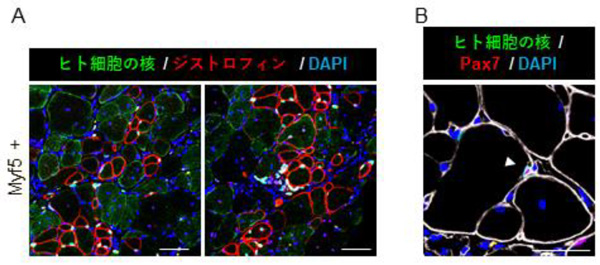
図3 細胞移植後のDMDモデルマウスの筋組織
A:移植後のDMDモデルマウスの筋組織。赤く見えるのがジストロフィンを再生できた筋線維。緑色のヒト核がたくさん生着しており、筋再生に寄与している様子がわかる。左右の写真は、それぞれ筋肉の別の部位を同条件下で撮影したもの。
B:サテライト細胞のマーカー遺伝子であるPax7の発現を確認。矢頭の核がヒト由来かつPax7陽性であることが分かる。
スケールバーは50µm。
最後に運動機能を評価するため、DMDモデルマウスの右ふくらはぎの筋肉(腓腹筋)に100-200万のMyf5陽性細胞を移植しました。移植後6週のマウスの筋力を測定すると、弱いながらも有意な筋張力の改善効果が示されました(図4)。
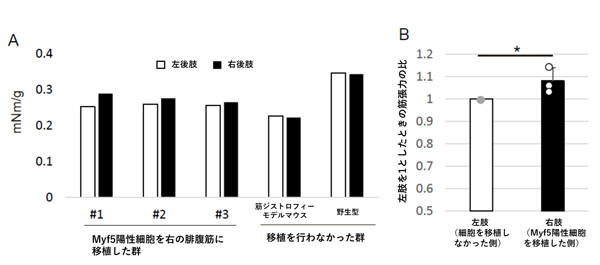
図4 細胞を移植したマウスと移植をしなかったマウスの筋張力の比較
A:Myf5陽性細胞を移植したマウスと、対照群のマウスの体重当たりの筋張力。
B:Myf5陽性細胞を移植したマウスにおける左脚と右脚の筋張力の比。
DMDの進行に伴って失われるジストロフィンを補うため、細胞移植療法が有効と目されていますが、これまで、安全性と治療効果の両方において有用な移植用の細胞は見出されてきませんでした。本研究では、骨格筋の発生過程を再現するという比較的臨床応用しやすいと考えられる方法で、ヒトiPS細胞から骨格筋前駆細胞を分化させる方法を確立しました。さらに、Myf5という遺伝子の発現の有無と発生段階の時期によって、筋再生能の高い胎児型の骨格筋幹細胞を抽出できることが明らかになり、実際にDMDモデルマウスでの移植効果を示しました。
今後はこの手法を改良し、治療効果の高い細胞を安定して作製する方法を確立することを目指します。
- 論文名
Induced Fetal Human Muscle Stem Cells with High Therapeutic Potential in a Mouse Muscular Dystrophy Model - ジャーナル名
Stem Cell Reports - 著者
Mingming Zhao1* §, Atsutoshi Tazumi1,2 §, Satoru Takayama1,2 §, Nana Takenaka-Ninagawa1, Minas Nalbandian1, Miki Nagai1, Yumi Nakamura1, Masanori Nakasa1, Akira Watanabe3, Makoto Ikeya1, Akitsu Hotta1, Yuta Ito4, Takahiko Sato5, and Hidetoshi Sakurai1*
§ 同等貢献
* 責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所 臨床応用研究部門
- 旭化成株式会社
- 京都大学iPS細胞研究所 未来生命科学開拓部門
- 名古屋学院大学リハビリテーション学部
- 藤田医科大学医学部 解剖学Ⅰ
本研究は、下記機関より支援を受けて実施されました。
- AMED 再生医療実現拠点ネットワークプログラム 技術開発個別課題
- AMED 再生医療実現拠点ネットワークプログラム iPS細胞研究中核拠点
- 国立精神・神経医療研究センター精神・神経疾患研究開発費
- AMED 産学連携医療イノベーション創出プログラム セットアップスキーム(ACT-MS)
注1)骨格筋幹細胞
骨格筋が損傷したとき、損傷部を修復するために骨格筋系の細胞に分化する幹細胞。
注2)筋張力
筋肉が伸び縮みする力。
注3)サテライト細胞
生体内で、筋線維の外側に張り付いている細胞。成人型の骨格筋幹細胞の名前。
注4)多能性幹細胞
ほぼ無限に増やすことができ、体のあらゆる細胞に変化することのできる性質をもつ細胞。多能性幹細胞には、ES細胞やiPS細胞がある。
注5)骨格筋前駆細胞
受精卵が分裂・成長してさまざまな細胞に変化していくときに生じる、骨格筋のもとになる細胞。
注6)胎児型の骨格筋幹細胞
サテライト細胞よりも未熟な骨格筋幹細胞。成人型であるサテライト細胞に比べて増殖能力が高く、移植後の生着率も高いといわれている。
注7)スペクトリン
筋組織に特徴的なタンパク質。今回の実験では、ヒト細胞のスペクトリンを発現している筋線維が多いほど、移植した細胞が筋線維に分化し生着していることを示す。
注8)ラミニンα2
細胞膜に存在するタンパク質。
注9)DAPI
DNAを染色する色素。























