
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2017年8月31日
iPS細胞由来神経細胞の他家移植におけるMHC適合の有用性
ポイント
- MHC注1不適合のサルiPS細胞由来ドパミン神経細胞を他のサルの脳に移植すると、免疫反応が引き起こされた。
- MHCを適合させることで、移植したドパミン神経細胞への免疫反応が抑制され、生着率が向上した。
- MHC不適合の場合でも、免疫抑制剤の利用により免疫反応を抑制できた。
森実飛鳥特定拠点助教(京都大学CiRA臨床応用研究部門)、髙橋淳教授(京都大学CiRA同部門)らの研究グループは、理化学研究所、東海大学、滋賀医科大学との共同研究により、iPS細胞由来神経細胞を他家移植注2する際のMHC適合の有用性を示しました。
現在、パーキンソン病などの脳神経疾患において、iPS細胞から作製した神経細胞を移植することで症状の改善を図る再生医療に向けた研究が進められています。その再生医療には、他家移植も視野に入れられています。一般的に免疫反応が起きやすい骨髄移植や腎臓移植では、HLAを適合させることが生着率を上げると知られています。神経細胞は免疫反応を起こしにくいとされており、これまで胎児神経細胞などの他家移植が行われてきましたが、HLA適合の有用性については議論が分かれていました。
本研究では、MHCの型をホモ接合体注3でもつ健常なカニクイザルからiPS細胞を作製し、ドパミン神経細胞へと変化(分化)させ、それをMHCが適合しないサル、あるいは同じMHCの型をヘテロ接合体注3でもつサルの脳に移植しました。その結果、MHC不適合の場合、移植片に対して免疫反応が引き起こされる一方、MHCを適合させた場合は免疫反応が有意に抑えられることが分かりました。また、MHCが不適合の場合でも免疫抑制剤の投与により、MHCを適合させた場合と同程度まで抑制できることが分かりました。さらに、MHCを適合させると、不適合の場合と比較し、移植した神経細胞の生着率が有意に高くなることも確認できました。
本研究では、免疫反応を起こしにくいとされていた神経細胞であっても他家移植の際にはMHC(ヒトの場合はHLA)を適合させることが有用であることを示しました。iPS細胞由来神経細胞を用いた再生医療の臨床応用に貢献できると期待されます。
この研究成果は2017年8月30日18時(英国時間:日本時間8月31日2時)に英国科学誌「Nature Communications」でオンライン公開されました。
パーキンソン病を含む様々な疾患の治療に向け、iPS細胞から作製した細胞を移植する再生医療の研究が進められています。iPS細胞は自分の体細胞から作製できるため、自家移植注4が可能となるという利点があります。しかしながら、現状では患者さん1人あたりのコストと時間が大きくかかります。また、疾患の遺伝的背景をもつ患者さんから作製したiPS細胞由来の細胞を移植した場合、再びその疾患にかかりやすくなる可能性があるため、他家移植が有望視されています。そこで、臨床応用に向け、他家移植の際の免疫反応が起きにくいHLA型の組み合わせをもつ健康な方から予めiPS細胞を作製し備蓄しておくという取り組みが始められています。
これまで神経細胞は免疫反応を起こしにくいとされてきました。パーキンソン病の治療を目指し、欧米では数十年にわたり胎児神経細胞を患者さんの脳に移植するという研究が行われており、HLA型を適合せずとも長期間移植した神経細胞が生着すると報告されています。一方で、移植細胞への免疫反応が生着率や機能に影響を及ぼすという報告もされています。
そこで、髙橋教授らのグループは、iPS細胞由来神経細胞の他家移植の医療応用に向け、MHCを適合させることの有用性の検討を行いました。
1. MHCが不適合な宿主への神経細胞移植は免疫反応を引き起こす
まず研究グループは、移植時の免疫反応に大きく関与するMHCの型の組み合わせ(ハプロタイプ)をホモ接合体でもつ健常なカニクイザルよりiPS細胞を作製し、脳のドパミン神経細胞へと分化させました。そのドパミン神経細胞約500万個を、同じハプロタイプを持たないサル(MHC不適合)、ヘテロ接合体にもつサル(MHC適合)のそれぞれ6頭ずつに移植しました。各サルの左脳の被殻という部位に6カ所ずつ移植しています。また、それぞれのサルに免疫抑制剤であるタクロリムスを投与する群もつくりました(図1)。
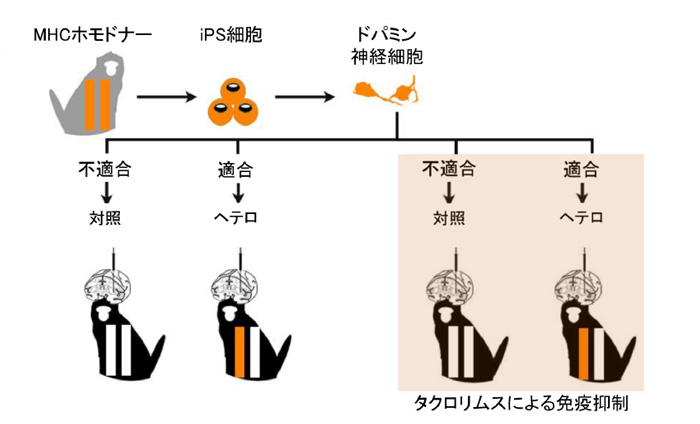
図1. 本研究での実験デザイン
MHCホモ接合体サルのiPS細胞由来ドパミン神経細胞を、同じハプロタイプをもたないサル(MHC不適合;対照群)とヘテロ接合体サル(MHC適合)に移植した。また、それぞれに免疫抑制剤(タクロリムス)投与群をつくった。
ドパミン神経細胞を移植してから3か月間、それぞれのサルの脳をPET注5画像にて観察しました。この際、脳の炎症を検出するPETプローブ注6を用いることで、免疫反応に関連した神経炎症を検出することができます。神経炎症は主にミクログリア注7の活性化に伴う輸送タンパク質の発現の度合いを計測することで評価します。その結果、MHC不適合の場合、移植片領域周辺で神経炎症が起こっていることが分かりました(図2)。
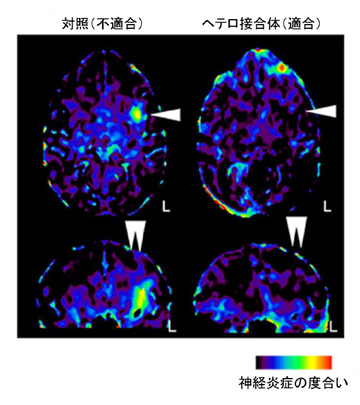
図2. ドパミン神経細胞移植後3か月の脳のPET画像
上段は水平な脳の断面画像、下段は垂直方向での脳を断面画像。
細胞を移植した領域周辺(矢頭)で、神経炎症が起きている様子が分かる。
これは、ドパミン神経細胞を移植した領域において免疫反応が起きたことを示しています。一方、MHC不適合でありながら、タクロリムスを投与した群においては、MHC適合群と同等まで神経炎症が抑えられていることが分かりました(図3)。
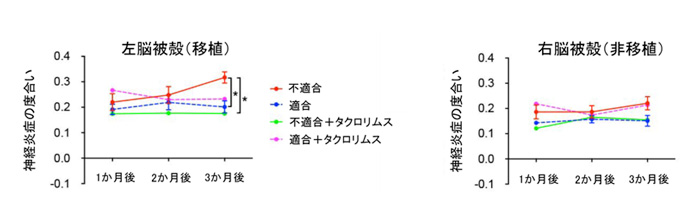
図3. 移植後3か月間における神経炎症の度合いの変化
左は実際にドパミン神経細胞を移植した左脳被殻における神経炎症の度合いを示し、右は細胞を移植していない右脳被殻での様子を示す(比較対象)。
MHC不適合で移植をした場合、適合させた場合よりも有意に高く神経炎症が引き起こされていることが分かる。(アスタリスクは有意差があることを示す。)
他家移植において、移植片の生着は急性・亜急性の免疫反応の有無が鍵を握ります。上記のPET画像を用いた解析の結果から、急性・亜急性免疫反応は多くは移植後2〜3か月から起こることが分かりました。そこで、研究グループはその時期が過ぎた移植後4か月に、移植領域周辺の免疫反応の様子を組織学的に検証しました。
その結果、MHC不適合の場合、活性化したミクログリアが蓄積しており、宿主由来のリンパ球が移植片へ浸潤していたことが分かりました。リンパ球の移植片への浸潤は、一般に宿主の細胞が移植片を攻撃する免疫反応の病理として知られており、今回の実験でもMHC不適合の宿主に移植されたドパミン神経細胞が免疫反応を受けていることが明らかとなりました。なお、タクロリムスを投与することにより、リンパ球の浸潤つまりは免疫反応が抑制されていることも分かりました(図4)。
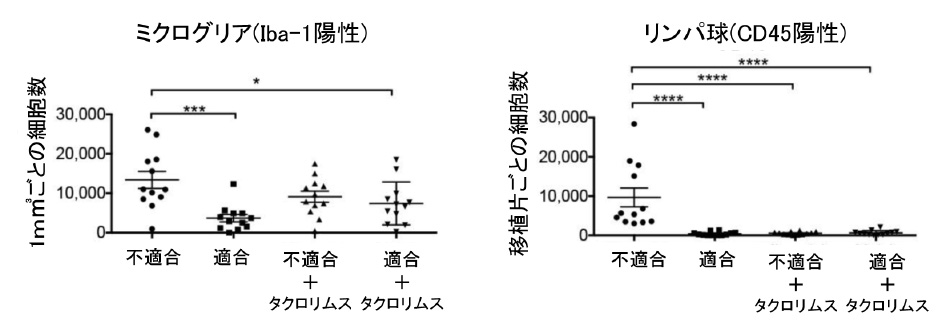
図4. 移植後4か月におけるミクログリア数ならびに移植片への浸潤リンパ球数
MHC不適合の宿主に移植した場合、MHC適合宿主への移植と比較して有意にミクログリアとリンパ球が増加しており、免疫反応が起きていることが確認できる。タクロリムスを投与した場合では、免疫反応は抑制される。(アスタリスクは有意差があることを示し、数が多いほど有意。)
2. MHC適合により、移植したドパミン神経細胞の生着率が向上する
次に研究グループは、MHCの適合・不適合によるドパミン神経細胞の脳への生着の違いを検証しました。その結果、MHCを適合させた場合、不適合の場合よりも有意に多数のドパミン神経細胞が生着していることが確認され、MHC適合により移植した神経細胞の生着率が向上することが明らかになりました(図5)。
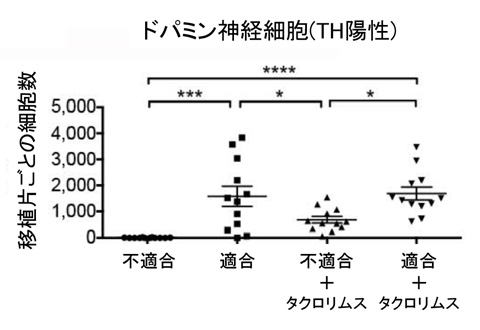
図5. 移植後4か月におけるドパミン神経細胞の生着数
MHCが適合する場合、ドパミン神経細胞の生着率は有意に高くなる。
(アスタリスクは有意差があることを示し、数が多いほど有意。)
これまで脳は免疫反応を起こしにくい臓器として知られていました。しかし、本研究により、神経細胞の脳への他家移植においても、MHCが不適合であると移植片に対する免疫反応が起こり、免疫抑制剤の利用で抑制できること、また、MHC適合が免疫反応を完全にではなくとも抑え、生着率を高めることが霊長類モデルにて確認できました。今後、遅発性の免疫反応についても研究を進める必要がありますが、本研究成果は将来のiPS細胞由来神経細胞の他家移植の臨床応用に貢献するものと期待されます。
- 論文名
"MHC matching improves engraftment of iPSC-derived neurons in non-human primates" - ジャーナル名
Nature Communications - 著者
Asuka Morizane1, Tetsuhiro Kikuchi1, Takuya Hayashi2, Hiroshi Mizuma2, Sayuki Takara2, Hisashi Doi2, Aya Mawatari2, Matthew F. Glasser3, Takashi Shiina4, Hirohito Ishigaki5, Yasushi Itoh5, Keisuke Okita1, Emi Yamasaki1, Daisuke Doi1, Hirotaka Onoe2, Kazumasa Ogasawara5, Shinya Yamanaka1,6, Jun Takahashi1,7 - 著者の所属機関
- 京都大学iPS細胞研究所
- 理化学研究所 ライフサイエンス技術基盤研究センター
- ワシントン大学医学部
- 東海大学医学部
- 滋賀医科大学医学部
- グラッドストーン研究所
- 京都大学大学院医学研究科
本研究は、下記機関より資金的支援を受けて実施されました。
- AMED再生医療実現拠点ネットワークプログラム
注1) MHC(major histocompatibility complex:主要組織適合遺伝子複合体)
免疫反応に関わる遺伝子を多く含む大きな遺伝子領域。ヒトではHLA(human leukocyte antigen:ヒト白血球型抗原)と呼ばれる。
注2) 他家移植
ある個体由来の細胞や組織を、同種の別個体の体内に移植すること。
注3) ホモ接合体、ヘテロ接合体
遺伝子座(遺伝子の場所)にある一対、または2 つ以上の遺伝子のことを対立遺伝子と呼ぶ。父親と母親それぞれから同一の対立遺伝子を受け継ぎ持つ場合をホモ接合体、それぞれ異なる対立遺伝子を持つ場合は、ヘテロ接合体という。
注4) 自家移植
ある個体由来の細胞や組織を、同一個体の体内に移植すること。
注5) PET(陽電子放出断層撮影)
プラスの電気を帯びた電子を放出する同位元素(アイソトープ)で標識された薬剤(PET薬剤)を注射し、体内分布を特殊なカメラで断層撮影する装置。がんの性質などの検査に有用な診断機器。
注6) PETプローブ
生体機能を調べられたり、特定の分子を認識できる分子の総称をプローブという。PETプローブは、PET検査の際に用いられるプローブをさす。
注7) ミクログリア
中枢神経系に存在するグリア細胞(神経系を構成する神経細胞以外の細胞)の一種。脳内で免疫機能を担っている細胞。























