
研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2023年12月1日
腎集合管オルガノイドを用いた多発性嚢胞腎モデルの作製
iPS創薬により治療薬候補を発見、治験開始へ
ポイント
- iPS細胞から作製した腎集合管注1オルガノイド注2を使って、多発性嚢胞腎モデルの作製に成功した。
- 疾患モデルを活用して多発性嚢胞腎の治療薬候補を見出した。
- 京大発スタートアップ企業のリジェネフロ社が近く治験を開始する。
前伸一特定拠点講師(CiRA増殖分化機構研究部門)および長船健二教授(CiRA同部門)らの研究グループは、iPS細胞から集合管を作製し、難病である多発性嚢胞腎の病態モデルを作製することに成功しました。また、このモデルを活用して、治療薬候補の物質を見出しました。
多発性嚢胞腎は、腎臓に水が溜まった袋(嚢胞)が多数形成され、腎臓の機能が低下してしまう難病です。中でも、常染色体顕性(優性)多発性嚢胞腎(ADPKD)注3では、主に集合管から嚢胞ができます。しかし、ヒト細胞を用いて、この症状を再現したモデルはありませんでした。これまでの報告では、ヒトiPS細胞から作製した腎尿細管嚢胞モデルが作製されていましたが、ADPKDの治療薬候補は見つかっていませんでした。本研究では、集合管を形成する前駆体である尿管芽注4を利用しました。ヒトiPS細胞から作製した尿管芽細胞の拡大培養を行い、集合管オルガノイドの発生段階を進めることに成功しました。ゲノム編集によりPKD1遺伝子を働かない状態にしたヒトiPS細胞を作製し、そのiPS細胞由来の集合管オルガノイドがすべて自発的に多数の嚢胞を形成することを示し、嚢胞形成の開始メカニズムを明らかにしました。さらに、嚢胞形成を有意に抑制する薬剤の候補として、レチノイン酸受容体(RAR)作動薬を同定することに成功し、その治療効果をADPKDマウスモデルで確認しました。今回開発した、集合管嚢胞モデルは、ADPKDの疾患メカニズムの解明と創薬に貢献すると期待できます。
この研究成果は2023年12月1日(日本時間)に「Cell Reports」で公開されました。
ADPKDは、腎臓内に多数の嚢胞を形成する進行性の難病で、人工透析や腎移植を必要とする末期腎不全に至ります。1,000〜4,000人に1人が罹患し、世界の腎不全の5~10%を占めています。ADPKD患者さんの腎嚢胞は、糸球体や腎尿細管上皮より発生することもありますが、主に集合管から発生します。集合管で特異的に発現するアルギニン・バソプレシン受容体2(AVPR2)の拮抗阻害剤であるトルバプタンは、ADPKDの治療薬として唯一承認されていますが、疾患の進行を止めることはできません。
これまでの研究で、ADPKD患者さん由来のiPS細胞から作製した腎尿細管嚢胞モデルがいくつか報告されています。これらのモデルを用いて嚢胞形成を抑制する候補化合物が同定されたものの、ADPKD動物モデルに対する治療効果は示されていません。ヒトiPS細胞から集合管オルガノイドを作製した報告もありますが、AVPR2などADPKDの集合管嚢胞形成に関与する分子を発現する発生段階に達していませんでした。さらに、集合管オルガノイドを用いてADPKDの嚢胞形成やトルバプタンの治療効果を再現した報告はありませんでした。
腎集合管の発生過程において、前駆組織である尿管芽(UB)は分枝を繰り返し、先端と幹という2つの異なるドメインを含む樹木状の構造を形成します。この過程で、先端が新たな先端と幹を生み出すことから、先端にある細胞が幹細胞として機能していることが示されています。これまでに研究グループは、ヒトiPS細胞を効率的に尿管芽オルガノイド(UBO)に分化させ、UBOを再構成することができる能力を持ったUB先端細胞(UBTC)コロニーを作製することに成功しています(CiRAニュース 2020年7月29日)。
本研究ではADPKDの原因遺伝子であるPKD1をゲノム編集により変異体(PKD1-/-)にしたiPS細胞から集合管オルガノイドを作製し、ADPKDにおける集合管で嚢胞が形成されるモデルを構築しました。
1. 集合管オルガノイドを利用したADPKDモデルの作製
Pkd1-/-変異を持つマウス胚は、UBの後期分枝期から集合管嚢胞を形成することが報告されています。ヒトでも同様であればPKD1-/-を持つUBTCから対応する発生段階で集合管へと誘導することで、集合管嚢胞を再現できると考えられます。以前の研究で作製していた、健常人由来ヒトiPS細胞を、ゲノム編集によりPKD1-/-としたiPS細胞を用いて、集合管オルガノイドにおける嚢胞の形成を調べました。すると、6週間以上拡大培養後に集合管へと誘導すると、嚢胞が自然に発生しました(Fig. 1)。
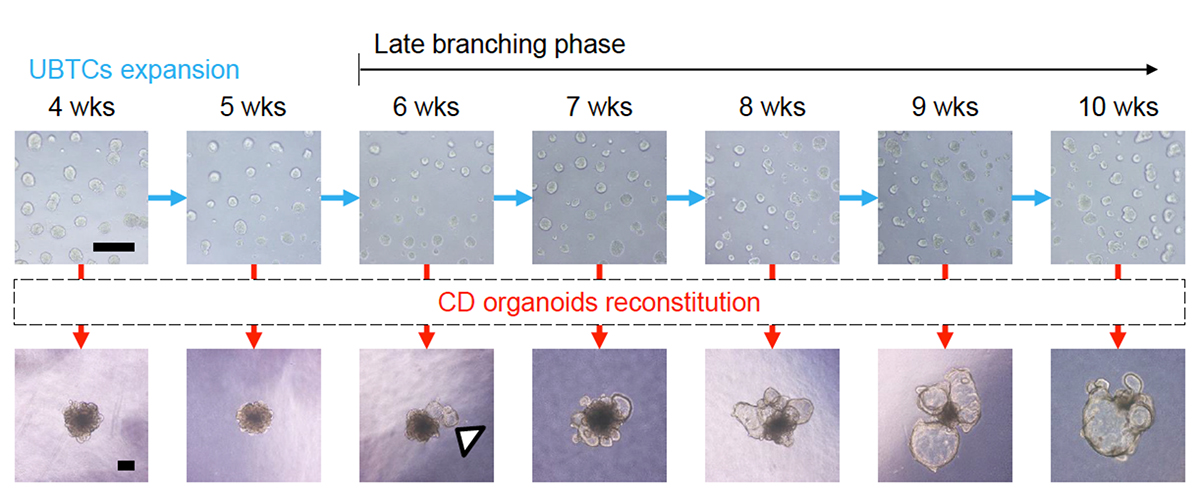
Fig. 1 拡大培養したUTBCと各培養期間から誘導した集合管オルガノイドの顕微鏡観察像
この集合管オルガノイドに、現在ADPKDの治療薬として使われているトルバプタンを作用させると、嚢胞のサイズは小さくなりました。
また、こうした集合管オルガノイドを活用したADPKDモデルを使って、一度に96種の薬剤の効果を測定することができるスクリーニング系を確立しました。
2. RAR作動薬は嚢胞増大を抑制する (in vitro)
確立したスクリーニング系を用いて、AVPにより拡大した嚢胞のサイズを、強力なRAR作動薬であるTTNPBや、オールトランス型レチノイン酸(ATRA)での処理が抑制することがわかりました(Fig. 2)。嚢胞抑制はRARシグナルを介していることが示唆されました。
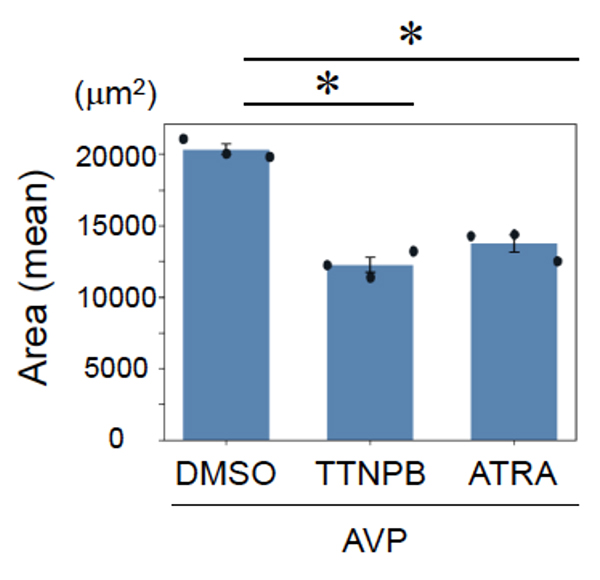
Fig. 2 嚢胞サイズの比較
3. ATRAはADPKDの進行を抑制する(in vivo)
ATRAはすでに他の疾患で治療薬として使用されています。ADPKDモデルマウスにおいてATRAが有効かどうかを検討しました。ADPKDモデルマウスは重篤な腎嚢胞を発症し、それに伴う腎不全により生後14日程度で死亡します。生後3日目のマウスに5または10 mg/kgのATRAを腹腔内注射し、生後9日目に解析を行いました。ATRA投与による体重減少は観察されませんでしたが、体重に対する腎臓の重さの割合(2KW/BW)は、ATRA投与群で対照群と比較して有意に減少しました(Fig. 3)。
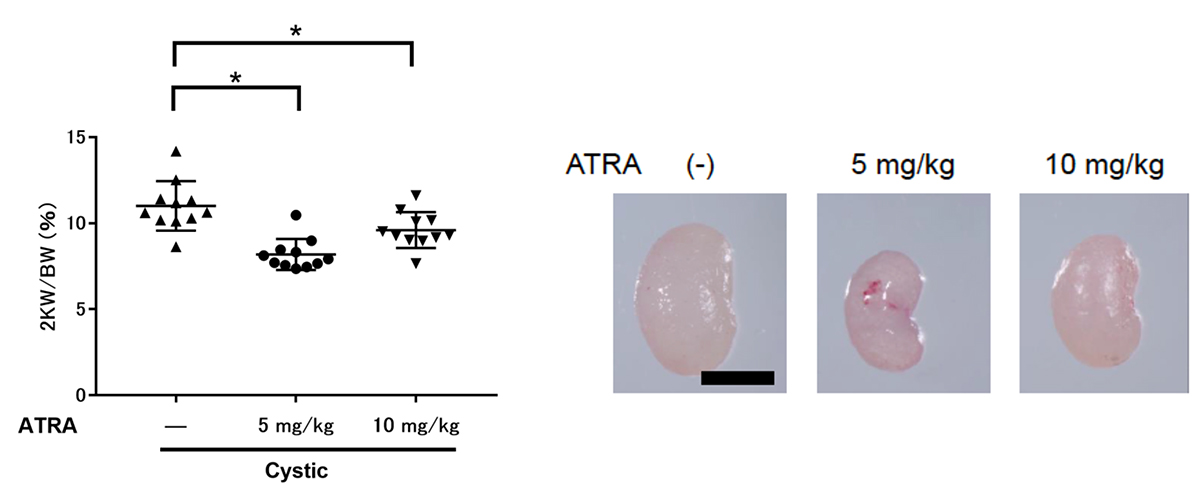
Fig. 3 腎臓のサイズと全体重に締める割合
また、腎臓の断面を観察すると、10 mg/kgのATRA処理群は対照群と比べて一部嚢胞の形成が抑制されていました(Fig. 4)。
さらに、マウスの血液検査において、10 mg/kgのATRA処理群は対照群と比べて腎機能の指標である血中尿素窒素値(BUN)の上昇が有意に抑制されていました。
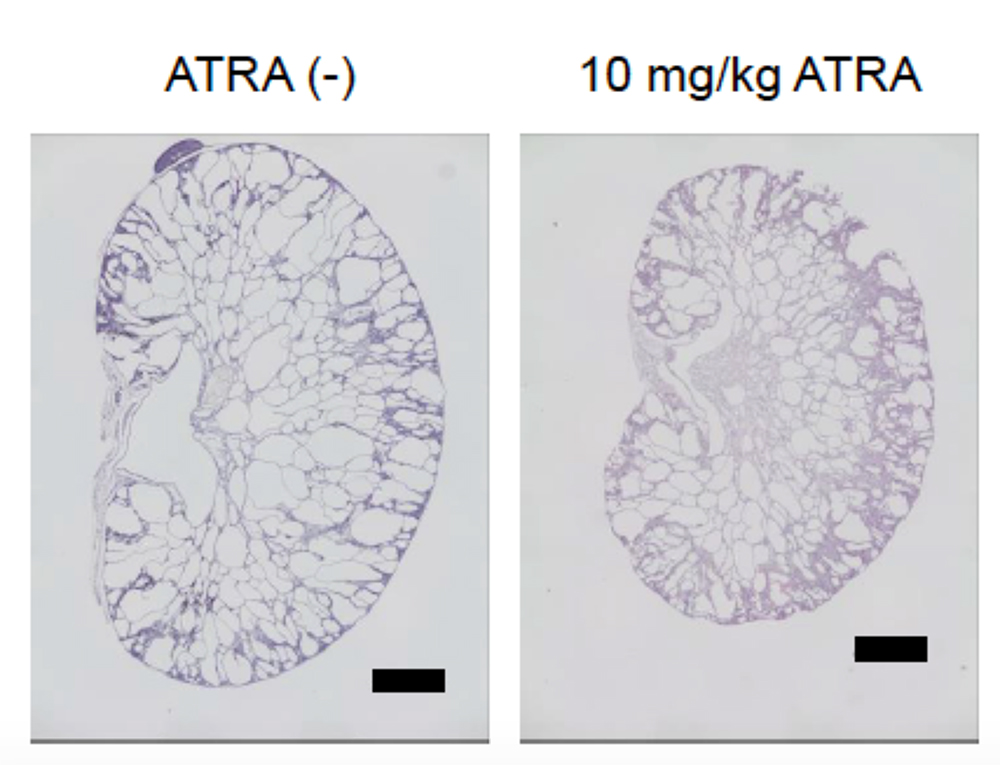
Fig. 4 腎臓の矢状断面図
以上の結果から、ATRA投与がin vitroおよびin vivo ADPKDモデルの両方において嚢胞形成と腎機能増悪を抑制する治療効果を発揮することが示唆されました。
今回の研究により、ヒトiPS細胞から作製した腎集合管オルガノイドを用いてADPKDのモデルを作製することに成功しました。このモデルを用いて、ADPKDの治療薬候補として、RAR作動薬を見出しました。実際にRAR作動薬のなかでも、白血病治療で用いられているATRAを用いて、マウスのADPKDモデルで嚢胞形成と腎機能増悪を抑制する効果が確認されました。
今後、今回見出した薬剤候補を用いて、リジェネフロ社が近く治験を開始する見込みです。
- 論文名
Human iPSC-derived renal collecting duct organoids model cystogenesis in ADPKD - ジャーナル名
Cell Reports - 著者
Shin-Ichi Mae1, Fumihiko Hattanda2, Hiroyoshi Morita1, Aya Nozaki1, Naoko Katagiri1,
Hanako Ogawa3, Kaori Teranaka3, Yu Nishimura3, Aoi Kudoh4, Sanae Yamanaka5, Kyoko Matsuse1, Makoto Ryosaka1, Akira Watanabe3,4, Tomoyoshi Soga5, Saori Nishio2, Kenji Osafune1*
*責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 北海道大学医学部・大学院医学研究科
- 株式会社CyberomiX
- 京都大学大学院医学研究科メディカルイノベーションセンター
- 慶應義塾大学先端生命科学研究所
本研究は、下記機関より支援を受けて実施されました。
- 大塚製薬株式会社
- 日本学術振興会 科研費 基盤研究C(19K08703)
- 国立研究開発法人 科学技術振興機構(JST)CREST(JPMJCR2123)
- 国立研究開発法人 日本医療研究開発機構(AMED)
(JP23bm0704072、JP22bm0104001、JP22bm0804013、JP23bm1123002) - ムーンショット型研究開発制度
- iPS細胞研究基金
注1)集合管
ネフロンは腎臓の中で、集合管と呼ばれる構造と連結している。集合管では尿細管から流れてきた尿から水分の再吸収が行われ、その後、尿が尿管から膀胱へと排泄される。ネフロンは後腎ネフロン前駆細胞(NP)から分化し、集合管、尿管および、膀胱の一部は尿管芽(UB)から分化する。
注2)オルガノイド
3次元的に試験管内で作られた小さな臓器のこと。
注3)常染色体優性多発性嚢胞腎(ADPKD)
両側の腎臓に多数の嚢胞が次第に発生・増大して、徐々に腎機能障害が進行する最も頻度の高い遺伝性嚢胞性腎疾患。腎臓以外にも、肝臓や膵臓などに嚢胞が生じることもある。全身の血管にも異常があり、高血圧、脳動脈瘤、心臓の弁異常を伴う頻度が高いことが分かっている。近年、トルバプタンという薬が嚢胞の増大を抑制することが注目されているが、根治的な治療法は現在のところない。
注4)尿管芽
胎生期の腎臓前駆組織の一つで、生体内では多数の枝分かれを繰り返して成熟し、将来尿の排泄路である集合管、下部尿路系などに分化する。























