
研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2026年5月13日
iPS細胞由来CAR導入キラーT細胞による固形がん動物モデルの治療効果を高めるサイトカインの組み合わせを発見 ―固形がん治療に向けた次世代型iCAR-T細胞の開発―
ポイント
- iPS細胞から作製したCAR-T細胞に、2種類のサイトカイン(IL-15, IL-21)を同時に発現させることで、固形がん克服を目指した次世代型iCAR-T細胞を作製した。
- 作製した細胞は、動物モデルにおいて、固形がんの塊(腫瘍)へ入り込み、長期間生存し、腫瘍の増大を抑え、個体の生存率を高め、その結果、従来のiCAR-T細胞を上回る治療効果を発揮した。
- IL-15とIL-21の相乗効果により、STAT1の活性化(リン酸化)を介して、CXCR3の発現が促進され、固形がんへの遊走能を強力に向上させる新たな仕組みを明らかにした。
- IL-15とIL-21の相乗効果により、iCAR-T細胞のメモリー機能が向上し、腫瘍内部で長く効果を発揮することを見出した。
- iPS細胞の利点を活かし、高品質・大量かつ安定供給が可能であり、免疫細胞療法が難しい固形がんに対しても広く有効で強力なiCAR-T細胞の実用化につながることが期待される。
石川晃大特命助教、金子新教授(CiRA臨床応用研究部門)らは、ヒトiPS細胞から作製した細胞傷害性T細胞(iPS-T細胞)にIL-15とIL-21という2種のサイトカイン注1)を産生させる遺伝子改変を行うことで、固形がんに対する抗腫瘍効果が大きく向上することを明らかにしました。
固形がんに対する免疫細胞療法の治療効果を向上させるには、①腫瘍内に移動(遊走・浸潤)するT細胞の増加、②長期にわたり増殖能を示す若いメモリーT細胞の維持が重要であることが報告されていましたが、これまで両方の基準を満たすiPS-T細胞の作製は困難でした。本研究では、がんを認識できるキメラ抗原受容体(CAR)注2)を発現したiPS-T細胞(iCAR-T細胞)の増殖に関与するIL-15を中心としたサイトカインの組み合わせに注目して研究を行いました。その結果、IL-15とIL-21を共発現することによってiCAR-T細胞内のSTAT1のリン酸化を介して、遊走に関わるケモカイン受容体注3)のCXCR3の発現が増加し、細胞の遊走が活発になることがわかりました。さらに、IL-15とIL-21を共発現したiCAR-T細胞は、腫瘍内に浸潤した後でも若いメモリーT細胞注4)のマーカーであるCD45RO、CD62L、CCR7の発現上昇が認められ、当該マーカー発現細胞は高い増殖能を有することが確認されました。本研究成果は、2026年5月12日(米国東部時間)に科学誌「Molecular Therapy」に掲載されました。
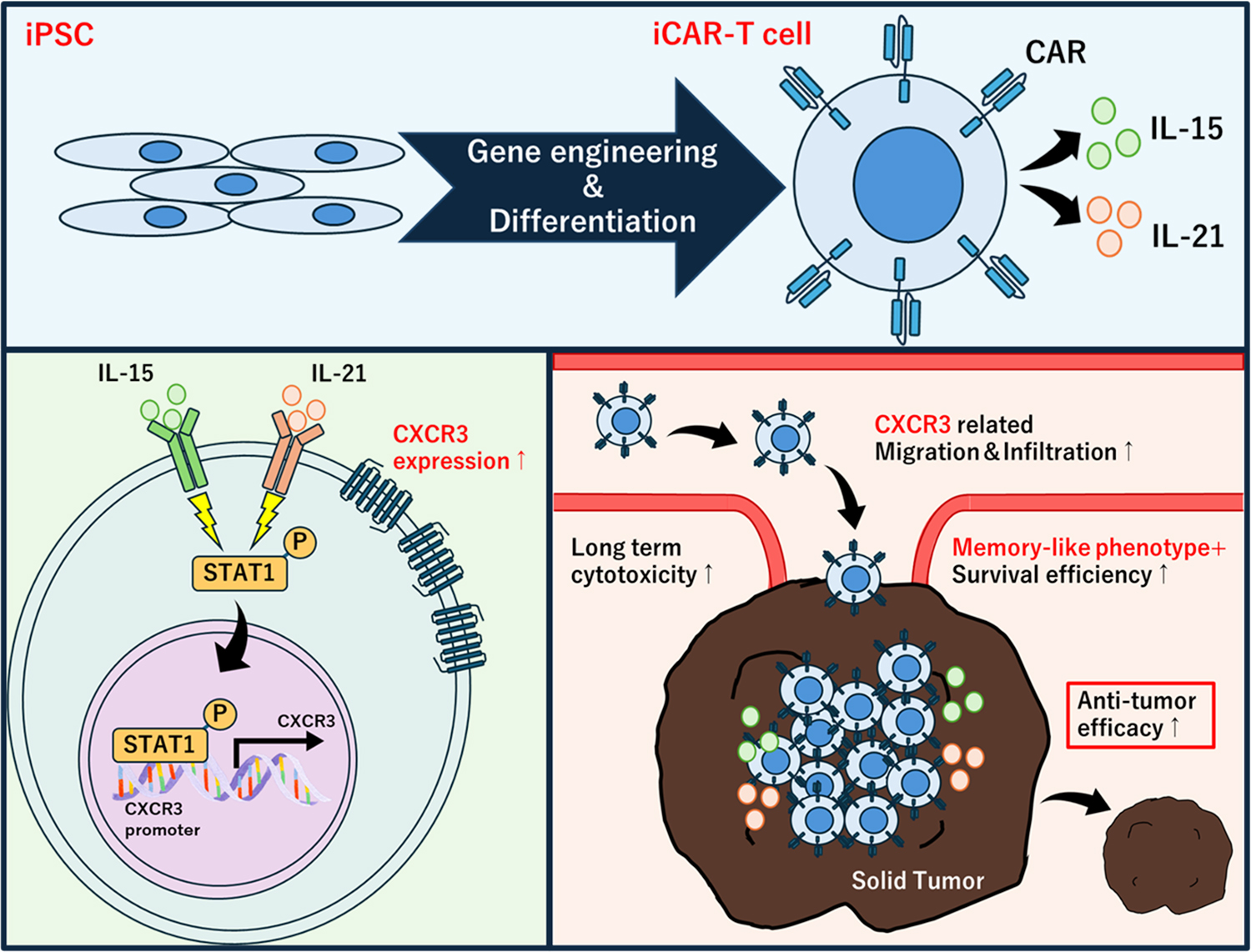
本研究の概要
現在、がん患者さんのT細胞をはじめとした免疫細胞を活性化させてがんを攻撃する「免疫療法」が注目されています。その代表格が、キメラ抗原受容体をT細胞に発現させたCAR-T細胞療法です。この治療法はB細胞性の血液がんには劇的な効果を示していますが、固形がんに対しては、十分な成果が得られていないのが現状です。その理由として、①がんの塊(腫瘍)の内部にT細胞が移動(遊走・浸潤)し、生き続けることが難しいこと、②がんの近くで増殖し続けることができない(疲弊)という課題、③患者さん自身の細胞を使うため、T細胞の数や質に個人差があることが考えられています。
こうした課題を解決するため、研究グループは、無限に増やすことができ、遺伝子操作も容易なiPS細胞に着目し、高品質なT細胞を大量かつ安定的に作る技術の開発に取り組んできました。T細胞の作製にiPS細胞を使うことで、T細胞の増殖能の低下(疲弊)や品質の個人差の課題を解消できると期待されています。研究グループはこれまでに、iCAR-T細胞にIL-15を発現させることで、血液がんへの効果を高めることに成功しています(CiRAニュース2021年1月18日)。しかし、固形がんに対する治療効果はまだ改善の余地が残されていました。
本研究では、iCAR-T細胞の機能を向上させる遺伝子の探索を行いました。その結果、「IL-15」と「IL-21」を共発現させることで、マウス体内の固形がんに対するiCAR-T細胞の攻撃力(細胞障害活性)が劇的に向上することを発見しました。さらに、IL-15とIL-21の組み合わせは、iCAR-T細胞が自らがん細胞へと遊走する能力を高めることで、腫瘍内部のiCAR-T細胞数の増加にもつながることを見出しました。腫瘍内部に入り込んだiCAR-T細胞は、若く、疲弊しておらず、攻撃力の高い状態を維持したまま、腫瘍の中で生き残ることも確認しました。本研究は、これまで治療が難しかった固形がんに対して、iPS-T細胞を用いたがん免疫細胞療法の新規研究開発に貢献することが期待されます。
1)サイトカイン発現iCAR-T細胞の開発と評価
研究グループは、作製したiCAR-T細胞にIL-15と他のサイトカインを組み合わせて発現させ、共培養したがん細胞を直接攻撃する「細胞傷害活性」を評価しました(図1A)。その結果、IL-15とIL-21を発現したiCAR-T細胞は、他の組み合わせと比較して長期にわたって細胞傷害活性が有意に高いことがわかりました(図1B)。さらに、がん細胞を皮下に投与し、腫瘍を形成したマウスに、IL-15とIL-21を共発現したiCAR-T細胞を投与したところ、腫瘍の増大が抑制され、マウスの生存率が改善することを確認しました(図1C, D, E)。
以上からIL-15とIL-21を組み合わせて発現させることにより、iCAR-T細胞が長期にわたって高い細胞傷害活性を発揮し、固形がんに対する治療効果を高めることがわかりました。
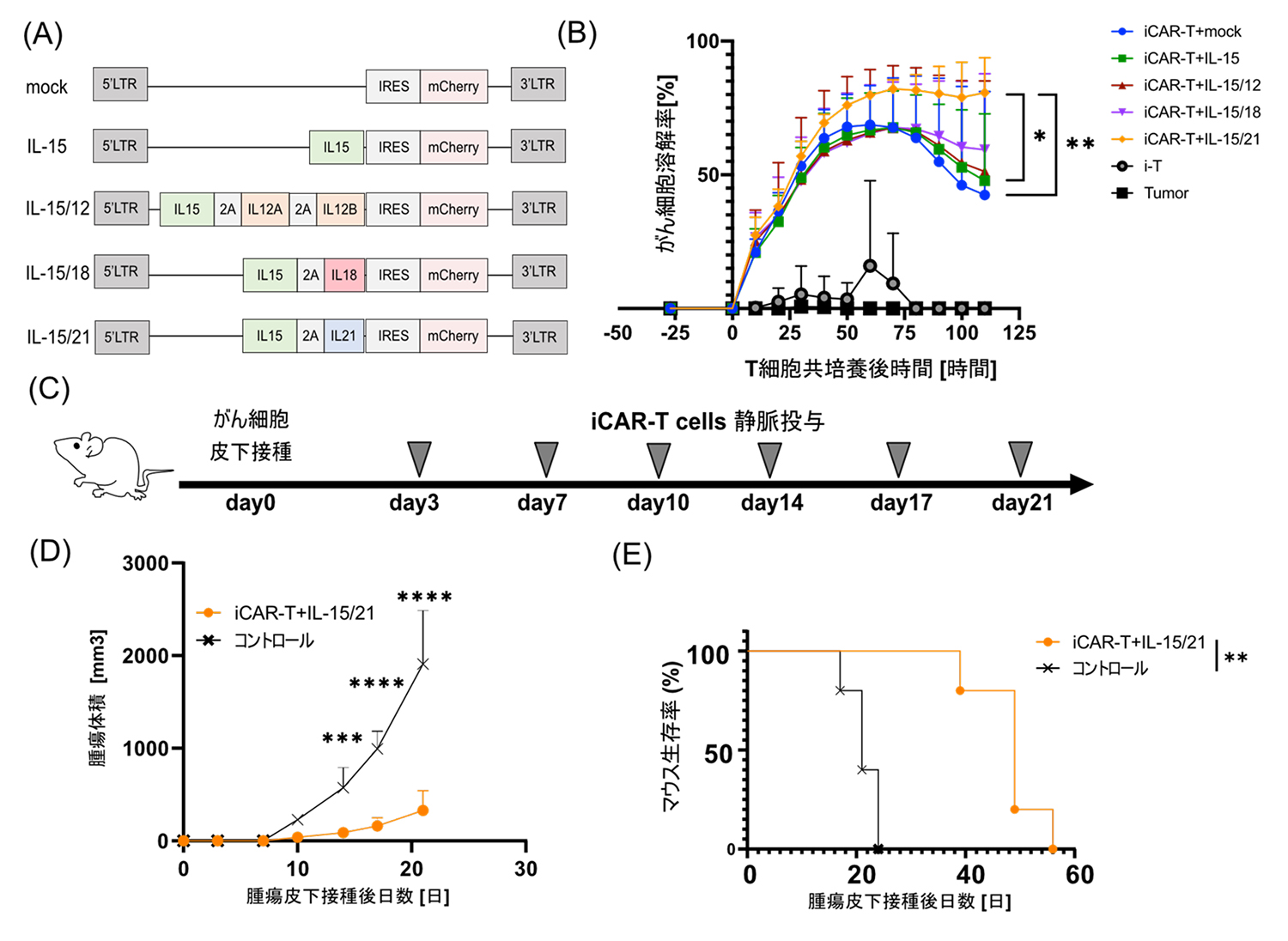
図1. IL-15とIL-21の組み合わせはiCAR-T細胞の固形がんへの攻撃力を高める
A:サイトカインを発現させるために使用したレトロウイルスベクターの概要。
B:時間当たりの細胞傷害活性能。
C:マウスへのiCAR-T細胞の投与スケジュール。免疫不全マウス注5)の皮下にがん細胞を投与(播種)し、腫瘍を形成させて実験に用いた(図2C、図4Aも同様)。
D:IL-15とIL-21を共発現するiCAR-T細胞投与後の腫瘍体積。
E:IL-15とIL-21を共発現するiCAR-T細胞投与後のマウス生存率。
2)IL-15とIL-21を共発現するiCAR-T細胞のCXCR3関連遊走能
次に、IL-15とIL-21を共発現するiCAR-T細胞が、固形がんに対して高い治療効果を発揮する仕組みを調べるために、がん細胞を培養した上清に対するiCAR-細胞の遊走能を評価しました。その結果、他のiCAR-T細胞と比べて、IL-15とIL-21を発現するiCAR-T細胞が、特に多く遊走しました(図2A)。そこで、細胞の遊走に関連するケモカイン受容体の発現を確認した結果、IL-15とIL-21を発現するiCAR-T細胞ではCXCR3といケモカイン受容体の発現が高いことがわかりました(図2B)。
研究グループはさらに、皮下に腫瘍を形成したマウスを用いてIL-15とIL-21を発現するiCAR-T細胞が腫瘍へと遊走し、内部へと入り込んだ(浸潤した)細胞数を評価しました(図2C)。その結果、iCAR-T細胞で発現しているCXCR3の機能を特異的に阻害する抗体(中和抗体)を投与すると、腫瘍に存在するiCAR-T細胞数が少なくなりました(図2D)。
以上から、IL-15とIL-21を発現させたiCAR-T細胞は、CXCR3の発現と関連する遊走能を向上させることで、腫瘍に浸潤したiCAR-T細胞数が増加することを見出しました。
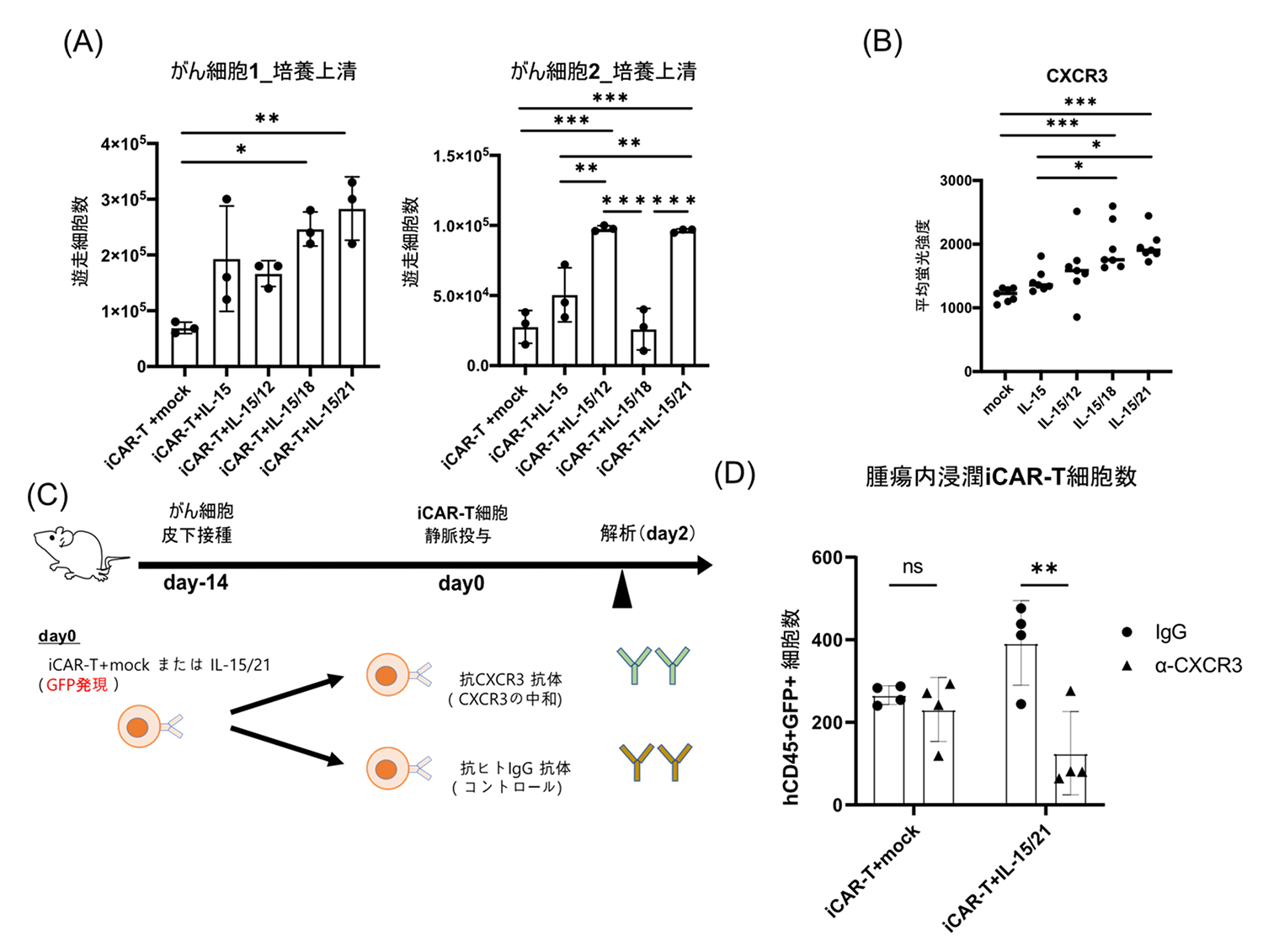
図2. IL-15とIL-21を共発現したiCAR-T細胞はCXCR3の発現による高い遊走能を発揮する
A:トランズウェル細胞遊走アッセイ注6)における、がん細胞培養上清に対する遊走細胞数の比較。がん細胞株のJHH7細胞(左)とskHep-1-GPC3細胞(右)の培養上清をそれぞれ用いた。
B:ケモカイン受容体(CXCR3)の発現量。
C:マウス(図1C注釈参照)にiCAR-T細胞と各種抗体を投与した(day0)。CXCR3特異的中和抗体(α-CXCR3)とCXCR3を認識しない抗体(IgG)をそれぞれ使用した。
D:腫瘍に浸潤したiCAR-T細胞数(投与2日後)。
3)IL-15とIL-21を発現するiCAR-T細胞はSTAT1のリン酸化によりCXCR3の発現が促進される
研究グループは、IL-15とIL-21の2種のサイトカインを発現させたiCAR-T細胞において、CXCR3の発現が誘導される仕組みを調べました。IL-15とIL-21は、JAK-STAT経路注7)と呼ばれるシグナル伝達経路(細胞内で行われる情報伝達経路)を通じてT細胞などを活性化することが報告されています。そこで、この経路の下流で遺伝子発現の制御を担う転写因子STATのリン酸化状態を調べました。その結果、IL-15とIL-21を発現させたiCAR-T細胞において、STAT1、STAT3、STAT5がリン酸化しており、特にSTAT1はIL-15とIL-21が共発現する場合に相乗的に有意にリン酸化されていることがわかりました(図3A,B)。
さらに、ChIP-qPCR法注8)を用いて、転写因子STAT1がCXCR3遺伝子のプロモーター領域に強く結合していることが確認されました(図3C)。そこで、ゲノム編集によりSTAT1遺伝子をノックアウトしたiPS-T細胞を作製し、CXCR3の発現を確認しました。その結果、STAT1をノックアウトしたiPS-T細胞ではCXCR3の発現が減少し、CXCR3に関連する遊走能も低下していることが確認されました(図3D)。
以上から、IL-15とIL-21を発現することでSTAT1、STAT3、STAT5がリン酸化され、特にSTAT1がCXCR3の発現を制御していることを初めて見出しました。
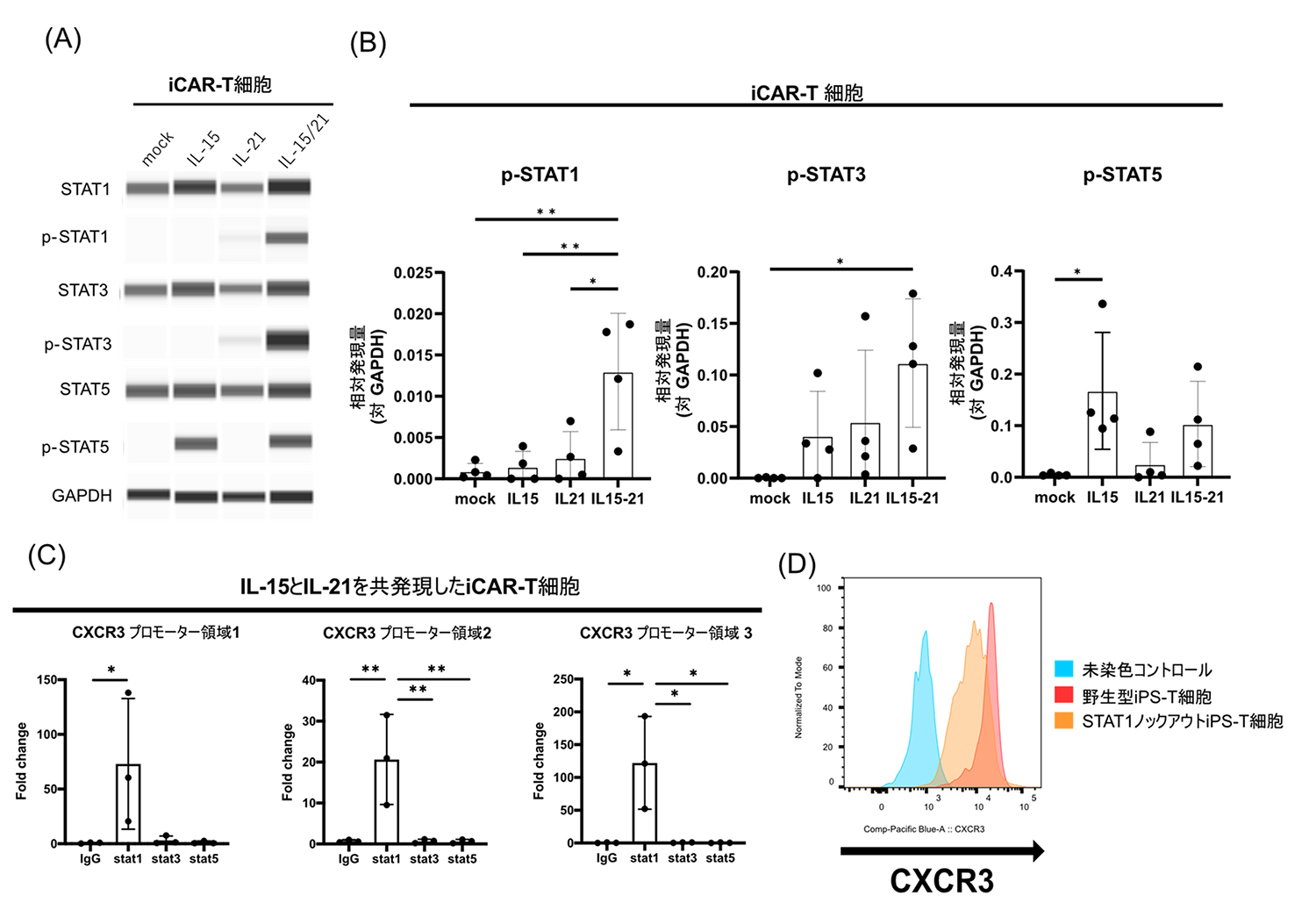
図3. iCAR-T細胞でのIL-15とIL-21の共発現がSTAT1をリン酸化し、CXCR3発現を制御する
A:ウェスタンブロットによるSTAT1、STAT3、STAT5の発現とリン酸化量。
B:Aの統計的解析。
C:ChIP-qPCRによるCXCR3プロモーター領域結合STATの評価。
D:STAT1ノックアウト細胞のCXCR3発現量。
A:ウェスタンブロットによるSTAT1、STAT3、STAT5の発現とリン酸化量。
B:Aの統計的解析。
C:ChIP-qPCRによるCXCR3プロモーター領域結合STATの評価。
D:STAT1ノックアウト細胞のCXCR3発現量。
4)IL-15とIL-21を発現するiCAR-T細胞は腫瘍内部で若いメモリー状態を維持する
研究グループは、IL-15とIL-21を発現したiCAR-T細胞により、固形がんに対する治療効果が向上した理由をさらに検証するために、腫瘍に浸潤したiCAR-T細胞を解析しました(図4A)。その結果、IL-15とIL-21を共発現させることで、腫瘍にiCAR-T細胞が有意に多く存在することがわかりました(図4B)。
また、腫瘍に浸潤したiCAR-T細胞の細胞表面マーカーを解析した結果、IL-15とIL-21を共発現させたとき、若いメモリーT細胞でみられるCD45RO、CD62L、CCR7を発現する細胞の割合が増えていました。若いメモリーT細胞は、腫瘍に存在するがん細胞に対して、免疫反応を長期的かつ持続的に発揮するために重要と考えられます。生体(末梢血)由来のCD8陽性CAR-T細胞でも同様の傾向を確認しました(図4C)。CD45RO、CD62L、CCR7を発現するiCAR-T細胞は、免疫反応を活性化するIL-2、IFN-γ、TNFαなどの炎症性サイトカインを複数発現し、増殖能ももつことがわかりました(図4D, E)。
最後に、シングルセルRNAシーケンス解析注9)により、腫瘍に浸潤したiCAR-T細胞の遺伝子発現パターンを解析しました。その結果、IL-15とIL-21を共発現するiCAR-T細胞は、他のiCAR-T細胞と異なる遺伝子発現パターンを示し、末梢血CD8陽性CAR-T細胞と似ていました(図4F)
以上から、IL-15とIL-21を発現させることにより、iCAR-T細胞から若いメモリーT細胞状態を維持する細胞集団が生じ、固形がんに対する高い治療効果に寄与していることがわかりました。
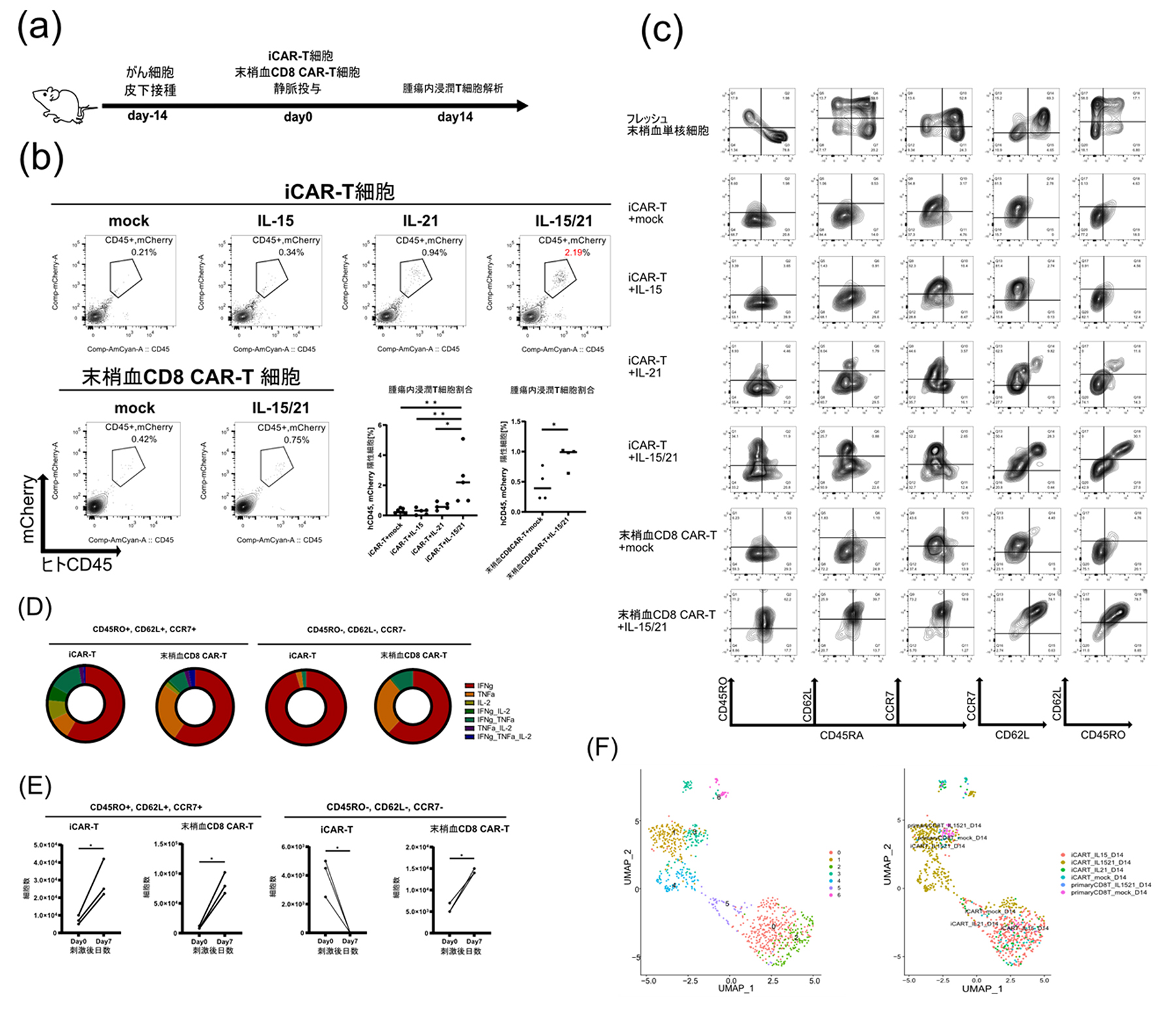
図4. IL-15とIL-21を共発現したiCAR-T細胞は若いメモリーT細胞状態を維持し、
固形がんに対する長期的かつ高い治療効果に貢献する
A:マウス(図1C注釈参照)への各種T細胞の投与スケジュール。
B:腫瘍に浸潤したiCAR-T細胞および末梢血由来CD8陽性CAR-T細胞の割合。
C:メモリーT細胞状態の指標となる遺伝子(CD45RO, CD62L, CCR7)の発現解析。
D:CD45RO, CD62L, CCR7発現細胞による炎症性サイトカインの発現割合。
E:CD45RO, CD62L, CCR7発現細胞の増殖細胞数。
F:腫瘍内浸潤iCAR-T細胞のシングルセルRNAシーケンス解析
A:マウス(図1C注釈参照)への各種T細胞の投与スケジュール。
B:腫瘍に浸潤したiCAR-T細胞および末梢血由来CD8陽性CAR-T細胞の割合。
C:メモリーT細胞状態の指標となる遺伝子(CD45RO, CD62L, CCR7)の発現解析。
D:CD45RO, CD62L, CCR7発現細胞による炎症性サイトカインの発現割合。
E:CD45RO, CD62L, CCR7発現細胞の増殖細胞数。
F:腫瘍内浸潤iCAR-T細胞のシングルセルRNAシーケンス解析
本研究では、iPS細胞から作製したiCAR-T細胞の機能を飛躍的に高めるサイトカインの最適な組み合わせを探索し、IL-15とIL-21という2つの物質を同時に導入することが、固形がんの治療において極めて有効であることを明らかにしました。
研究の結果、この組み合わせによって、特にSTAT1により媒介されるJAK-STATシグナル経路がiCAR-T細胞で相乗的に活性化され、がん細胞を感知するケモカイン受容体CXCR3の発現が促進され、腫瘍への遊走能が強力に向上すること、さらに、腫瘍の内部で若いメモリーT細胞状態を維持し、増殖能を保持することを突き止めました。これにより、これまでiCAR-T細胞の課題となっていた、固形がんへの遊走能と腫瘍内部での生存率が大幅に改善され、動物モデルにおいて強力な治療効果を確認することに成功しました。
本技術は、従来の細胞療法では太刀打ちできなかった、固形がんという難攻不落の壁を突破するための重要な鍵となります。また、遺伝子改変を行いやすく、無限に増やすことのできるiPS細胞を原料とすることで、患者さんが必要とするときに、高品質な治療細胞を大量かつ安定的に提供できる「オフザシェルフ(既製品)型」の次世代免疫療法としての活用が可能です。
今後は、IL-15とIL-21を発現させたiCAR-T細胞の臨床応用を目指したさらなる検証を進めるとともに、これまで免疫療法が効きにくかった多くのがん患者さんに対する、新たな治療アプローチの開発につながることが期待されます。
- 論文名
IL-15 and IL-21 Synergy Improves Antitumor Efficacy of iPSC-Derived Cytotoxic T Cells in Solid Tumors - ジャーナル名
Molecular Therapy - 著者
Akihiro Ishikawa1, Masazumi Waseda1, Yohei Kawai1, Tomoko Ishii1, Shin Kaneko1,2,*
*:責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 筑波大学トランスボーダー医学研究センター
本研究は、下記機関より支援を受けて実施されました。
-
日本医療研究開発機構(AMED)
- 再生医療実現拠点ネットワークプログラム
「再生医療用iPS細胞ストック開発拠点」
「次世代型ヒト人工染色体ベクターによるCAR交換型高機能再生T細胞治療の開発拠点」- 革新的がん医療実用化研究事業
「GPC3発現手術不能進行・腹膜播種卵巣明細胞腺癌を対象としたヒト同種iPS 細胞由来GPC3-CAR 再生自然キラーリンパ球(ILC/NK)の安全性、忍容性および薬物動態を検討する第I相臨床試験」 - シノビ・セラピューティクス株式会社
- iPS細胞研究基金
注1)サイトカイン
細胞同士が情報をやり取りするために出す「メッセージ物質」の総称。多くの種類があり、「もっと増えろ」「がんを攻撃しろ」といった命令を伝える。今回の研究で使われたIL-15やIL-21もサイトカインの一種。
注2)キメラ抗原受容体(CAR)
がん細胞を認識するためにT細胞の表面に人工的に発現させる受容体。T細胞ががん細胞を特異的に見つけ出し、認識するための高性能なアンテナとして機能し、がん細胞に対する攻撃力を高める。英語では、Chimeric Antigen Receptorといい、CARはその略称。
注3)ケモカイン受容体
T細胞などが特定の場所へ移動(遊走)するために、がん細胞などが放つ「ケモカイン」という物質を感知するセンサーとしてはたらく。
注4)メモリーT細胞
T細胞受容体に特異的な抗原を提示され活性化することで、ナイーブT細胞からエフェクターT細胞へと変化する。エフェクターT細胞の一部は、長期間体内に残り続けるメモリーT細胞となる。メモリーT細胞は、再度、抗原を認識すると、短期間に効率よく増殖し、免疫反応を再開できるため、がんの再発の防止や、治療効果の持続に寄与する。
注5)免疫不全マウス
生まれつき免疫の働きが弱く、異物(人間の細胞など)を排除できない実験用マウス。マウスと種の異なるヒトの治療細胞やがん細胞を移植しても拒絶されないことから、個体での治療の効果を確かめることができる。
注6)トランズウェル細胞遊走アッセイ
細胞がどれくらい移動(遊走)できるかを調べる方法。薄い膜で隔てられた培養容器を使い、一方に存在する物質に反応して、自力で膜を通り抜けて移動した細胞数により評価する。
注7)JAK-STAT経路
細胞の表面に届いたサイトカインなどの情報を細胞内の核へ伝えるシグナル伝達経路の一つ。JAK-STAT経路は、細胞の増殖や分化などにかかわることが知られている。
注8)ChIP-qPCR法
目的のタンパク質(STAT1, STAT3, STAT5)と結合するゲノム上のDNA断片を回収し(クロマチン免疫沈降法:Chromatin Immunoprecipitation, ChIP)、qPCRによって結合するゲノム領域を特定する実験手法。
注9)シングルセルRNAシーケンス解析
複数の細胞をひとまとめにして解析する従来法に対して、一つひとつの細胞ごとに(=シングルセル)、ゲノム上の遺伝子発現パターンを網羅的に分析する技術。従来の解析を、遠くから撮ったぼやけた集合写真だとすると、シングルセル解析は最高画質のカメラで一人ひとりの表情までクローズアップして撮り分ける高解像度なデータを取得できる技術である。多様なT細胞の集団の遺伝子発現を平均化することなく、一つひとつのT細胞の遺伝子発現パターンの分布や傾向を知ることができる。























