
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2015年3月23日
患者さん由来のiPS細胞を用いて脊髄性筋委縮症の病態を再現
吉田路子研究員、斎藤潤准教授、中畑龍俊教授ら(CiRA臨床応用研究部門)の研究グループは、脊髄性筋萎縮症(spinal muscular atrophy : SMA)患者さんの皮膚の細胞から樹立したiPS細胞を用いて、SMAの神経筋接合部注1における病態を再現し、それを既存の治療薬で回復させることに成功しました(図1)。この研究は、京都大学iPS細胞研究所と京都府立医科大学大学院医学研究科小児発達医学教室の共同研究によって行われました。
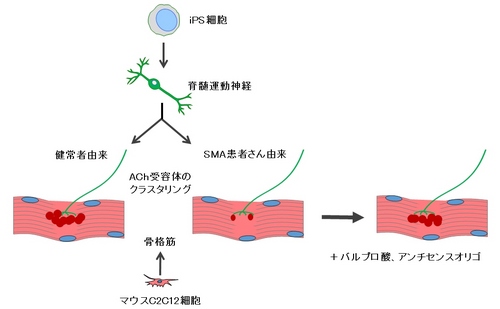
図1. 研究の概略
SMA患者さんiPS細胞由来の運動神経を用いると、アセチルコリン受容体のクラスタリングが
障害され、バルプロ酸やアンチセンスオリゴの投与により回復する。
SMAはSMNタンパク質注2の減少によって、筋肉の萎縮や筋力の低下がおこる神経筋疾患です。最重症型の1型SMA患者さんは、乳児期に呼吸不全をきたし、人工呼吸療法が必要となり、有効な治療法はありません。従来SMAは、運動神経の細胞死によって、支配される筋肉の萎縮と筋力の低下が引き起こされて発症すると考えられてきましたが、近年、SMAのモデルマウスを用いた研究で、運動神経細胞死よりも先に、神経筋接合部の形成障害が観察されることが報告されています。しかし、ヒトの患者さんでも同様に神経細胞死より神経筋接合部の異常が先行するのか、また、その場合なぜ神経筋接合部病変が起こるのか、などについては、十分に解明されていませんでした。
そこで、吉田路子研究員らは神経筋接合部に着目し、iPS細胞から分化させた運動神経とマウスの筋細胞株を混ぜて培養することによって、神経筋接合部の形成初期に起こるアセチルコリン受容体のクラスタリング注3を再現することに成功しました。1型SMA患者さんのiPS細胞由来の運動神経を用いて解析を行うと、このアセチルコリン受容体のクラスタリングが著しく障害されており、確かに神経筋接合部に病変が存在しうることがわかりました(図2)。また、神経筋接合部の異常は、運動神経が原因となって起きることがわかりました。
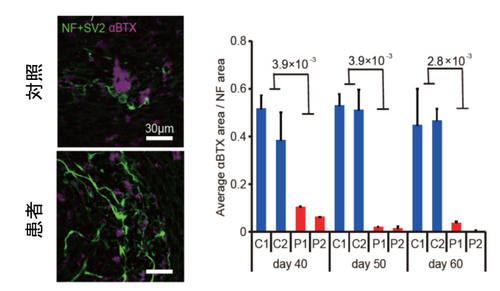
図2.神経筋接合部の形成
患者さんでは、赤紫で示すアセチルコリン受容体のクラスタリングの量や大きさが低下している。
右のグラフはそれを定量化したもの。C1, C2:対照細胞。P1, P2:患者細胞。
過去にいくつかの研究グループが、1型SMA患者さんのiPS細胞由来の運動神経は細胞死を起こしやすいことを報告していますが、今回の研究では神経筋接合部形成以前には患者さんの過剰な運動神経細胞死は観察されず、運動神経の細胞死ではなく機能異常が先行し、これが神経筋接合部形成障害を引き起こすことが示唆されました。
また、SMNタンパク質量を増加することが知られているバルプロ酸注4やアンチセンスオリゴヌクレオチド注5であるモルフォリノ注6を培地に加えることによって、上記の異常が改善されたことから、このSMAの神経筋接合部モデルは薬効評価にも使用できることが示されました(図3)。このモデルを応用することにより、SMAの病態解析に加え、治療薬の開発が進むことが期待されます。
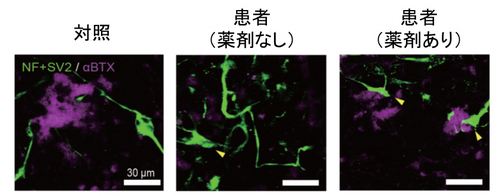
図3.SMA患者さん由来神経細胞に対する薬剤の効果
患者細胞にモルフォリノを添加すると、赤紫色で示した神経筋接合部様構造が回復する。
- 論文名
Modeling the Early Phenotype at the Neuromuscular Junction of Spinal Muscular Atrophy Using Patient-Derived iPSCs - ジャーナル名
Stem Cell Reports Vol. 4 1-8 April 14, 2015 - 著者
Michiko Yoshida, Shiho Kitaoka, Naohiro Egawa, Mayu Yamane, Ryunosuke Ikeda, Kayoko Tsukita, Naoki Amano, Akira Watanabe, Masafumi Morimoto, Jun Takahashi, Hajime Hosoi, Tatsutoshi Nakahata, Haruhisa Inoue, and Megumu K. Saito.
本研究は、主として下記の機関より資金的支援を受けて実施されました。
- 日本学術振興会 科学研究費補助金
- 文部科学省 「再生医療の実現化プロジェクト」
- 厚生労働省 難治性疾患克服研究事業
- JST 再生医療実現拠点ネットワークプログラム 「iPS 細胞研究中核拠点」
- JST 再生医療実現拠点ネットワークプログラム 「疾患特異的iPS細胞を活用した難病研究」
注1 神経筋接合部
脊髄運動神経とその支配を受ける骨格筋がアセチルコリンを介して信号の伝達を行う部位。
注2 SMN(survival motor neuron: 生存運動神経)タンパク質
スプライシング(DNAの遺伝情報がmRNAに転写される際に不要なものを切り離して編集すること)を担うRNA結合タンパク質に作用するタンパク質。SMNタンパク質量が減少することによりSMAを引き起こすと考えられている。
注3 アセチルコリン受容体のクラスタリング
神経筋接合部を形成する際に、筋肉表面にあるアセチルコリンの受容体が局所に集まる現象。
注4 バルプロ酸
SMNタンパク質量を増やすことが知られている薬剤。抗てんかん薬として広く使われている。
注5 アンチセンス・オリゴヌクレオチド
アンチセンス・オリゴヌクレオチドは、目的の配列に相補的な一本鎖のDNAまたはRNAである。15〜20程度の短い鎖長のもので、相補的なRNAと結合することにより、特異的な遺伝子の発現を制御する。
注6 モルフォリノ
アンチセンスオリゴヌクレオチド作用により、SMN2遺伝子のスプライシングを変化させてSMNタンパク質量を増やすことが報告されている化合物。























