
研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2025年8月25日
ヒトiPS細胞から胸腺上皮細胞を作製―ヒトナイーブT細胞の再生に向けた技術基盤を開発―
ポイント
- ヒトiPS細胞から成熟した胸腺上皮細胞(iTEC)を作製することに成功した。
- iTECは、T細胞に抗原提示を受ける能力を賦与する皮質上皮細胞と、自己寛容を担う髄質上皮細胞を含む、多様な上皮細胞集団から構成されていた。
- iTECは、ヒトT前駆細胞と共培養したオルガノイドを作製すると、多様な反応性をもつナイーブT細胞注1)への分化を支持することができた。
- 今後、ヒト胸腺の発生や小児先天性無胸腺症や胸腺低形成症候群を試験管内で再現するモデルとして、またヒトT細胞再生のための新たな医療応用の基盤技術となることが期待される。
プレテマー・ヤン特定拠点助教、濵﨑洋子教授(CiRA未来生命科学開拓部門)らのグループは、ヒトのiPS細胞から成熟した胸腺上皮細胞を試験管内で分化誘導する方法を初めて開発しました。
「胸腺」は、病原体やがんなどのさまざまな異物に対する免疫応答の中心となる「T細胞」を産生する重要な臓器です。胸腺は皮質と髄質と呼ばれる領域に大きく分かれ、機能の異なる種類の胸腺上皮細胞が存在します。T前駆細胞はこれらの上皮細胞と相互作用することで、異物を認識し、かつ自己を攻撃しないT細胞(ナイーブT細胞)へと分化します。
本研究では、胸腺組織の発生過程にみられるシグナル伝達経路の働きを模倣することで、ヒトiPS細胞から、実際のヒト胸腺に類似したさまざまなタイプの成熟した胸腺上皮細胞を試験管内で作製することに成功しました。また、ヒトT前駆細胞をiPS細胞由来の胸腺上皮細胞と共培養してオルガノイドを作製すると、さまざまな反応性をもつナイーブ型T細胞集団に分化しました。すなわち、胸腺機能を試験管内で再現できることが分かりました。
本分化誘導系は今後、ヒト胸腺の発生や先天性無胸腺症・胸腺低形成症候群のメカニズムを詳細に解明するための新たな研究ツールになると考えられます。また、上述した生まれつき胸腺が形成されない疾患でみられる重度の免疫不全や、加齢や各種治療後のT細胞数減少の克服に向けたT細胞再生のための新たな技術基盤となることが期待されます。
この研究成果は2025年8月25日(英国時間)に、国際学術誌「Nature Communications」でオンライン公開されました。
胸腺は、未熟なT細胞(T前駆細胞)の分化・選択を支持し、体内を循環するT細胞を産生する獲得免疫システム構築に必須の臓器です。したがって、生まれつき胸腺が欠損すると(先天性無胸腺症)T細胞がほとんどできず、死に至る免疫不全となります。
胸腺では、まず皮質の上皮細胞が発現する自己のMHC分子注2)と自己ペプチドの複合体がT前駆細胞と相互作用し、自己MHCから抗原提示をうける能力をもつT前駆細胞(=何らかの抗原を認識できる細胞)が選ばれます(正の選択)。この最初の選択に合格した~10%ほどの細胞が、髄質に移行します。髄質の上皮細胞は、体内にあるさまざまな自己抗原を発現しており、これらに強く反応性する(=自己反応性をもつ)T前駆細胞は、髄質で除去されます(負の選択)。この過程は、自己免疫疾患を防ぐ重要なしくみです(自己免疫寛容)。このように、胸腺の皮質および髄質の上皮細胞とT前駆細胞が相互作用することで、さまざまな異物に反応し、かつ自分自身の細胞を攻撃しない、ナイーブT細胞集団が作られます。胸腺は、このように重要な役割をもつにもかかわらず、思春期以降はサイズが徐々に小さくなり、機能が低下します(胸腺退縮)。これは、加齢にともなう免疫機能低下の一因になると考えられています。
ヒトiPS細胞から胸腺上皮細胞を分化誘導することで、このユニークな機能をもつ胸腺上皮細胞が分化する過程、さらにヒトの体内で多様な抗原特異性をもつナイーブT細胞集団が作られる過程を試験管内で詳細に調べることができると考えられます。しかし、T前駆細胞からさまざまな抗原に対する反応性をもつT細胞へ分化させる能力をもつ成熟した胸腺上皮細胞を、ヒトiPS細胞やES細胞から試験管内で作製する方法はこれまで報告されていませんでした。
また、キラーT細胞はがん細胞やウイルス感染細胞を破壊し排除する働きをもつことから、新たながん治療のアプローチとして、がん細胞に反応するT細胞をヒトiPS細胞から大量に作製する研究開発が国内外で活発に行われています。しかしながら、患者さん自身のT細胞にがん抗原への特異性をもたせたCAR-T細胞療法においてすでに報告されているように、突然変異によりがん細胞が標的抗原を発現しなくなることで免疫逃避が起き、高い確率で再発が起こることが課題となっています。胸腺機能を再構築することができれば、多様な反応性をもつT細胞を再生することが可能となるため、こうした抗原特異的T細胞再生療法がもつ課題に対して一つの解決策の候補を提示することが可能となります。
このような背景のもと、本研究では、ヒトiPS細胞から成熟した胸腺上皮細胞(induced thymic epithelial cell; iTEC)を誘導する培養法を確立し、iTECを用いてヒトの免疫システムが本来有する多様な反応性をもつT細胞を再生する技術基盤を開発しました。
1)ヒトiPS細胞から成熟した胸腺上皮細胞(iTEC)を完全に試験管内で作製
研究グループは、ヒトiPS細胞から分化誘導7日目の細胞(前方前腸内胚葉)に、ビタミンAの代謝産物であるレチノイン酸を添加することで、胸腺上皮細胞のマスター制御因子であるFOXN1の発現が28日目頃に誘導されることを見出しました(図1A, B)。また、レチノイン酸の量は多すぎても少なすぎてもFOXN1の発現は誘導されませんでした(図1C)。厳密にコントロールされた量のレチノイン酸によりHOXA3の遺伝子発現が一定量誘導されることで、咽頭内胚葉(将来胸腺になる場所)が分化すると考えられます。さらに、その後あらゆる添加物を除き基礎培地のみで培養を継続することで、皮質と髄質の胸腺上皮細胞関連遺伝子を発現する細胞へと自発的に分化することが分かりました。また培養皿の中で、皮質と髄質のような領域が形成されている像が観察されました(図1D)。80日目頃には成熟した胸腺上皮が発現する分子(HLA-DR)注3)がFOXN1陽性の胸腺上皮細胞に発現してくることが分かりました(図1E)。

図1
A:ヒトiPS細胞から胸腺上皮細胞(iTEC)への分化誘導の過程。
B:誘導した各時点の細胞の様子(明視野)。
C:レチノイン酸の濃度とHOXA3およびFOXN1の遺伝子発現誘導との関係。
D:皮質と髄質の胸腺上皮細胞で発現するタンパク質(皮質:PSMB11、髄質:KRT5)の免疫染色。2つの領域に分かれている。
E:FOXN1が発現すると赤い蛍光(mCherry)を発するレポーターiPS細胞株から分化誘導した胸腺上皮細胞(FOXN1mCherry)と成熟マーカー(HLA-DR)の染色。
2)iTECを用いたオルガノイド形成によるナイーブT細胞の分化誘導
次に、ヒト胸腺から単離したT前駆細胞(CD4/8ダブルポジティブ:DP細胞)とiTEC(培養37日のFOXN1陽性細胞)を混合して、胸腺組織を再現したオルガノイドを形成し、14日間培養しました(図2A)。その結果、コントロールがDP細胞の状態にとどまっているのに対し、iTECと共培養すると、CD4/8両陽性のDP細胞からCD4単陽性(CD4+:ヘルパーT細胞系列)およびCD8単陽性(CD8+:キラーT細胞系列)へと効率よく分化することが示されました(図2B)。また、これらの細胞は胸腺での通常の分化過程でできるナイーブ型の表現型を示すことが確認されました。特に、iTECがCD4+ T細胞の選択に必要なクラスII MHC分子(HLA-DRなど)を高発現したことで、これまで技術的に難しいとされてきた試験管内でのCD4+ T細胞への分化が可能になったと考えられます。また、T前駆細胞から分化したT細胞は、多様なT細胞受容体をもつことが確認されました。以上のことから、iTECがさまざまな抗原に反応するナイーブT細胞の分化を支持できる可能性が示唆されました。
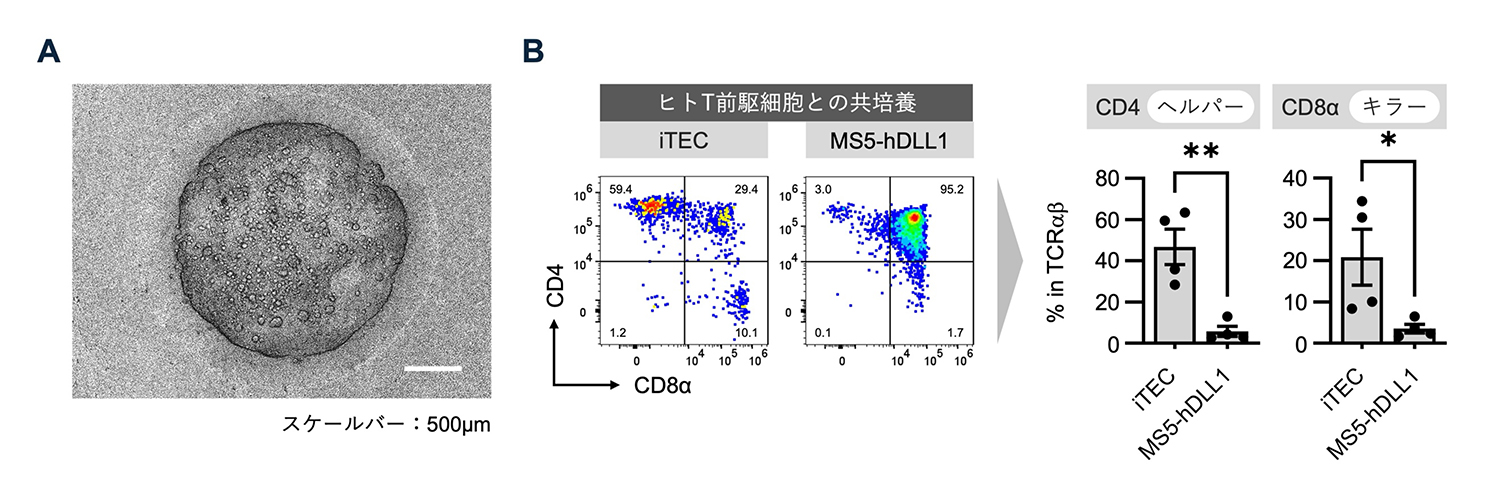
図2
A:iTECとヒトT前駆細胞を共培養したオルガノイド。
B:T前駆細胞(DP細胞)とiTECとの共培養14日後のフローサイトメトリ解析結果。CD45+CD3+TCRαβ+ 分画におけるCD4/8の割合(左)。TCRαβ+ 分画におけるヘルパーT細胞系列(CD4+SP)とキラーT細胞系列(CD8+SP)の割合をグラフ化した(右)。iTECの比較対照として、DP細胞への分化誘導能が高いhDLLを発現するマウス間葉系細胞株(MS5-hDLL1)を用いた。
3)iPS細胞から胸腺上皮細胞への分化過程とサブセット多様性の解析
iPS細胞から成熟した胸腺上皮細胞(iTEC)へと分化する過程の細胞を経時的に採取し、単一細胞ごとに網羅的に遺伝子発現パターンを解析しました(図3A)。その結果、皮質上皮細胞に加えて、いくつかの異なるタイプの髄質上皮細胞の集団に分化していることが明らかになりました(図3B)。これらの細胞集団は、生体の胸腺上皮細胞を同様に解析した結果の分布と重なることから、ヒト胸腺に実在するさまざまなタイプの胸腺上皮細胞集団が分化したと考えられました。
さらに、各タイプの胸腺上皮細胞系列が、分化誘導の過程でどのように分岐したのかを推定する解析を行いました(図3C)。その結果、髄質上皮細胞(mTEC)の一部の集団は、胸腺上皮細胞のマスター制御因子であるFOXN1を発現する前段階の咽頭内胚葉(PE)から分岐する可能性が示唆されました。胸腺髄質では、自己寛容を誘導するためにさまざまな自己抗原を発現するだけでなく、体内にある実際の細胞を模倣した擬態(mimetic)胸腺髄質上皮細胞注4)が存在することが最近明らかとなり注目されています。この結果は、胸腺髄質にきわめて多様な上皮細胞が存在するメカニズムを解明するための新たな手がかりとなることが期待されます。
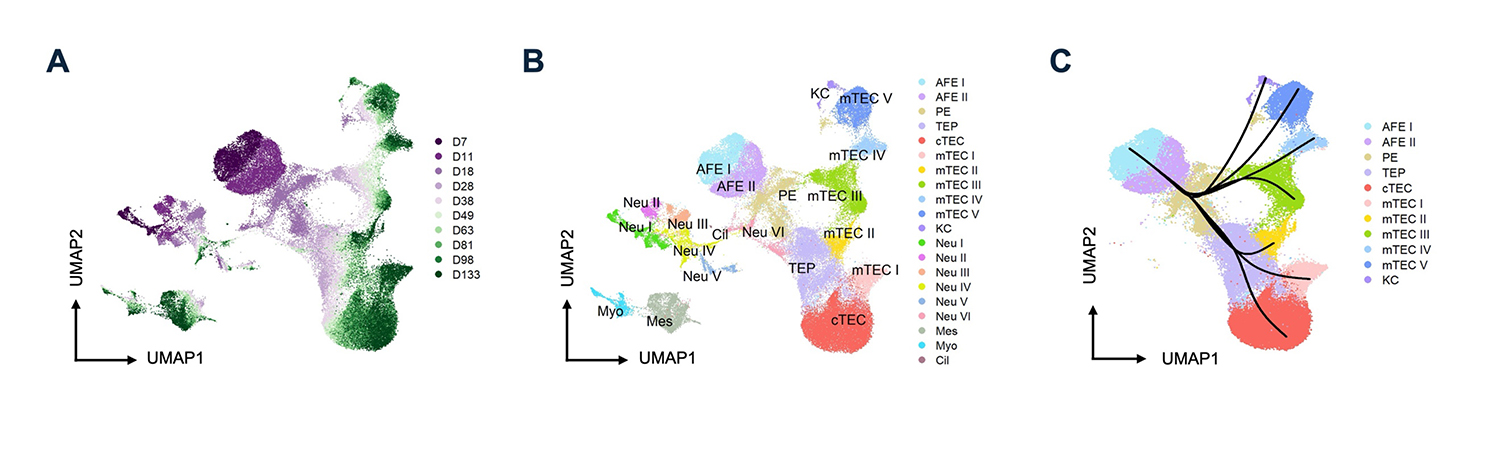
図3
A:ヒトiPS細胞から分化7日後(D7)から分化133日後(D133)までの各時点の細胞を用いて、一細胞単位で遺伝子発現パターンを網羅的に解析し、細胞集団の分布として可視化した結果。
B:Aの細胞の分布図を、遺伝子発現パターンから対応する細胞種ごとに集団を同定した結果。AFE:前方前腸内胚葉、PE:咽頭内胚葉、TEP:胸腺上皮前駆細胞、cTEC:皮質の胸腺上皮細胞、mTEC:髄質の胸腺上皮細胞。
C:Bの細胞の分布図に、遺伝子発現パターンから推定される細胞群の分化過程の経路を示した図。
4)T前駆細胞との共培養により自己寛容に必要な髄質上皮細胞も成熟
本分化誘導培養系では、皮質上皮細胞に比べて髄質上皮細胞が未成熟な傾向にあり、胸腺髄質上皮細胞がさまざまな組織自己抗原を発現するために必要な転写因子AIRE(ヒトで欠損すると100%自己免疫疾患を発症)は発現誘導されていませんでした。AIREの発現や髄質上皮細胞の成熟にはT前駆細胞からのシグナルが必要であることから、研究グループはT前駆細胞との共培養後にはAIRE が発現すると仮定しました。そこで、iTECとT前駆細胞の共培養によるオルガノイド形成後の細胞を用いて再度、単一細胞遺伝子発現解析を行いました。その結果、髄質上皮細胞の一部のAIREの発現に加え、さらに共培養前には存在しなかった、神経組織の自己抗原NEUROD1 を発現する擬態胸腺髄質上皮細胞に一部が分化していることを確認しました(図4A,B)。さらに、制御性T細胞注5)に似た遺伝子発現を示す細胞も確認されました。以上のことから、iTECは自己寛容の成立にも寄与する可能性が示唆されました。
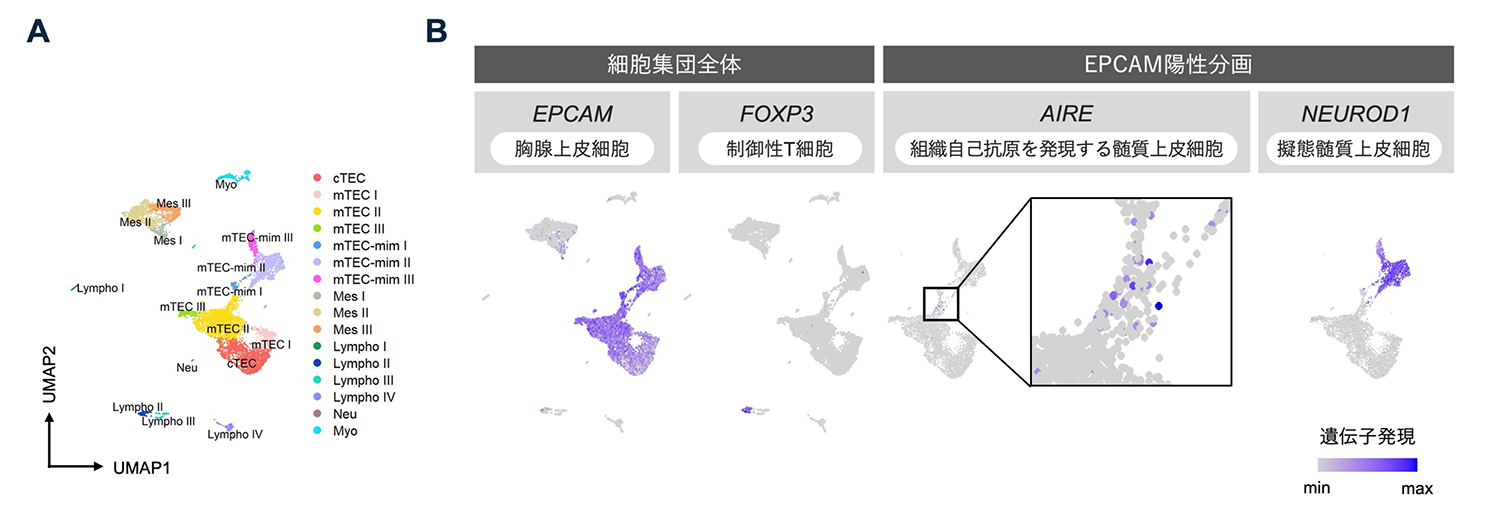
図4
A:iTECとヒトT前駆細胞の共培養によるオルガノイド形成の2週間後、一細胞単位で遺伝子発現パターンを網羅的に解析し、細胞種ごとに集団を同定した結果。
B:Aの分布に、EPCAM、FOXP3、AIRE、NEUROD1の遺伝子発現を示した図。AIRE、NEUROD1は、胸腺上皮細胞に相当するEPCAM陽性分画の各細胞の遺伝子発現を示す。
本研究では、胸腺の皮質や髄質に存在するT細胞の分化選択に関わる多様な機能をもつ成熟した胸腺上皮細胞(iTEC)を、ヒトiPS細胞から試験管内で作製することに成功しました。本分化誘導培養系は、ヒトの胸腺の発生や胸腺発生不全のメカニズムを詳細に解析するための有用なツールになると考えられます。また、iTECとT前駆細胞をオルガノイドとして共培養することで、多様な反応性をもつナイーブT細胞を誘導できる可能性を示しました。今後、胸腺発生不全を伴う重度の免疫不全、加齢に伴う免疫の老化、がんや自己免疫疾患などへの各種治療後のT細胞数減少に対して、T細胞の免疫システムを再構築する全く新しいアプローチの基盤となることが期待されます。
- 論文名
An iPSC-based in vitro model recapitulates human thymic epithelial development and multi-lineage specification - ジャーナル名
Nature Communications - 著者
Yann Pretemer1, Yuxian Gao1,2, Kaho Kanai1,3, Takuya Yamamoto1,4,5, Kohei Kometani1, Manami Ozaki1,3, Karin Nishigishi1,3, Tadashi Ikeda6, Huaigeng Xu1,7, Akitsu Hotta1, Yoko Hamazaki1,2*
*:責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 京都大学大学院 医学研究科 免疫生物学分野
- 京都大学大学院 医学研究科 人間健康科学系専攻
- 京都大学高等研究院ヒト生物学高等研究拠点(WPI-ASHBi)
- 理化学研究所革新知能統合研究センター(AIP)
- 京都大学大学院 医学研究科 心臓血管外科学講座
- カリフォルニア大学サンフランシスコ校
本研究は、下記機関より支援を受けて実施されました。
-
日本学術振興会(JSPS)
- 科研費(JP23KK0136, JP22J13683, JP22KJ1841, JP25K18473, JP20K06469)
- 卓越大学院プログラム「メディカルイノベーション大学院プログラム」
-
日本医療研究開発機構(AMED)
- 再生医療実現拠点ネットワークプログラム
「胸腺機能の再構成による多様な反応性を持つヒトT細胞の再生」- 再生・細胞医療・遺伝子治療実現加速化プログラム
「次世代医療を目指した再生・細胞医療・遺伝子治療研究開発拠点」
「多様な反応性を持つヒトナイーブT細胞を再生する人工胸腺デバイスの開発」 -
科学技術振興機構(JST)
- 次世代研究者挑戦的研究プログラム(JPMJSP2110)
- 武田科学振興財団
- iPS細胞研究基金
注1)ナイーブT細胞
胸腺でつくられたのち、自身が反応する抗原にまだであっておらず体内を循環(パトロール)している状態のT細胞をさす。それぞれの細胞は異なる抗原受容体を発現しているため、ナイーブT細胞がたくさんあることで、私たちは幅広い異物への反応性をもつことができる。特異的な抗原を認識することで活性化・増殖し、他の免疫細胞のはたらきを調節する司令塔としての役割を担うヘルパーT細胞(CD4陽性)や、病原体に感染した細胞やがん細胞などを排除するキラーT細胞(CD8陽性)などエフェクターT細胞に分化する。広い反応性をもつことに加え、増殖能が高く、体内に長期間維持され次の感染に際して強く早い応答を起こす記憶(メモリー)細胞をつくることもできる。
注2)MHC(主要組織適合抗原複合体)
抗原ペプチドをT細胞に提示する分子で、ヒトではHLAとよばれる。クラスIはほぼ全ての有核細胞に発現し、ウイルスなど細胞内のペプチドをCD8+ T細胞に提示する。クラスIIは主に抗原提示細胞に発現し、取り込んだ抗原由来のペプチドをCD4+ T細胞に提示する。胸腺皮質上皮細胞は自己のMHCクラスI/IIを高発現することで、自己MHCを認識できる(自己MHCから抗原提示を受けることができる)T細胞を選びだす。この過程で、クラスIを認識する細胞はCD8陽性に、クラスIIを認識する細胞はCD4陽性T細胞に分化する。
注3)HLA-DR
クラスII MHCに属しCD4陽性のヘルパーT細胞に抗原提示することができる。胸腺上皮細胞にHLA-DRが発現することは、CD4陽性ナイーブT細胞が分化するために必要である。
注4)模倣/擬態(mimetic)胸腺髄質上皮細胞
本来胸腺にない体内のさまざまな組織に発現する遺伝子発現をランダムにオンにするAIREという転写因子の働きに加え、組織に実際に存在する細胞(皮膚や筋肉や腸の細胞など)を模倣した擬態胸腺髄質上皮細胞が、自己寛容の成立にかかわることが最近明らかになってきている。
注5)制御性T細胞
自己応答や過剰な免疫応答を抑制するT細胞。FOXP3の発現により特徴づけられる。























