
研究活動
Research Activities
研究活動
Research Activities
研究成果
Publications
2016年11月22日
iPS細胞疾患モデルを用いて川崎病におけるガンマグロブリン療法不応性のメカニズムの一端を解明
池田和幸研究員(京都大学CiRA増殖分化機構研究部門、京都府立医科大学小児循環器腎臓科・学内講師)、長船健二教授(京都大学CiRA増殖分化機構研究部門)らの研究グループは、iPS細胞技術を用いて乳幼児に発生する頻度が高い原因不明の血管炎症候群である川崎病の病態解明を目指し、標準的な治療法であるガンマグロブリン静脈注射療法(IVIG)への不応性(反応が見られず、効果がないこと)や川崎病の重症度の病態関連候補分子を発見しました。
川崎病におけるIVIG不応の病態解析はこれまでにも報告がありますが、川崎病患者さん由来白血球を用いた解析しか存在せず、患者さん由来血管内皮細胞を用いた解析はありませんでした。本研究では、IVIG不応およびIVIG反応川崎病患者さんから体細胞を採取し、iPS細胞を作製しました。さらに、既報のプロトコールを用いて川崎病患者さん由来iPS細胞を血管内皮細胞へ誘導し、RNA-sequencing解析(注1)を行いました。解析の結果、IVIG不応川崎病患者さん由来iPS細胞から誘導した血管内皮細胞において、CXCL12遺伝子の発現が有意に上昇しており、Gene Set Enrichment Analysis (GSEA)(注2)では、IL-6関連遺伝子群の発現が有意に上昇していました。
本報告は、川崎病患者さん由来iPS細胞を用いた疾患モデル作製研究の初めての報告であり、IVIG不応や川崎病の重症度に密接に関連しているCXCL12を発見し、IL-6関連遺伝子群もこれらの病態に深く関与していることを見出しました。
この研究成果は2016年11月19日に「Circulation Journal」のオンライン版に掲載されました。
川崎病は主に乳幼児に発生する原因不明の急性熱性疾患であり、治療しない場合には約25%の割合で冠動脈病変を合併します。IVIGにより冠動脈病変合併頻度は3~10%へ減少しましたが、15〜20%の割合でIVIGにより解熱しないIVIG不応例が存在し、冠動脈病変を高率に合併します。冠動脈破裂等により死に至る可能性もあり(致死率 0.03%)、IVIG不応のメカニズムの解明は急務の課題です。
川崎病急性期の病態は、免疫系の過剰な活性化を特徴とし、IL-6、TNF-αなどの炎症性サイ
トカインが末梢血中で上昇します。これら炎症性サイトカインを産生する主たる細胞は、単核球が想定されていますが、血管内皮細胞が主にサイトカインを産生している可能性が報告されています。
川崎病の発症には、病原性微生物の関与や、宿主側の要因の関与が推測され数多くの論文が報告されています。IVIGの効果がないと治療前に予測された川崎病患者さんの白血球において、川崎病におけるIVIG不応や冠動脈病変形成に関連のある遺伝子の発現が実際に上昇していたことから、宿主側の要因の関与が示唆されています。そこで、iPS細胞を用いた疾患モデル作製研究を行うことにより、宿主側の要因の観点からも川崎病におけるIVIG不応のメカニズムの解明が可能となり、病態関連分子の探索から新規治療標的分子の同定につながると考えました。
1)川崎病患者さん由来iPS細胞の作製と血管内皮細胞への誘導
解析対象は、IVIG不応川崎病患者さん2例、IVIG反応川崎病患者さん2例としました。患者さんの皮膚線維芽細胞もしくは末梢血T細胞にエピソーマルベクターを用いて初期化6因子を導入しiPS細胞を作製することができました(Figure 1A)。さらに、既報のプロトコール(Taura D et al., Arterioscler Thromb Vasc Biol, 2009)を用いて、川崎病患者さん由来iPS細胞を血管内皮細胞へ誘導しました(Figure 1B, C)。
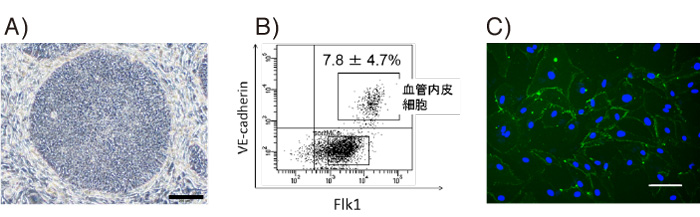
Figure 1 川崎病患者さん由来iPS細胞の樹立と血管内皮細胞への誘導
A) 川崎病患者さん由来iPS細胞のコロニー(固まり)、B) 血管内皮細胞表面マーカーであるFlk-1, VE-cadherinを用いたフローサイトメトリー解析(注3)、C) 血管内皮細胞表面マーカーであるCD31を用いた川崎病患者iPS細胞由来血管内皮細胞の免疫染色。青色:hoechst33342による核染色。緑色:血管内皮細胞、スケールバー, 100μm。
2)主成分分析(Principal component analysis:PCA)(注4)を用いたIVIG不応およびIVIG反応川崎病患者さんiPS細胞由来血管内皮細胞の遺伝子発現プロファイルの比較
IVIG不応川崎病群、IVIG反応川崎病群、健常対照群の各iPS細胞由来血管内皮細胞を用いてRNA-sequencing (RNA-seq) 解析を行ったところ、3群とも独立した遺伝子発現分布を示しました (Figure 2)。
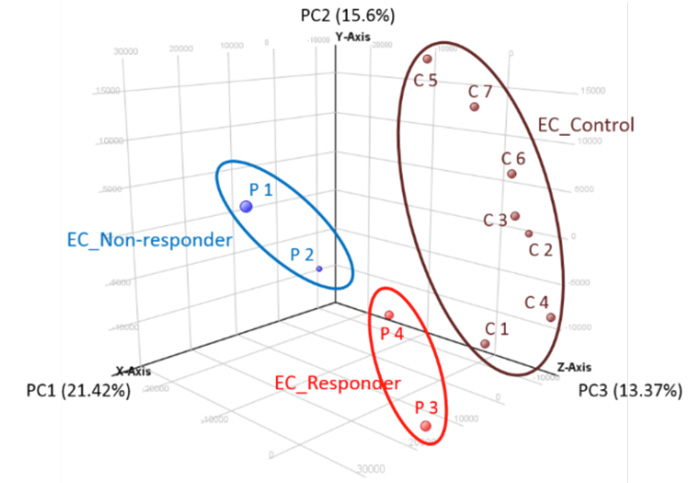
Figure 2 川崎病患者iPS細胞から誘導した血管内皮細胞を用いた主成分分析(PCA)
P1,P2(青色) IVIG不応川崎病群、P3,P4(赤色) IVIG反応川崎病群、C1-C7(茶色) 健常対照群の各iPS細胞由来血管内皮細胞のRNA-seq データを用いて得られたPCAプロット。
3)CXCL12は川崎病IVIG不応に関連した病態関連候補分子である
IVIG不応川崎病群、IVIG反応川崎病群、健常対照群の各iPS細胞由来血管内皮細胞の特徴を解析する目的で、RNA-seq データを用いてgene ontology (GO) 解析(注5)を行いました。IVIG不応川崎病群とIVIG反応川崎病群の比較、およびIVIG不応川崎病群と健常対照群の比較解析において、CXCL12が有意な発現変動遺伝子として抽出されました。
4)IL-6関連遺伝子群はIVIG不応川崎病iPS細胞から誘導した血管内皮細胞において発現が上昇した
IVIG不応川崎病群、IVIG反応川崎病群、健常対照群の各iPS細胞由来血管内皮細胞のRNA-seqデータを用いてGSEAを行ったところ、IVIG不応川崎病群において、IL-6関連遺伝子群の発現が有意に上昇していました。
川崎病患者さん由来iPS細胞を用いた疾患モデル作製研究の報告を初めて行いました。川崎病患者さんiPS細胞由来血管内皮細胞を用いてRNA-seq解析を行うことにより、IVIG不応の病態や川崎病の重症度に密接に関与する病態関連分子であるCXCL12を発見しました。CXCL12は炎症時の血管壁における白血球の遊走に密接にかかわっていることが報告されており、また重症川崎病症例ではより多くの単球、マクロファージ(注6)が血管壁へ浸潤することからも、CXCL12がこれらの病態における鍵となる分子であることが示唆されました。
さらに、血清IL-6値の上昇はIVIG不応川崎病急性期患者さんにおける現象として既に報告されており、患者さんiPS細胞由来血管内皮細胞を用いた本研究での解析結果からも、IL-6のIVIG不応の病態への関与が示唆されました。今回得られた病態関連候補分子について、さらに研究を重ねることにより、新規治療法の開発へと進めていく予定です。
- 論文名
"Transcriptional Analysis of Intravenous Immunoglobulin Resistance in Kawasaki Disease Using an Induced Pluripotent Stem Cell Disease Model" - ジャーナル名
Circulation Journal - 著者
Kazuyuki Ikeda1, 2, Yasutaka Mizoro2, 3, Tomonaga Ameku2, Yui Nomiya2, Shin-Ichi Mae2, Satoshi Matsui2, Yuki Kuchitsu1, Chinatsu Suzuki1, Akiko Hamaoka-Okamoto1, Tomoyo Yahata1, Masakatsu Sone4, Keisuke Okita2, Akira Watanabe2, 3, Kenji Osafune2, Kenji Hamaoka1 - 著者の所属機関
- 京都府立医科大学小児循環器腎臓科
- 京都大学iPS細胞研究所(CiRA)
- 京都大学物質―細胞統合システム拠点
- 京都大学糖尿病・内分泌・栄養内科
本研究は、下記機関より資金的支援を受けて実施されました。
- 国立研究開発法人日本医療研究開発機構(AMED)の再生医療実現拠点ネットワークプログラム「iPS細胞研究中核拠点」
- 独立行政法人日本学術振興会・科学研究費・基盤研究(C)研究代表者:池田和幸「iPS細胞技術を用いたガンマグロブリン不応川崎病に対する新規治療標的分子の同定」
- 武田科学振興財団医学系研究奨励金 研究代表者:池田和幸「iPS細胞技術を用いたガンマグロブリン不応川崎病に対する新規治療標的分子の同定」
- 日本川崎病研究センター研究補助金 研究代表者:池田和幸「iPS細胞技術を用いたガンマグロブリン不応川崎病の病態解明」
- 川崎病治療懇話会研究 研究代表者:池田和幸「iPS細胞技術を用いたガンマグロブリン不応川崎病の病態解明
注1)RNA-sequencing (RNA-seq)
高速シーケンサーを用いてRNA のシーケンシング(配列情報の決定)を行い、細胞内で発現するトランスクリプトーム(細胞内の全転写産物・全RNA)の定量を行う解析。
注2) Gene Set Enrichment Analysis (GSEA)
今回行ったRNA-sequencing解析の結果に最も近いマイクロアレイデータ(あるいはRNA-sequencing解析データ)を過去のデータベースから探し出す解析方法。
注3)フローサイトメトリー解析
流動細胞計測法。レーザー光を用いて光散乱や蛍光測定を行うことにより、水流の中を通過する単一細胞の大きさ、DNA量など、細胞の生物学的特徴を解析することができる。
注4)主成分分析・Principal component analysis(PCA)
多くの変数を持つデータに対して、より少ない変数に縮約することにより、データの特徴をより際立たせる方法。
注5)gene ontology (GO) 解析
全遺伝子のGO term(注7)と発現比較解析の結果から同定された発現変動遺伝子のGO termについて、出現頻度の比較とFisher検定による有意差検定を行う。発現変動遺伝子の特徴的なGO termを推定することができる。
注6)マクロファージ
抗原提示能をもち、生体内の異物を自分の細胞内に取り込み、分解して排泄する細胞。
注7)GO term
遺伝子の生物学的プロセス、細胞の構成要素、分枝機能に着目してつけられる各遺伝子のキーワード。























