
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2017年1月5日
iPS細胞技術によるがん関連遺伝子の働き制御
ポイント
- iPS細胞技術によりがん関連遺伝子の働きを変えることが可能である。
- iPS細胞技術によるがん細胞の運命制御の可能性を提示した。
- がんの発生には遺伝子によらない要因もある。
橋本恭一元大学院生、山田洋介研究員、山田泰広教授(京都大学CiRA未来生命科学開拓部門)らの研究グループは、iPS細胞技術により、がん化に関わる遺伝子であるApc遺伝子の働きを変えうる事、さらには腫瘍細胞の運命を制御しうる事を明らかにしました。
一般的にがんは遺伝子変異が原因と言われていますが、がんのできる臓器によって変異が検出される遺伝子は異なっており、がん遺伝子の働きには、細胞の種類に依存したなんらかの影響があるのではないかと考えられます。しかし、遺伝子変異以外の要因がどの程度がん遺伝子変異の働きに関与しているのか、まだわかっていません。研究グループは大腸がんの原因として知られているApc遺伝子に変異のある大腸がんマウスモデルを用いて大腸の腫瘍細胞をiPS細胞技術注1)により初期化注2)し、初期化腫瘍細胞(RTC)を作製しました。RTCおよび腸管の細胞で、Apc遺伝子の変異によって影響を受ける遺伝子を比較すると、共通する遺伝子はほとんどなく、iPS細胞技術でApc遺伝子変異の作用が変わることがわかりました。変異したApc遺伝子を一時的に正常なApc遺伝子に戻すと、RTCに多能性注3)が与えられ、マウスの体内で様々なタイプの細胞へと分化しました。マウス体内において大腸腫瘍由来の細胞は、腸管細胞に分化すると再び腫瘍を作りましたが、別の種類の細胞では腫瘍にはなりませんでした。これらの結果は、iPS細胞技術によりがん遺伝子の働きを変化させる事が可能であることを示し、腫瘍細胞の運命制御の可能性を示唆しています。
この研究成果は2017年1月2日の週に米国科学アカデミー紀要にオンライン公開されました。
遺伝子変異が原因となって、がんをはじめとして様々な疾患が生じます。しかし、遺伝子変異の影響は必ずしも全身で同じように現れるわけではなく、臓器によって異なっており、遺伝子の働きには、細胞の種類に依存したなんらかの影響があるのではないかと考えられます。しかし、遺伝子変異以外の要因がどの程度遺伝子変異の働きに関与しているのか、特に複数の遺伝子変異が関与するがんでは、まだわかっていません。
iPS細胞を作る技術は細胞が持つ遺伝子の配列情報は変更せずに細胞の運命を変えることができる技術であり、遺伝子変異の働きとそれ以外の要因と関連を研究する上で有用なツールとなります。例えば、腫瘍細胞からiPS細胞を作れば、腫瘍が大きくなる原因となる遺伝子配列異常の情報を持った多能性幹細胞を得ることができ、様々な研究に利用することができます。研究グループは大腸がんの原因として知られているApc遺伝子に変異のある大腸がんマウスモデルを用いて、大腸の腫瘍細胞をiPS細胞技術により初期化し、初期化腫瘍細胞(RTC)を作製し、研究に用いました。
Apc遺伝子が変異した大腸の腫瘍細胞を元にiPS細胞技術により初期化したRTCは、iPS細胞やES細胞に近い遺伝子発現パターンが見られるなど、iPS/ES細胞と同様の性質を示しました。この細胞に正常なApc遺伝子を導入した細胞を用いて、Apc遺伝子変異によって影響をうける遺伝子を調べました。すると影響を受けた遺伝子は、腸管でApc遺伝子変異の影響を受ける遺伝子とほとんど重なっていませんでした(Fig. 1)。
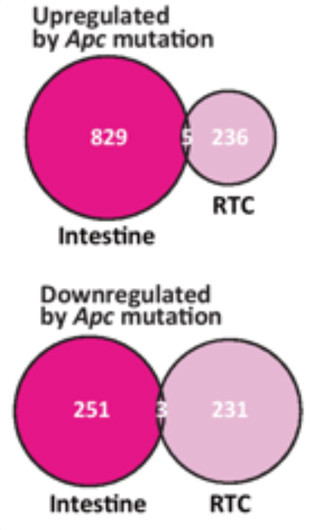
Fig. 1 Apc遺伝子の変異により変化する遺伝子の数
上側:遺伝子発現が増加する遺伝子
下側:遺伝子発現が減少する遺伝子
Intestine:腸管
RTC:初期化腫瘍細胞

Fig. 1 Apc遺伝子の変異により変化する遺伝子の数
上側:遺伝子発現が増加する遺伝子
下側:遺伝子発現が減少する遺伝子
Intestine:腸管
RTC:初期化腫瘍細胞
RTCはiPS/ES細胞に類似した性質を示しましたが、免疫不全マウス注4)に移植をしてもiPS/ES細胞のようにマウスの体内で奇形腫注5)をつくる能力はなく、多能性は失われていました。しかし正常なApc遺伝子を導入したRTCを免疫不全マウスに移植すると、神経細胞や軟骨細胞、上皮細胞などを含む奇形腫を作りました(Fig. 2)。また、正常なApc遺伝子を働かせたRTC由来のキメラマウスをつくると様々な臓器でこの細胞由来の細胞が観察されました。このことから正常なApc遺伝子を働かせるとRTCも多能性を持つことがわかりました。
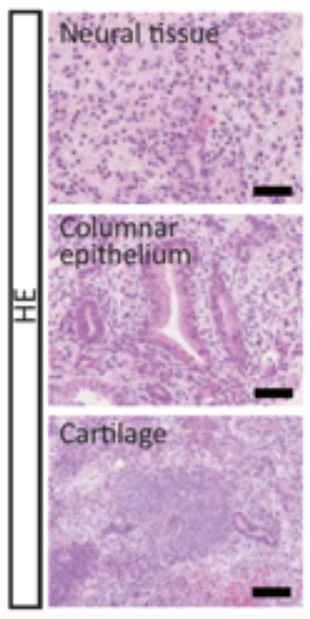
Fig. 2 RTC由来細胞が免疫不全マウス内で形成した奇形腫の様子
Neural tissue:神経組織
Columnar epithelium:上皮組織(円柱上皮)
Cartilage:軟骨組織
スケールバー:50 μm

Fig. 2 RTC由来細胞が免疫不全マウス内で形成した奇形腫の様子
Neural tissue:神経組織
Columnar epithelium:上皮組織(円柱上皮)
Cartilage:軟骨組織
スケールバー:50 μm
2で作成したRTC由来のキメラマウスは、Apc遺伝子が正常に働いており、全身の様々な臓器にRTC由来の細胞を含んでいます。また、RTC由来の細胞には細工を施してあり、ある薬剤が作用するとApc遺伝子が一部欠損して働かなくなります。このキメラマウスに薬剤を投与して、RTC由来の細胞でのみApc遺伝子が働かないようにし、全身の臓器で腫瘍の形成を調べたところ、腸管の細胞に分化したものは再び腫瘍を作りましたが、別の種類の細胞では腫瘍にはなりませんでした(Fig. 3)。
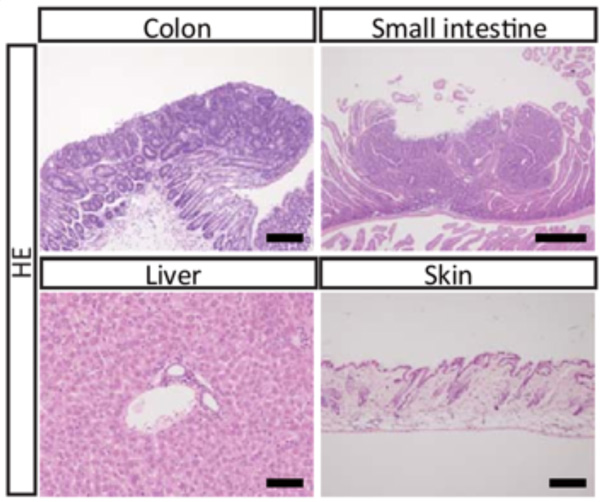
Fig. 3 キメラマウスの各臓器における腫瘍形成の様子
Colon:結腸=大腸の一部 (200 μm)
Small intestine:小腸 (500 μm)
Liver:肝臓 (100 μm)
Skin:皮膚 (200 μm)
(カッコ内はスケールバーの長さ)
本研究により、がん遺伝子の働きは細胞の種類によって異なること、がんの発生には遺伝子によらない要因もある事を示しました。つまり、iPS細胞技術によりがん遺伝子の働きを変化させる事が可能であることを示し、腫瘍細胞の運命制御の可能性を示唆しています。
- 論文名
The cellular context-dependent consequences of Apc mutations on gene regulation and cellular behavior - ジャーナル名
Proceedings of the National Academy of Sciences - 著者
Kyoichi Hashimoto1,2*, Yosuke Yamada1,3*, Katsunori Semi1,4, Masaki Yagi1, Akito Tanaka1, Fumiaki Itakura1, Hitomi Aoki5, Takahiro Kunisada5, Knut Woltjen1,6, Hironori Haga3, Yoshiharu Sakai2, Takuya Yamamoto1,4,7, Yasuhiro Yamada1,4
* 筆頭著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 京都大学大学院医学研究科
- 京都大学医学部附属病院
- 京都大学物質-細胞システム統合拠点(iCeMS)
- 岐阜大学大学院医学系研究科
- 京都大学白眉センター
- 科学技術振興機構 CREST
本研究は、下記機関より資金的支援を受けて実施されました。
- 日本医療研究開発機構 次世代がん医療創生研究事業(P-CREATE)
- 文部科学省 科学技術研究費補助金
- 日本医療研究開発機構 戦略的国際共同研究プログラム(SICORP)
- 武田科学振興財団
- 内藤記念科学振興財団
注1) iPS細胞技術
体細胞からiPS細胞をつくる技術。iPS細胞を作る方法は様々あるが、ここでは山中因子(OCT3/4、SOX2、KLF4およびc-MYC)を遺伝子導入する方法を用いている。一時的に山中因子は細胞内で働くが、細胞が持っていた元々の遺伝子には影響を与えず、最終的に導入した遺伝子は脱落して残らない。
注2) 初期化
分化した体細胞の核がリセットされ受精卵のような発生初期の細胞核の状態に戻すこと。多能性幹細胞(iPS細胞やES細胞など)に近い状態に変化させること。
注3)多能性
様々な体細胞へと分化する能力を持つこと。
注4)免疫不全マウス
免疫機能が低下しているマウス。このような動物は他の個体や異種の細胞を移植しても拒絶反応を起こさずに体内に生着する。
注5)奇形腫(テラトーマ)
ES細胞やiPS細胞を免疫不全マウスの皮下などに注射すると、腫瘍を形成する。この腫瘍は奇形腫と呼ばれ、様々な種類の組織が混在している。奇形腫を観察し、様々な組織に分化していることを確認することは、細胞の分化多能性を調べる一般的な方法の一つである。























