
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2017年10月18日
患者さん由来iPS細胞により乳児型Pompe病の骨格筋病態を再現
ポイント
- 乳児型Pompe病患者さんのiPS細胞から筋肉細胞を作製し、骨格筋における病態の再現に成功した。
- 患者さん由来の筋肉細胞ではライソゾーム注1内にグリコーゲン注2が異常に蓄積しており、酵素補充により改善することを確認した。
- 異常なグリコーゲン蓄積により、細胞内代謝を調節するmTORC1注3の活性化が障害されていることが骨格筋病態の一部と推測された。
吉田健司元大学院生(現京都大学大学院医学研究科発達小児科学助教)、櫻井英俊准教授(京都大学CiRA臨床応用研究部門)らの研究グループは、乳児型Pompe病患者さんから作製したiPS細胞を用いて、この疾患の骨格筋病態を再現することに成功しました。
Pompe病は、ライソゾーム内でグリコーゲンを分解する酵素が生まれつき欠損することで、骨格筋や心臓にグリコーゲンが異常に蓄積する病気です。酵素が完全に欠損する乳児型Pompe病では、無治療で長期に生存することが難しく、酵素を補充することにより生存率は改善しますが、骨格筋症状への効果は限定的です。また、グリコーゲン蓄積が骨格筋症状を引き起こす機序も十分解明されていません。
本研究では、乳児型Pompe病患者さんから作製したiPS細胞を筋肉細胞に分化させました。患者さん由来の筋肉細胞では、この病気の特徴であるライソゾーム内のグリコーゲン蓄積を認め、それらは酵素を補充することで改善することが確認できました。さらに、グリコーゲン蓄積が筋肉細胞に与える影響を解析したところ、ライソゾームが細胞内代謝を調節する際に重要なmTORC1の活性化が障害されていることが観察されました。また、mTORC1に関連した、細胞内エネルギー状態やミトコンドリア機能の悪化も認めました。これらのことからmTORC1活性化障害が乳児型Pompe病の骨格筋病態の一部であることが推測されます。今回の研究は、より良い治療法や新しい治療法の開発に役立つと期待されます。
この研究成果は2017年10月18日午前10時(英国時間:日本時間10月18日午後6時)に英科学誌「Scientific Reports」で公開されました。
Pompe病(糖原病Ⅱ型または酸性マルターゼ欠損症)はライソゾーム酵素である酸性αグルコシダーゼ(GAA)が欠損する遺伝性の病気です。GAAはライソゾーム内のグリコーゲンをグルコースに分解する酵素であり、GAAが欠損すると骨格筋や心臓などの臓器にグリコーゲンが異常に蓄積します。酵素が完全に欠損する乳児型Pompe病では、出生後すぐに全身の筋力低下と心不全を認め、無治療では長期に生存することが難しい重篤な病気です。現在使用可能な唯一の治療である遺伝子組換えヒトGAA(rhGAA)による酵素補充療法は生存率を著明に改善させますが、骨格筋への効果は限定的であり、rhGAAの効果を弱める抗体が出来てしまうことも大きな問題となっています。また、ライソゾーム内にグリコーゲンが蓄積することが、なぜ筋肉の症状を引き起こすのかは十分に解明されていません。
本研究では、乳児型Pompe病患者さんから作製したiPS細胞を用いて、新しい治療法を探すのに適した安定したプラットフォームを作ることと、筋肉の症状を引き起こす病態の解明を目指しました。
1. 患者さんiPS細胞由来の筋肉細胞ではライソゾーム内に異常なグリコーゲン蓄積
まず、3人の乳児型Pompe病患者さんと、3人の健常者の方からiPS細胞を樹立しました。それぞれのiPS細胞に、筋肉細胞への分化を促すMyoD遺伝子を導入しました。薬剤によりMyoDを強制的に発現させることで、10日間という短期間に安定した筋肉細胞を得ることができました。すると、患者さんiPS細胞由来の筋肉細胞では、ライソゾーム内にグリコーゲンが異常に蓄積していました(Fig.1)。一時的にグルコースを含まない培養液で筋肉細胞を培養し、グリコーゲンの分解を促した後に解析することにより、正確にライソゾーム内のグリコーゲンを定量することができました。さらに、培養液にrhGAAを加えて培養することで、異常に蓄積したグリコーゲンがrhGAA濃度依存的に改善することが観察されました。これらの結果から、現在唯一の治療であるrhGAA補充の効果を定量的に評価できるプラットフォームの作製に成功したと考えました。
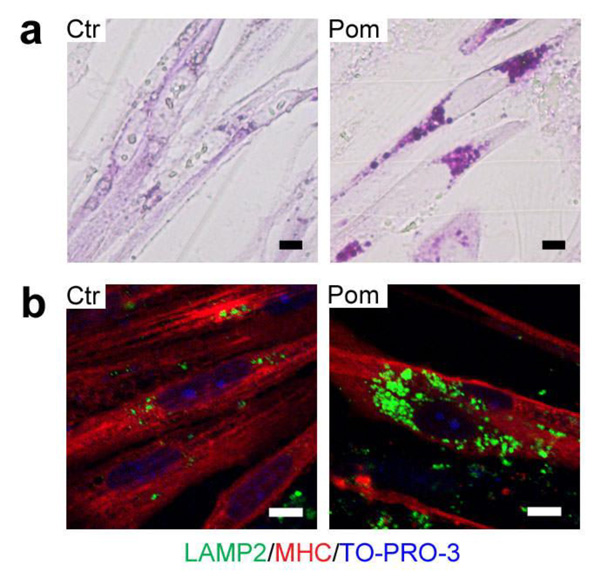
Fig.1 患者さんiPS細胞由来筋細胞のライソゾーム内グリコーゲン異常蓄積
a. グリコーゲンを検出するPAS染色。患者さんiPS細胞由来の筋細胞(Pom)では、健常者の方(Ctr)に比べ、細胞核の周囲に濃染する顆粒を多数認めます。バー:10µm。
b. 免疫染色。患者さんiPS細胞由来の筋細胞(Pom)では、健常者の方(Ctr)に比べ、細胞核の周囲にライソゾームを示す緑色(LAMP2)を多数認めます。バー:10µm。
2. 患者さんiPS細胞由来の筋肉細胞ではmTORC1活性化が低下
最近の研究によりライソゾームはmTORC1を介して様々な細胞内代謝を調節していると考えられています。そこで、iPS細胞由来の筋肉細胞において、mTORC1の主なターゲットであるS6Kや4E-BP1のリン酸化を解析しました。すると、患者さんiPS細胞由来の筋肉細胞ではS6Kや4E-BP1のリン酸化が障害されており、mTORC1の活性化が抑制されていることが分かりました(Fig.2)。さらにmTORC1障害の影響を詳細に調べるため、メタボローム解析などの網羅的な解析を行った結果、細胞内エネルギー状態の悪化やミトコンドリア注4酸化機能障害を示す所見が得られました。Pompe病モデルマウスや遅発型Pompe病患者さんの筋肉で認めるような、オートファジー注5の変化は認めませんでした。これらの結果から、グリコーゲンが蓄積したライソゾームでは、mTORC1を介した細胞内代謝の調節機構が乱れている可能性が示唆されました。
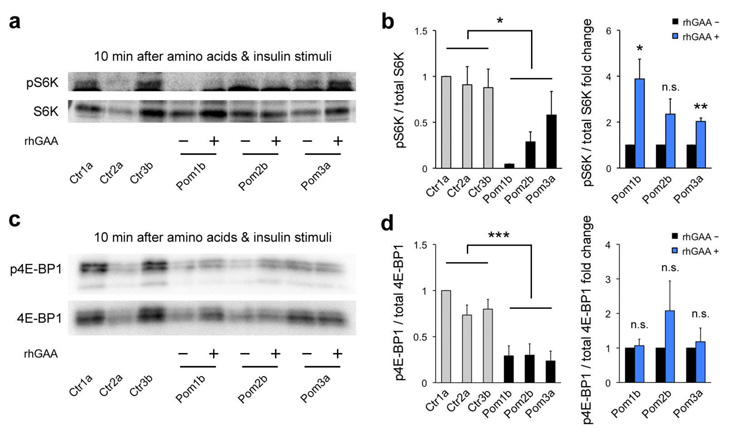
Fig.2 mTORC1のターゲットであるS6Kおよび4E-BP1のリン酸化解析
a. ウエスタンブロットという手法で、リン酸化されたS6K(pS6K)とS6K全体の割合を調べました。
b. a.のバンドの濃さを定量化したところ、患者さんiPS細胞由来の筋肉細胞ではS6Kのリン酸化の割合が低下していました。一部の細胞では酵素補充により改善が観察されました。
c. a.と同様にリン酸化4E-BP1(p4E-BP1)と4E-BP1全体の割合を調べました。
d. 患者さんiPS細胞由来の筋肉細胞では4E-BP1のリン酸化の割合が低下していました。酵素補充での改善ははっきりしませんでした。
乳児型Pompe病患者さん由来のiPS細胞から筋肉細胞を分化誘導して、骨格筋の病態を再現することに成功しました。患者さんiPS細胞由来の筋肉細胞では、ライソゾーム内にグリコーゲンが異常に蓄積し、さらに細胞内代謝調節に重要な役割を持つmTORC1の活性が低下していることが観察されました。これらのことから、乳児型Pompe病の骨格筋病態にmTORC1活性化障害が関与しており、新たな治療のターゲットとなる可能性が示唆されます。今後、本研究がより良い治療法や新しい治療法の開発に役立つことが期待されます。
- 論文名
A Skeletal Muscle Model of Infantile-onset Pompe Disease with Patient-specific iPS Cells - ジャーナル名
Scientific Reports - 著者
Takeshi Yoshida1,2, Tomonari Awaya2,3, Tatsuya Jonouchi1, Ryo Kimura3, Shigemi Kimura4, Takumi Era5, Toshio Heike2 and Hidetoshi Sakurai1*
*責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 京都大学大学院医学研究科 発達小児科学
- 京都大学大学院医学研究科 形態形成機構学
- 熊本市こども発達支援センター
- 熊本大学発生医学研究所 幹細胞部門幹細胞誘導分野
本研究は、下記機関より資金的支援を受けて実施されました。
- AMED 難治性疾患実用化研究事業
- AMED 再生医療実現拠点ネットワークプログラム
「疾患特異的iPS細胞を活用した難病研究」 - AMED 再生医療実現拠点ネットワークプログラム「iPS細胞研究中核拠点」
- JSPS 科研費「若手研究(B)」
注1)ライソゾーム
リソソームやライソソームとも呼ばれる細胞内小器官の一つ。内部に様々な加水分解酵素を含み、細胞内老廃物などを分解します。最近の研究によると、老廃物を分解するだけではなく、細胞内代謝状態を感知し、自ら代謝を調節する機能もあると考えられています。
注2)グリコーゲン
グルコースが多数結合した構造で、グルコースを貯蔵するために肝臓や骨格筋で主に合成されます。
注3)mTORC1
mTORC1(mTOR複合体1)はライソゾームの膜状で活性化され、下流の酵素であるS6K1や4E-BP1をリン酸化することで、ミトコンドリアや蛋白合成といった様々な細胞内代謝を調節していると考えられています。
注4) ミトコンドリア
ミトコンドリアの役目は、内膜で酸素を使って炭水化物と脂肪酸を分解して、細胞が使用するエネルギーをつくりだすことです。ミトコンドリア酸化機能障害とはこのエネルギー代謝がうまく機能していないことを意味します。
注5) オートファジー
細胞自身が、細胞内のタンパク質を分解するしくみのひとつで、自食ともいわれています。























