
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2020年2月14日
糖尿病病態はヒトiPS細胞由来膵内分泌前駆細胞の移植後のインスリン分泌能力を高める
ポイント
- マウスにおいて、糖尿病病態注1はヒトiPS細胞から作製した膵内分泌前駆細胞注2の移植後のインスリン注3分泌能力を高めることを明らかにした。
- その機序として、ホストの血中インスリン濃度の低下と、移植片中のインスリン産生細胞数の増加が関与することを示した。
- 本知見は、ヒト多能性幹細胞由来膵細胞を用いた糖尿病の移植治療において、移植後の糖尿病病態の最適なコントロール方法の選択に役立つと期待される。
糖尿病の根治的な治療法として、ES細胞やiPS細胞などのヒト多能性幹細胞から作製した膵細胞の移植が期待されています。生体内に移植される膵細胞は複雑なホスト環境注4に暴露されるため、それが移植成績に影響を与える可能性も考えられますが、不明な点が多くあります。
持田泰佑 主任研究員(武田薬品工業株式会社T-CiRAディスカバリー、T-CiRA注5)および豊田太郎 講師(CiRA増殖分化機構研究部門、T-CiRA)らの研究グループは、免疫不全マウスへの移植実験によって、糖尿病病態がヒトiPS細胞由来の膵内分泌前駆細胞の移植後のインスリン分泌能力を高めることを見出しました。また、その機序として、ホストの血中インスリン濃度の低下が、移植片に含まれるインスリン産生細胞数を増加させることを示しました。これらの知見は、ヒトiPS細胞由来膵細胞を用いた移植治療において、移植後の糖尿病病態の最適なコントロール方法の選択に役立つと期待されます。
この研究成果は、2020年1月31日(米国時間)に米国科学誌「Diabetes」にオンライン公開されました。
膵島の移植は糖尿病に対する根治療法の一つですが、移植用膵島の不足が問題となっています。そのため、ヒト多能性幹細胞(ES細胞およびiPS細胞)から作製する膵細胞を代わりに利用することが期待されています。培養皿上で膵島様細胞を作製する研究は近年大きな進捗があるものの、生体内に存在するような完全に成熟した膵島を作製することは難しく、移植後に生体内の環境を利用しながら望ましい分化・成熟させることが重要です。しかしながら、生体内に移植される膵細胞が暴露される環境は複雑であり、それが移植成績に与える影響については不明な点が多くあります。
そこで本研究グループは、ヒトiPS細胞由来膵細胞の臨床応用に向けて、膵内分泌細胞の分化過程の初期段階である膵内分泌前駆細胞(Pancreatic endocrine progenitor, EP細胞)をヒトiPS細胞から作製し、ホストの糖尿病病態がEP細胞の移植後の機能や成熟度に与える影響について検討しました。
1) 糖尿病病態のホスト環境下では移植早期において移植片のインスリン分泌能力が高まる
ストレプトゾトシン投与によって糖尿病を誘発した免疫不全マウスの腎被膜下に、ヒトiPS細胞から作製したEP細胞を移植し(糖尿病+EP)、移植片由来のインスリン分泌の指標である血中ヒトC-ペプチド注6量(図1A)および血糖値(図1B)を測定しました。比較対照として、無処置の非糖尿病マウスへも移植しました(非糖尿病+EP)。その結果、糖尿病病態では非糖尿病よりも移植後早期から血中ヒトC-ペプチド量が増加することが示されました。また、その血中ヒトC-ペプチド量の増加は、移植後長期において血糖値が正常域にまで低下してからは落ち着きました。これらの結果から、糖尿病病態のホスト環境下では移植早期において、EP細胞由来の移植片のインスリン分泌能力が高まることが分かりました。
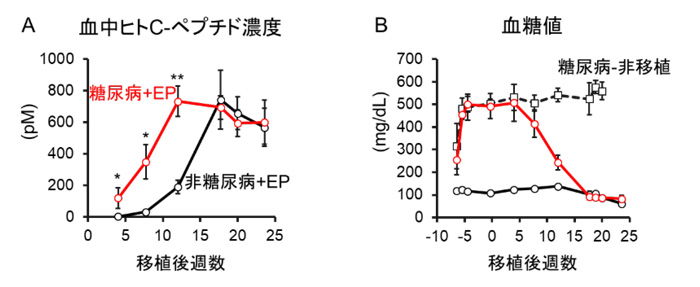
図1 EP細胞移植後の飽食時血中ヒトC-ペプチド濃度(A)と血糖値(B)の推移
* p < 0.05, ** p < 0.01 対 非糖尿病+EP群
2) 移植片のインスリン分泌能力はホストの血中インスリン濃度と逆相関する
次に、糖尿病マウスで血中インスリンの分泌能力が高まる原因として、ホストのインスリン不足が関与しているか検討しました。まず、インスリンを持続投与して血糖値をコントロールした糖尿病マウスにEP細胞を移植したところ(図2A)、非インスリン処置群に比べて血中ヒトC-ペプチド量の増加が鈍化し、それは非糖尿病マウスに移植した場合と同等でした(図2B)。続いて、血糖値の関与を検討するために、インスリン非依存的経口血糖降下薬であるSGLT2阻害薬ダパグリフロジン(Dapa)を反復投与して高血糖を部分的に改善した糖尿病マウスにEP細胞を移植しました(図2C)。Dapa投与による血糖値の部分的な改善では、血中ヒトC-ペプチド量の増加が鈍化しませんでした(図2D)。これらの結果から、ホストの血中インスリン濃度の低下が、EP細胞の移植後のインスリン分泌能力を高めていると考えられました。
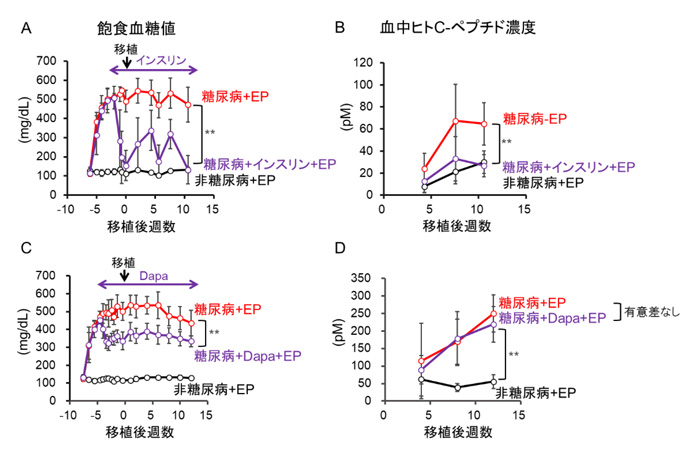
図2 EP細胞移植後の飽食時血糖値(A, C)と血中ヒトC-ペプチド濃度(B, D)の推移
A, B:インスリン処置の影響を検討
C, D:SGLT2阻害薬ダパグリフロジン(Dapa)処置の影響を検討
** p < 0.01
3) 糖尿病病態は移植片に含まれるインスリン産生細胞数を増加させる
糖尿病病態で移植片中からのインスリン分泌能力が高まる機序を明らかにするために、EP細胞の移植6週後に移植片を摘出し、組織学的解析をしました。糖尿病マウス由来の移植片は、非糖尿病マウス由来の移植片に比べて、総重量に差がないにも関わらず(図3A)、膵内分泌ホルモンであるインスリンおよびグルカゴン注7を多く含んでいました(図3B)。また、各々の移植片から切片を作製して蛍光免疫染色による定量解析をした結果、糖尿病マウス由来の移植片ではインスリンに陽性を示す面積の割合が高いことが分かりました(図3C)。さらに、培養皿上でEP細胞をインスリン細胞に分化誘導する過程において、インスリンシグナルの阻害は、インスリン産生細胞への分化効率を高めました。これらの結果から、糖尿病病態ではEP細胞のインスリン産生細胞への分化促進やインスリン産生細胞の増殖亢進によって移植片に含まれるインスリン産生細胞数が増加していると考えられました。
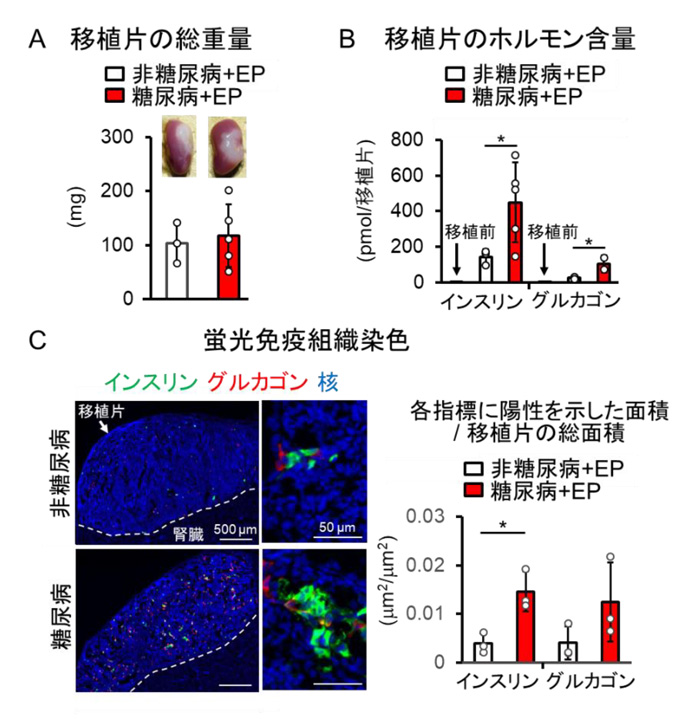
図3 EP細胞移植片の総重量(A)、膵内分泌ホルモンの含量(B)および蛍光免疫組織染色(C)
C:各移植片から切片を作製し、インスリン(緑)およびグルカゴン(赤)について
蛍光免疫組織染し、定量した。左は代表的な染色像。
* p < 0.05
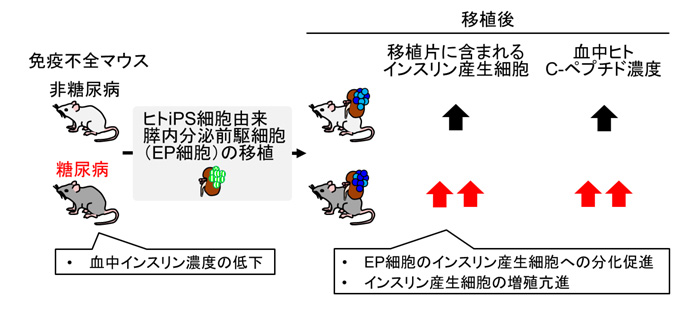
本研究では、免疫不全マウスを用いて糖尿病病態が、ヒトiPS細胞由来EP細胞の移植後のインスリン分泌能力を高めることを見出しました。さらに、その機序として、ホストの血中インスリン濃度の低下が関与していること、また、EP細胞のインスリン産生細胞への分化促進やインスリン産生細胞の増殖亢進によって移植片に含まれるインスリン産生細胞数が増加することが関与していることを示しました。これらの知見は、将来のヒトiPS細胞由来膵細胞を用いた移植治療において、移植後の糖尿病病態の最適なコントロール方法の選択に役立つと期待されます。
-
論文名
"Insulin-deficient diabetic condition upregulates the insulin-secreting capacity of human induced pluripotent stem cell-derived pancreatic endocrine progenitor cells after implantation in mice" - ジャーナル名
Diabetes - 著者
Taisuke Mochida1,3, Hikaru Ueno1,3, Noriko Tsubooka-Yamazoe1,3, Hideyuki Hiyoshi1,3, Ryo Ito1,3, Hirokazu Matsumoto1,3, Taro Toyoda2,3 - 著者の所属機関
- 武田薬品工業株式会社 T-CiRAディスカバリー
- 京都大学 iPS細胞研究所(CiRA)増殖分化機構研究部門
- T-CiRAプログラム
本研究成果は、CiRAと武田薬品工業株式会社との共同研究プログラムT-CiRAによるものです。
注1) 糖尿病病態
インスリンが十分に働かないために血糖値が高くなった病態。全身の臓器に影響が現れ、合併症につながる危険がある。
注2) 膵内分泌前駆細胞
膵島に存在する各種内分泌細胞のもととなる細胞。
注3) インスリン
血液中の糖を取り込ませるように細胞に働きかけ、血糖値を下げる効果があるホルモン。膵臓の中でも膵島と呼ばれる部分にある内分泌細胞であるβ細胞で作られ、放出される。
注4) ホスト環境
ここでは、細胞移植を受けるホスト(宿主)の生体内環境
注5)T-CiRA(Takeda-CiRA Joint Program for iPS Cell Applications)
CiRAと武田薬品工業株式会社との共同研究プログラム。T-CiRA豊田プロジェクトでは、糖尿病に対するiPS細胞由来膵島細胞を用いた医療開発のために研究を実施している。
注6) C-ペプチド
インスリンが合成される際には、前駆体(プロインスリン)が切断され、インスリンとC-ペプチドが1:1の割合で作られる。さらにインスリンとC-ペプチドは同程度の割合で分泌されるため、インスリンの合成量や分泌量の指標として使われる。
注7) グルカゴン
肝臓などエネルギーを蓄えている細胞に働きかけ、血液中に糖を放出するように働きかけ、血糖値を上げる効果があるホルモンの一種。膵臓中の膵島にある内分泌細胞であるα細胞で作られて放出される。























