
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2021年8月24日
6型コラーゲンを補う細胞移植がウルリッヒ型先天性筋ジストロフィーモデルマウスの病態を改善する
ポイント
- 6型コラーゲン遺伝子の変異はウルリッヒ型先天性筋ジストロフィー注1)の原因となる
- 細胞移植により6型コラーゲンタンパク質を補うとモデルマウス内で筋肉の再生や成熟が見られた
- 全身で同様の筋肉の再生や機能改善が起こすことができれば治療法につながると期待できる
竹中菜々研究員(CiRA臨床応用研究部門)、櫻井英俊准教授(CiRA同部門)らの研究グループは、ウルリッヒ型先天性筋ジストロフィー(UCMD)のモデルマウスに、細胞移植により6型コラーゲンタンパク質を補うことで、筋肉をより太く成熟させることに成功しました。
間葉系間質細胞(MSC: Mesenchymal stromal cells)注2)は6型コラーゲンタンパク質をはじめ、各種因子を分泌することで、骨格筋を維持する機能をもっています。6型コラーゲン遺伝子に変異が生じると、UCMDの原因となります。これまで、UCMDの患者さんから採取した細胞やモデルマウスから、骨格筋の再生不全が報告されていました。しかし、6型コラーゲンタンパク質の有無がどのように症状に影響をあたえているのか、ほとんど知られていませんでした。
研究グループは、免疫不全UCMDモデルマウス(Col6a1KO)の筋肉内にMSCを移植したところ、少なくとも12週間生着することができました。さらに6型コラーゲンを産生するMSCを移植すると、細胞が生着し、6型コラーゲンが補充された部位でのみ筋再生や成熟が進みました。UCMDモデルマウスから分離した骨格筋サテライト細胞注3)は、6型コラーゲンを産生するMSCと共培養することで、増殖能力と、骨格筋への分化・成熟能力が改善しました。
これらの結果から、6型コラーゲンを補うことが、筋肉再生や成熟を向上させたことを示しています。
この研究成果は2021年8月9日に「Stem Cell Research & Therapy」で公開されました。
UCMDは生まれたときから筋力が低下し、徐々に筋萎縮が進行していく疾患で、現在のところ効果的な治療法は見つかっていません。また、UCMDの患者さんでは、筋線維を組織と結合するために重要な働きをする6型コラーゲンタンパク質が、全身の骨格筋を含む様々な組織で作られないことがわかっています。
これまでに、MSCから分泌される6型コラーゲンタンパク質や他の細胞外マトリックス注4)などの因子が、骨格筋の分化や再生・維持に重要な働きをしていることがわかっていました。しかし、MSCの移植による効果なのか、6型コラーゲンタンパク質の補充による効果なのか、わかっていませんでした。
1. 移植した細胞で6型コラーゲンタンパク質を発現していた
6型コラーゲン遺伝子を持たないUCMDのモデルマウス(Col6a1KO)の後肢の筋肉に、健康な人の骨格筋組織から分離したMSC(pMSC)、健康な人のiPS細胞から作製したMSC(iMSC)、6型コラーゲン遺伝子をノックアウトしたiMSC(KO-iMSC)を、それぞれ移植しました。
細胞移植2週間後および12週間後に、移植した部分を蛍光染色し顕微鏡で観察したところ、6型コラーゲン遺伝子をもつpMSCおよびiMSCの移植2週間後(tx2w)で6型コラーゲンタンパク質(緑色)が検出されました(Fig. 1)。また、12週間後(tx12w)でも6型コラーゲンタンパク質は維持されていました。
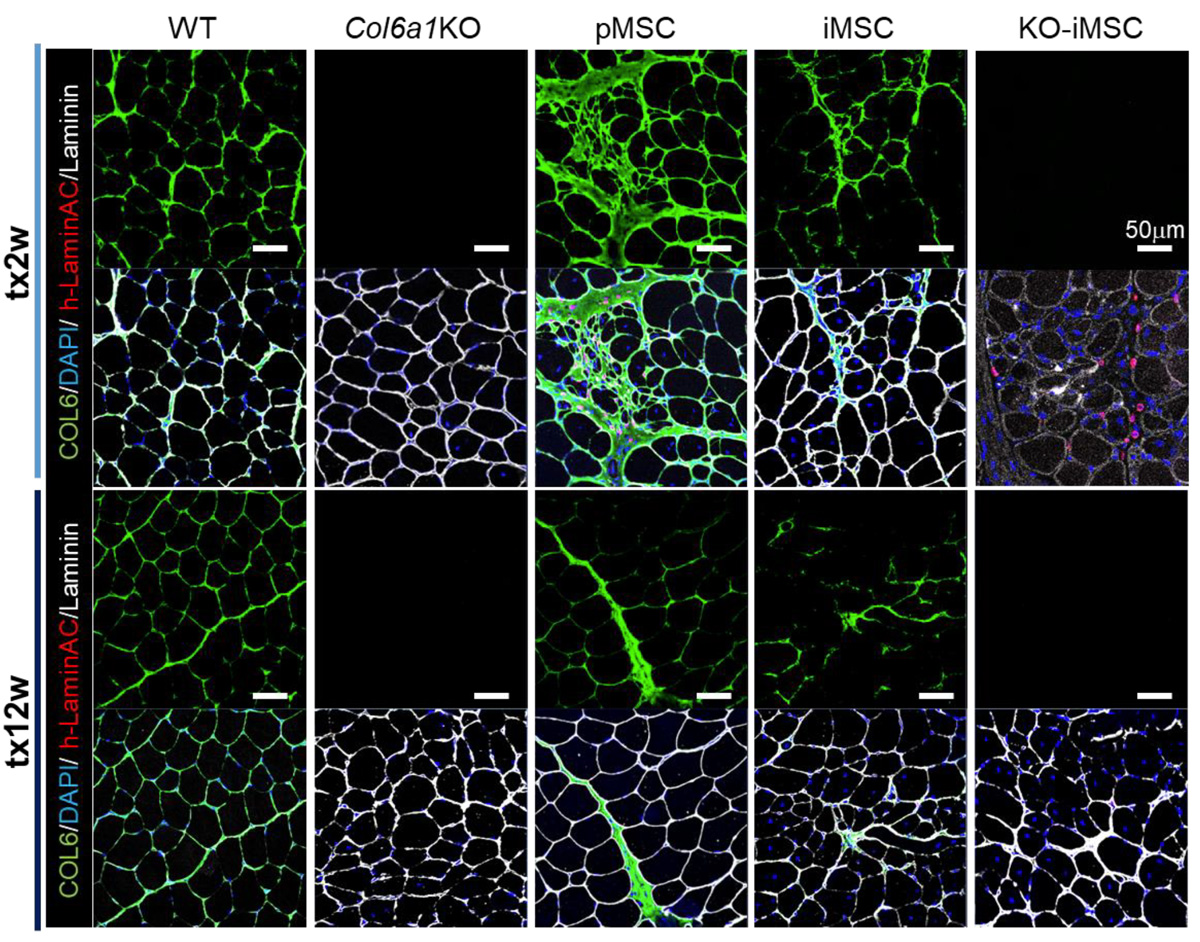
Fig. 1 細胞移植後のマウス筋肉内での6型コラーゲンタンパク質
緑色:COL6 6型コラーゲンタンパク質
青色:DAPI 細胞核の場所を示すマーカー
赤色:h-LaminAC ヒトの細胞核の場所を示すマーカー(移植した細胞の場所を示す)
白色:Laminin 骨格筋細胞の基底膜
WTは野生型マウス
2. 細胞移植により筋線維が太く成熟した
1.と同様にCol6a1KOの後肢の筋肉に、pMSC、iMSC、KO-iMSCを移植し、1週間後に移植した部位を染色し顕微鏡で観察しました。
もとのモデルマウス(Col6a1KO)ではeMHC陽性(赤色)の再生筋線維は極小径の細いものに限られており、筋線維の成熟が不十分な状態でとどまっていますが、6型コラーゲンをもつpMSCやiMSCを移植すると、eMHC陽性(赤色)の細胞数が増えており、かつ、それらがより太く成熟している様子が見られました(Fig. 2)。また、pMSCやiMSCでは一つの筋線維の中に核が複数みられるものも多数あり(黄色矢印)、このことからも、筋線維の成熟が促進されていることがわかりました。
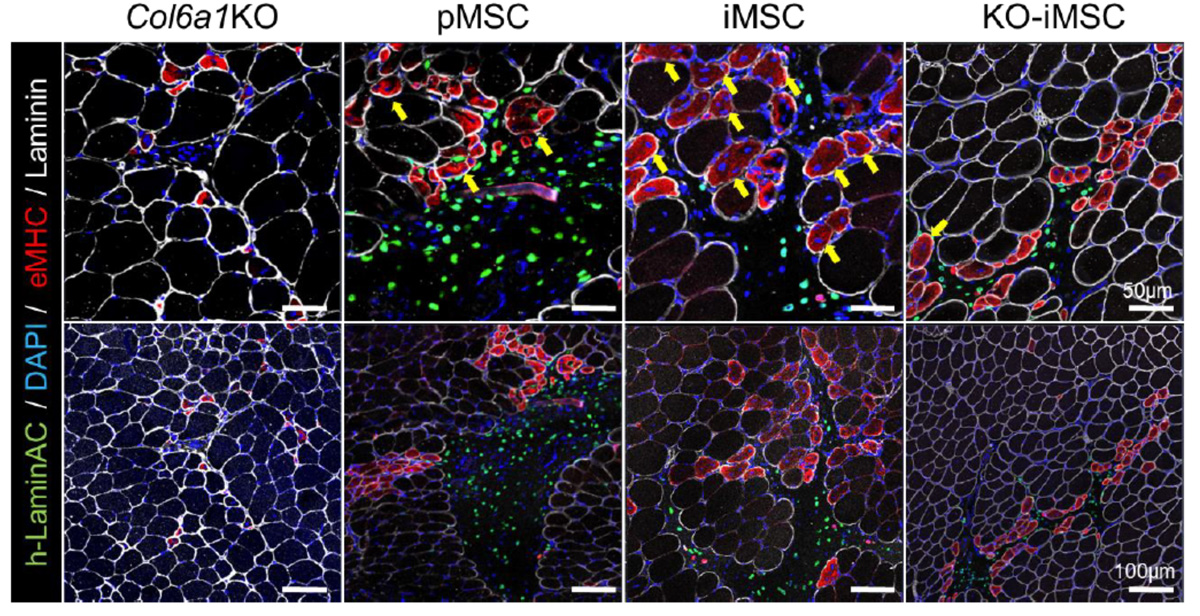
Fig.2 6型コラーゲンの補充により筋線維が再生され成熟化する
緑色:h-LaminAC ヒトの細胞核の指標(移植した細胞の場所を示す)
青色:DAPI 細胞核を示す
赤色:eMHC 再生した筋線維の指標
白色:Laminin 骨格筋細胞の基底膜
上段は下段の一部を拡大したもの。
また、再生した筋線維1本あたりの横断面積を計算したところ、pMSCやiMSCを移植したマウスでは移植しなかった場合と比べて3倍程度太くなりました(Fig. 3)。
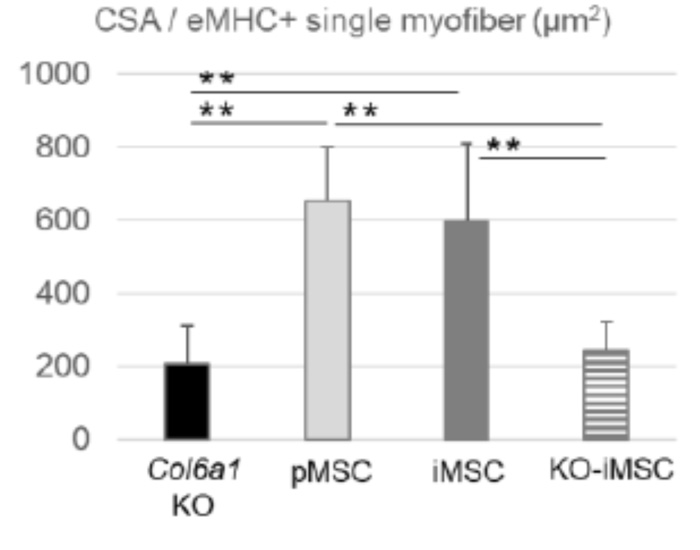
Fig.3 筋線維あたりの断面積
UCMDのモデルマウスにpMSC やiMSCを移植することで、6型コラーゲンタンパク質が補われ、筋肉の再生や成熟を起こすことができました。UCMDの治療戦略の一つとして、6型コラーゲンタンパク質を補う細胞移植療法の可能性を高めました。
また、iPS細胞由来のiMSCにより、6型コラーゲンを補う事ができることを示しました。現在、公益財団法人京都大学iPS細胞研究財団にて準備が進められているゲノム編集をしたiPS細胞ストックからiMSCを作ることで、多くの患者さんに利用可能な細胞移植療法につながると期待できます。
再生した筋肉がどの程度機能するのかはさらなる検証を行う必要があります。今回の成果では細胞移植部位でのみ筋肉の再生がみられており、実際の治療法とするためには広範囲の筋肉で同様の筋再生を促す方法の開発が求められます。
- 論文名
Collagen-VI supplementation by cell transplantation improves muscle regeneration in Ullrich congenital muscular dystrophy model mice - ジャーナル名
Stem Cell Research & Therapy - 著者
Nana Takenaka-Ninagawa1*, Jinsol Kim1, Mingming Zhao1, Masae Sato1, Tatsuya Jonouchi1,
Megumi Goto1, Clémence Kiho Bourgeois Yoshioka1, Rukia Ikeda1, Aya Harada1, Takahiko Sato2, Makoto Ikeya1, Akiyoshi Uezumi3, Masashi Nakatani4, Satoru Noguchi5, Hidetoshi Sakurai1*
*責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 藤田医科大学 解剖学I
- 東京都健康長寿医療センター研究所
- 藤田医科大学 総合医科学研究所
- 国立精神・神経医療研究センター 疾病研究第一部/トランスレーショナル・メディカルセンター
- 京都大学iPS細胞研究所(CiRA)
本研究は、下記機関より資金的支援を受けて実施されました。
- 日本学術振興会 科研費 若手研究
- AMED再生医療実現拠点ネットワークプログラム 「技術開発個別課題」「iPS細胞研究中核拠点」
注1) ウルリッヒ型先天性筋ジストロフィー(UCMD: Ullrich congenital muscular dystrophy)
6型コラーゲンの遺伝子の変異が原因。生まれた直後から筋力が低く、筋萎縮の状態になる。肘・肩・膝などの関節が正常な範囲で動かなくなったり、手足の関節が過剰に伸びた状態になる。
注2) 間葉系間質細胞(MSC: Mesenchymal stromal cells)
骨・脂肪・軟骨などへと分化する能力をもつ幹細胞の一種。体内にもともと存在している。
注3) サテライト細胞
骨格筋系幹細胞のうち、生体内で筋線維の外側に張り付いている成人型の細胞。この細胞が分裂して筋肉の修復や増強を行っている。
注4) 細胞外マトリックス
細胞間の隙間を埋める生体高分子(コラーゲンやプロテオグリカンなど)の集合体。骨・軟骨、歯、皮膚などに多く含まれ、組織を支えてメカニカル(クッション・伸び縮みなど)な機能を果たしている。























