
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年2月13日
ヒトiPS細胞で肺線維症の「修復不全」を再現
―病態をリセットする新たな治療標的候補を特定―
ポイント
- ヒトiPS細胞を使って肺線維症で肺胞上皮細胞が正常に分化しない状態(ATCS)を再現した。
- このモデルを用いた検証により、ATCSをリセットし、肺の線維化を抑制する薬剤の候補としてp300/CBP阻害剤を見つけた。
筒井優介研究員、後藤慎平教授(CiRA臨床応用研究部門)らの研究グループは、ヒトiPS細胞技術とマルチオミクス解析注1)を駆使し、致死的な疾患である特発性肺線維症(IPF)注2)の新たな治療標的を明らかにしました。
IPFは肺組織が進行性に線維化し、呼吸不全を招く難病です。近年の研究から、患者の肺では肺胞上皮細胞注3)が正常に分化できず、「肺胞移行細胞状態注4)(本研究ではAlveolar Transitional Cell State: ATCSと呼称)」という異常な状態で停滞することが知られていますが、これが線維化の悪化に寄与するかどうかは不明なままでした。
研究グループは、肺線維症の新たな治療ターゲットの同定のためにヒトiPS細胞から作製した肺胞オルガノイド注5)と線維芽細胞注6)を共培養した病態モデルを構築しました。このモデルを用いて264種類の化合物スクリーニングを実施し、肺胞の収縮(線維化の指標)を抑制する薬剤を探索しました。スクリーニングの結果、p300/CBP阻害剤が極めて高い線維化抑制効果を示すことが判明しました。
さらに研究グループは、iPS細胞からATCS様細胞(iATCs)を高効率に誘導・単離する新たな技術を確立しました。iATCsを用いた詳細な解析により、ATCSが直接線維化の進行に関与すること、並びにp300/CBP阻害剤がこのプロセスを直接的に抑制し、それによって周囲の線維芽細胞の活性化を抑えていることが明らかになりました。さらに、単一細胞レベルの解析(scRNA-seq等)を通じて、p300が転写因子注7)AP-1やHNF1Bと協力してATCSの遺伝子プログラムを制御しているという分子メカニズムも突き止めました。
本研究は、ヒトiPS細胞モデルが難病の創薬スクリーニングに極めて有効であることを実証しました。特定されたp300/CBP阻害剤は、従来の治療薬とは異なり「細胞の分化異常」を標的とする新しい治療戦略となることが期待されます。今後はこの知見を基に、より効果的で安全なIPF治療薬の開発が進むことが望まれます。
この研究成果は2026年2月12日に「Nature Communications」で公開されました。
特発性肺線維症(IPF)は、肺胞の壁が厚く硬くなり、酸素の取り込みが困難になる進行性の難病です。現在、線維化を遅らせる治療薬は存在しますが、病気の進行を完全に止めたり、失われた機能を回復させたりすることは難しく、より根本的な治療法の開発が強く望まれています。
肺の正常な機能を保つためには、ガス交換を担う「I型肺胞上皮細胞(AT1)」と、その補充や保護を担う「Ⅱ型肺胞上皮細胞(AT2)」のバランスが重要です。通常、肺が損傷を受けると、Ⅱ型肺胞上皮細胞がI型肺胞上皮細胞へと分化することで組織を修復します。
しかし、IPF患者の肺では、このⅡ型肺胞上皮細胞からI型肺胞上皮細胞への再生プロセスが破綻し、「肺胞移行細胞状態(ATCS)」という異常に分化した細胞へと姿を変えて停滞し、最終的に「修復不全」に陥っていることが近年の研究で判明しました。
これまで、このATCSが線維化の「真の原因」なのか、あるいは線維化が起きた後の単なる「結果」なのかについては議論が分かれていました。また、これまでの実験モデルでは、この停滞したATCSが異常な因子を放出し、周囲の線維芽細胞を過剰に刺激し続けることで、さらなる線維化を招くという悪循環が示唆されていましたが、ヒト特有の複雑なⅡ型肺胞上皮細胞の分化プロセスやATCSの挙動を十分に再現できないことが、創薬研究の大きな壁となっていました。
本研究グループは、ヒトiPS細胞から作製した肺胞組織(オルガノイド)を用い、Ⅱ型肺胞上皮細胞がATCSを経て線維化を誘導するプロセスを試験管内で精密に再現することに成功しました。このヒト特有の再生不全モデルを確立したことで、従来の「対症療法」ではなく、細胞の分化を正常化させて「病態を根本からリセットする」という全く新しい視点での創薬研究が可能となりました。
1)ヒトiPS細胞由来 肺線維症モデルによる病態再現
研究グループが過去に独自開発した「線維芽細胞依存性肺胞オルガノイド(FD-AOs)」を用いました。これはヒトiPS細胞から作ったⅡ型肺胞上皮細胞と線維芽細胞を共培養する肺モデルです。ここに薬剤(ブレオマイシン:BLM注8))で損傷を与えることで、ヒトの肺内部で起こる「Ⅱ型肺胞上皮細胞がATCSへと変化し、周囲の組織が硬く収縮する」という病態を培養皿上で再現することに成功しました。
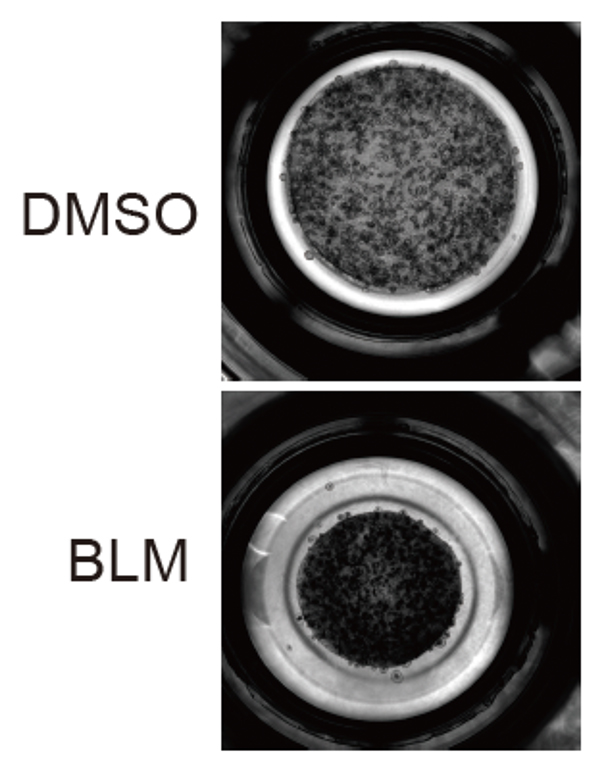
Fig.1 BLM処理により肺胞オルガノイドが収縮し、肺線維症の病態を再現している。
2)264種類の薬剤候補から「p300/CBP阻害剤」の同定
構築したモデルを用いて、既存の化合物ライブラリーから線維化を抑える薬剤を探すスクリーニングを実施しました。その結果、タンパク質の働きを調節するエピジェネティック制御因子注9)である「p300/CBP」の働きを阻害する薬剤(CBP30、GNE781)が、肺胞オルガノイドの収縮を有意に抑制することを発見しました。
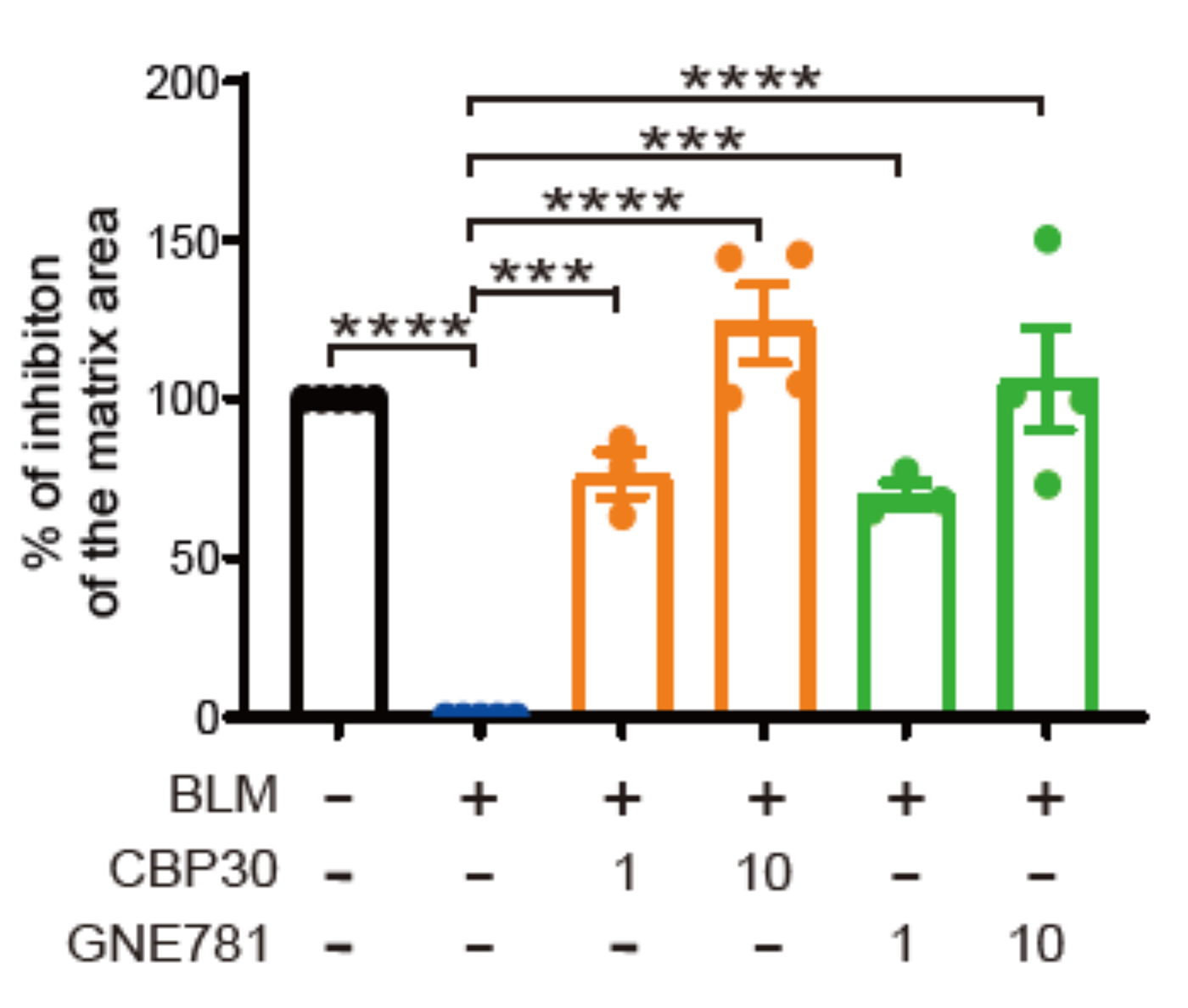
Fig.2 BLM添加による肺胞オルガノイドの収縮をCBP30およびGNE781が抑制する。
3)ATCSへの移行を制御する遺伝子ネットワークの解明
次世代シーケンシング技術(CUT&Tag法)を用い、p300がゲノム上のどこで働いているかを網羅的に解析しました。その結果、p300がATCSを引き起こす重要な遺伝子群の「スイッチ(エンハンサー)」に直接結合し、「オン(H3K27ac)」にしていることを発見しました。さらに、AP-1やHNF1Bといった転写因子と「協力」して、Ⅱ型肺胞上皮細胞からATCSへの異常な変化を指揮する司令塔として機能していることを解明しました。
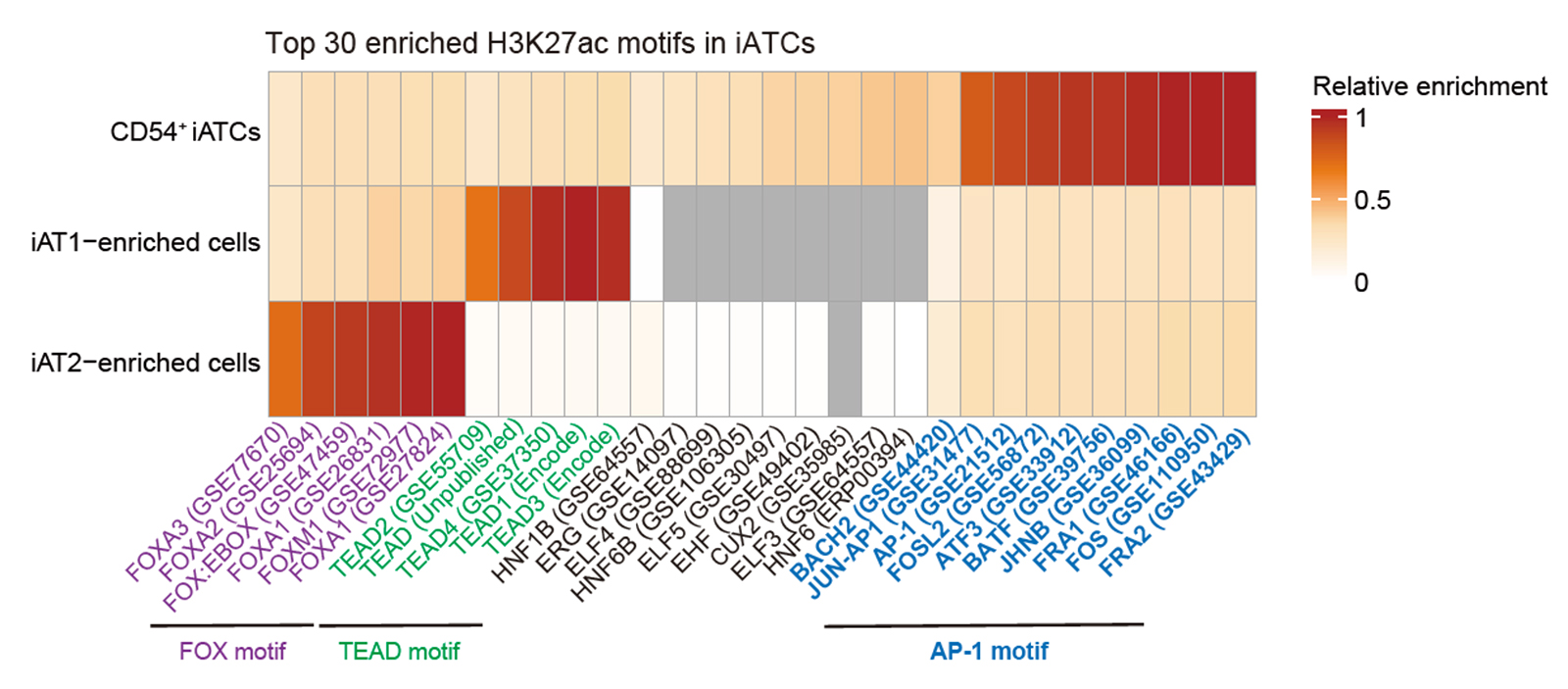
Fig. 3 ATCS状態の細胞に見られる上位の転写因子
本研究は、ヒトiPS細胞から作製した高精度な病態モデルを用いることで、これまで解析が困難だった特発性肺線維症(IPF)の根本的な発症メカニズムの一端を解明しました。最大の手がかりは、肺胞の再生が途中で止まってしまった「修復不全状態(ATCS)」の細胞が、周囲の組織の線維化について直接の引き金になっていることを突き止めた点にあります。
さらに、この異常な細胞状態への移行を支配する「司令塔」としてタンパク質「p300/CBP」を特定し、その阻害剤が病態をリセットし、強力に線維化を抑制することをヒトの細胞レベルで証明しました。これは、従来の「炎症を抑える」あるいは「進行を遅らせる」といった対症療法的なアプローチとは異なり、「細胞の分化状態を正常化させる」という全く新しい治療コンセプトを提示するものです。
今回の成果は、iPS細胞技術が実際の創薬スクリーニングにおいて極めて有効であることを示す重要な実例でもあります。今後は、本研究で見出されたp300/CBP阻害剤の有効性と安全性をさらに詳しく検証するとともに、より最適な投与方法や、他の薬剤との併用療法の検討が進むことが期待されます。
肺線維症は依然として予後不良な難病ですが、今回の知見を基盤として、失われた肺の再生を促すような革新的な治療法の開発を加速させ、患者さんのQOL(生活の質)向上と根治の実現を目指します。
- 論文名
Human iPSC-based modeling of pulmonary fibrosis reveals p300/CBP inhibition suppresses alveolar transitional cell state - ジャーナル名
Nature Communications - 著者
Yusuke Tsutsui1, Atsushi Masui1, Satoshi Konishi1, Taro Tsujimura2, Mio Iwasaki1, Takuya Yamamoto1,2,3, Shimpei Gotoh1*
*責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 京都大学高等研究院 ヒト生物学高等研究拠点(WPI-ASHBi)
- 理化学研究所 革新知能統合研究センター (AIP) iPS細胞連携医学的リスク回避チーム
本研究は、下記機関より支援を受けて実施されました。
- 杏林製薬株式会社
- iPS細胞研究基金
-
日本医療研究開発機構(AMED)
- 再生・細胞医療・遺伝子治療実現加速化プログラム
- 次世代医療を目指した再生・細胞医療・遺伝子治療研究開発拠点(JP23bm1323001)
- 疾患特異的iPS細胞を用いた病態機序解析による特発性間質性肺炎の層別化と創薬システムの開発(JP23bm1423004)
- 再生医療等実用化研究事業
- レポーターiPS細胞を用いた難治性呼吸器疾患に対する革新的創薬(JP25bk0104190)
- 革新的先端研究開発支援事業
- 肺胞幹細胞ストレスに起因する特発性肺線維症の早期分子経路の解明と治療薬の創製(JP24gm1910009)
注1)マルチオミクス解析
遺伝子(ゲノム)やタンパク質(プロテオーム)、代謝物(メタボローム)など、生体内の多種多様な網羅的情報を組み合わせて統合的に解析する手法。
注2)特発性肺線維症(IPF)
原因不明で肺の壁が徐々に厚く硬くなり(線維化)、酸素の取り込みが困難になる進行性の難病。
注3)肺胞上皮細胞(I型・Ⅱ型)
肺でガス交換を担う「I型」と、肺の修復や保護、I型への補充を担う「Ⅱ型」の2種類がある。
注4)肺胞移行細胞状態(ATCS)
肺が損傷した際、Ⅱ型肺胞上皮細胞がI型へ変化(分化)しようとして途中で停滞した、異常な修復不全状態のこと。
注5)オルガノイド
iPS細胞などから試験管内で作られた、生体の臓器に似た構造や機能を持つ立体的なミニ組織のことです。
注6)線維芽細胞
コラーゲンなどを作り出し、組織の構造を支える細胞です。肺線維症ではこれが過剰に活性化し、肺を硬くする。
注7)転写因子
特定の遺伝子に結合して、その働きをコントロールする役割を持つタンパク質の総称。
注8)ブレオマイシン(BLM)
肺に損傷を与えて線維化を引き起こす性質があり、実験的に肺線維症の病態を再現するために使われる薬剤。
注9)エピジェネティック制御遺伝子
DNAの配列そのものは変えずに、後天的に遺伝子の働きの強弱を調節する物質のこと。























