
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年3月23日
多線毛細胞への分化の鍵「デューテロソーマル細胞」をヒトiPS細胞から分化誘導
―特異的表面マーカーにより、気道防御の司令塔細胞の解析が可能に―
ポイント
- ヒトiPS細胞由来気道上皮細胞から、多線毛細胞の前駆細胞であるデューテロソーマル細胞に特異的な表面マーカーCD36(目印となるタンパク質)を同定しました。
- 線毛機能不全症候群(PCD)の患者さん由来iPS細胞から誘導した気道上皮細胞の解析により、Cyclin O (CCNO) 遺伝子がデューテロソーマル細胞において中心小体を大量につくるプロセスを制御し、正常な線毛形成に必須の役割を持つことを明らかにしました。
- PCD患者さん由来iPS細胞から誘導した気道上皮細胞の単一細胞トランスクリプトーム解析により、CCNOの機能低下がデューテロソーマル細胞から多線毛細胞への正常な分化を阻害し、異常な多線毛細胞を招く病態を解明しました。
山城春華 大学院生(京都大学CiRA臨床応用研究部門/同大学院医学研究科)、小西聡史 特定拠点助教、および後藤慎平 教授(京都大学CiRA臨床応用研究部門)らは、ヒトiPS細胞から、気道上皮の多線毛細胞注1)へと分化する際に見られる前駆細胞「デューテロソーマル細胞注2)」の特異的な表面マーカーを同定するとともに、線毛形成のメカニズムと難病「線毛機能不全症候群(PCD)注3)」の一部の病型の発症機構を解明しました。
気道上皮に存在する多線毛細胞は、無数の線毛を動かすことで吸い込んだ異物や病原体を排出する、生体防御に不可欠な細胞です。多線毛が形成される過程では、非膜性細胞小器官である「デューテロソーム」を介して中心小体注4)が大量に増幅されますが、この過程で現れる「デューテロソーマル細胞」は数が少なく一過性であるため、ヒトにおける詳細な解析は困難でした。研究グループは、ヒトiPS細胞から気道上皮細胞を誘導する系を用い、単一細胞トランスクリプトーム解析注5)を行うことで、デューテロソーマル細胞に特異的に発現する表面マーカーとしてCD36注6)を同定しました。これにより、生きた状態のデューテロソーマル細胞を単離して詳細に解析することが可能になりました。なお、CD36は生体内の気道組織では顕著な発現が見られないものの、iPS細胞からの気道上皮細胞への分化過程においてデューテロソーマル細胞を同定・回収するための有用なツールとなることが示されました。
さらに、線毛の形成や運動に異常が生じる遺伝性疾患であるPCDの病態解明のため、CCNO 遺伝子に病的な変化(病的バリアント)を持つPCD患者さん由来のiPS細胞と、ゲノム編集技術で病的バリアントを修復したiPS細胞から気道上皮細胞を誘導して比較しました。解析の結果、CCNOの機能が低下した状態では、正常なデューテロソーマル細胞を介した多線毛細胞への分化経路が阻害され、細胞がデューテロソ―マル細胞の状態をバイパスするような異常な分化経路を辿ることが明らかになりました。この過程で、NEK2、ANLN、CDC20 といった遺伝子群がCCNOの下流でデューテロソーマル細胞の成熟を制御していることも明らかになりました。本研究は、ヒトの気道線毛形成メカニズムの理解を深め、PCDの病態を細胞の分化異常という新たな切り口で解明しただけでなく、PCDの新たな治療法開発や薬物スクリーニングのための強力なプラットフォームを提供したといえます。
この研究成果は2026年3月20日に「Stem Cell Reports」で公開されました。
気道上皮に存在する多線毛細胞は、細胞表面に生えた200本程度の線毛をリズミカルにそろって動かすことで、吸い込んだ病原体や異物を粘液とともに体外へ排出する「粘膜線毛クリアランス」を担っています。この機能は生体防御において極めて重要であり、その異常は慢性的な呼吸器感染症を引き起こします。
多線毛が形成される過程では、線毛が伸びるための土台となる構造(基底小体)の前駆体である「中心小体」を大量に作り出す必要があります。この中心小体増幅の足場として「デューテロソーム」と呼ばれる特殊な構造体が現れます。このデューテロソームを持つ多線毛細胞の前駆細胞(デューテロソーマル細胞)は、多線毛形成の鍵を握る存在ですが、生体内では数が極めて少なく、出現時期も限定的であるため、ヒトにおけるデューテロソーマル細胞の詳細な分子メカニズムの解析は困難とされてきました。
また、遺伝性疾患である「線毛機能不全症候群(PCD)」の中には、CCNO 遺伝子の変化が原因で多線毛細胞に形成される運動性線毛の数が著しく減少する病型があることが知られています。CCNOが中心小体増幅に関与していることは示唆されていましたが、ヒトの気道上皮細胞の分化過程において具体的にどの段階で、どのような分子群と協調して機能しているのかという詳細な仕組みは不明なままでした。
本研究は、ヒトiPS細胞から気道上皮を誘導する技術と単一細胞トランスクリプトーム解析を駆使することで、捉えにくいデューテロソーマル細胞の特性を定義し、CCNOによる多線毛形成の制御機構とPCDの病態をヒトの細胞レベルで解明することを目指して行われました。
1)ヒトiPS細胞由来のデューテロソーマル細胞の同定と特異的表面マーカーの発見
研究グループは、ヒトiPS細胞から気道上皮細胞を誘導し、単一細胞トランスクリプトーム解析(scRNA-seq)を行いました(Fig. 1)。この解析に基づき、多線毛細胞へと分化する途中に現れる一過性の前駆細胞「デューテロソーマル細胞」を特定し、DEUP1 やCCNO といったデューテロソーム関連遺伝子マーカーを発現するデューテロソーマル細胞群が、分化の初期(気液界面培養4日目付近)にピークを迎え、その後成熟した多線毛細胞へと変化していく過程を確認しました。そして、デューテロソーマル細胞の細胞表面に特異的に発現するタンパク質を探索した結果、CD36をそのマーカーとして同定しました。CD36を用いた細胞ソーティング(FACS)により生きたデューテロソーマル細胞を単離することに成功し、単離した細胞が高い多線毛形成能を持つことを実証しました。
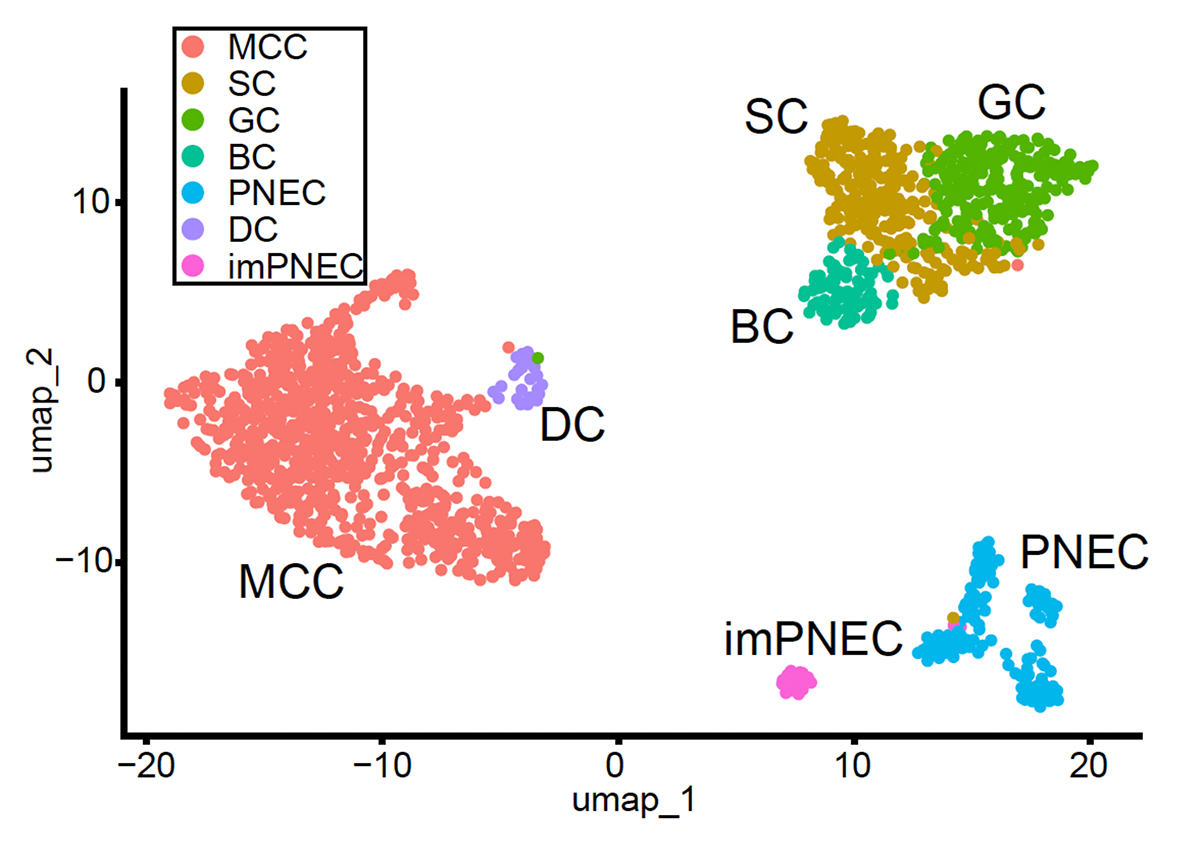
Fig. 1 ヒトiPS細胞由来気道上皮細胞のscRNA-seqに基づくUMAP解析
一つ一つの点が細胞1個を表しており、近くに表示された細胞ほど似た性質を持っている。デューテロソーマル細胞(DC)の集団が存在することが確認された。
2)CCNO 遺伝子に病的バリアントを持つ線毛機能不全症候群の患者さん由来iPS細胞を用いた病態の再現
CCNO 遺伝子に病的バリアントを持つ線毛機能不全症候群(PCD)の患者さんからiPS細胞を樹立しました。さらに、ゲノム編集技術を用いて病的バリアントを健常者と同じ遺伝子配列に修復したコントロールiPS細胞を作製し、両者を気道上皮細胞(iAEC)へ分化させて比較解析を行いました。
電子顕微鏡観察の結果、コントロールiPS細胞由来の気道上皮細胞(CCE1-iAEC)では正常な線毛と基底小体が形成されましたが、PCD患者さん由来iPS細胞から分化させた気道上皮細胞(PCD-iAEC)では線毛がほとんど存在せず、基底小体の形成も著しく阻害されていました(Fig. 2)。PCD-iAECでは、デューテロソーマル細胞の指標となるCD36陽性細胞がほとんど検出されませんでした。また、CCNO 遺伝子に病的バリアントがあると、NEK2 やANLN、CDC20 といったデューテロソーム関連遺伝子の発現が低下することが判明しました。
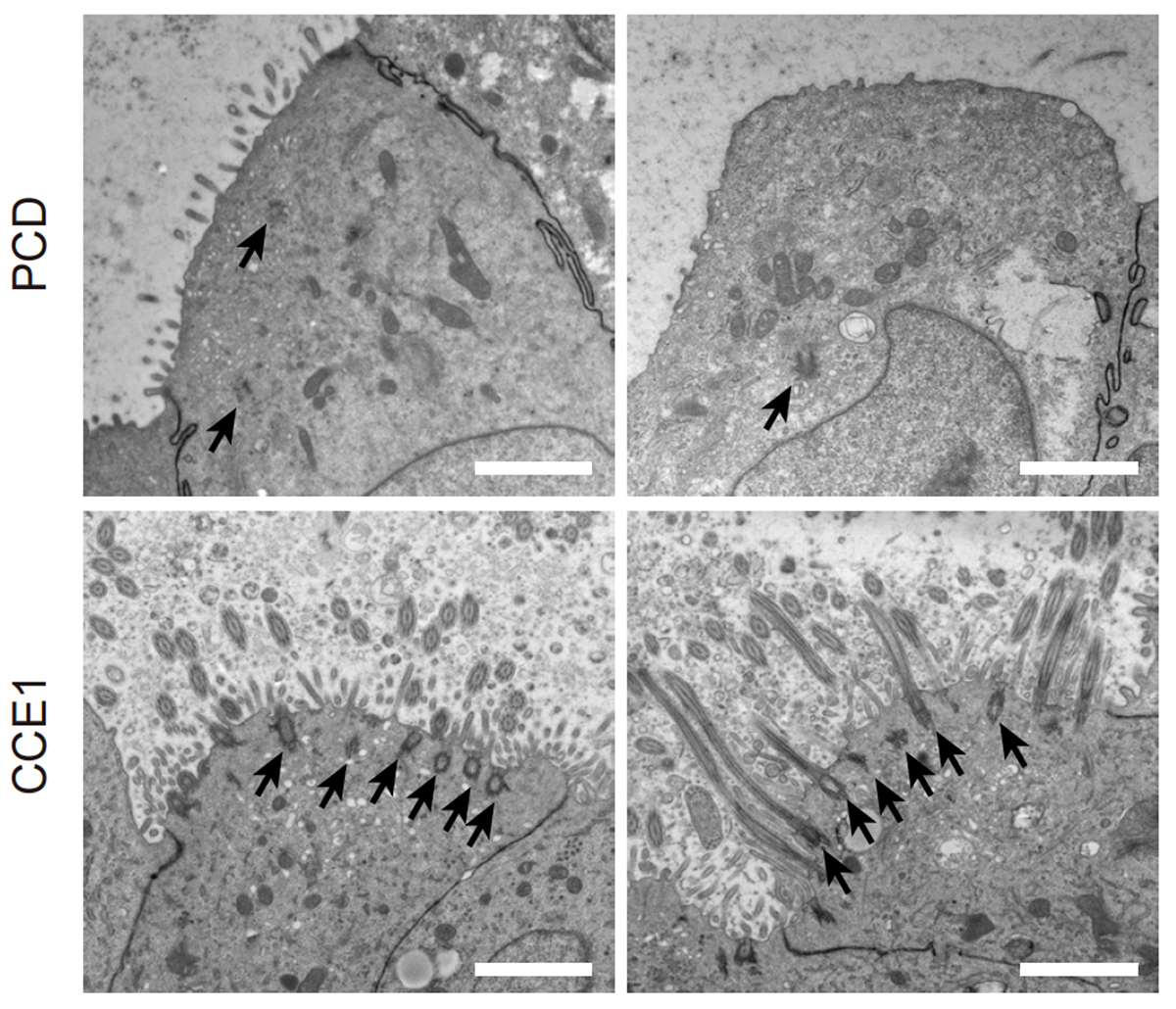
Fig. 2 iPS細胞から作製した気道上皮細胞の電子顕微鏡画像(矢印:基底小体)
CCNOはヒトの多線毛形成において、デューテロソームを介した中心小体増幅に必須の役割を担っており、その機能不全がPCDにおける重篤な多線毛形成減少を引き起こす一因であることが確認されました。
3)単一細胞トランスクリプトーム解析による異常な多線毛細胞分化経路の解明
デューテロソーマル細胞が豊富に存在するタイミングで、線毛機能不全症候群(PCD)患者さん由来iPS細胞から分化させた気道上皮細胞(PCD-iAEC)とコントロールiPS細胞由来気道上皮細胞(CCE1-iAEC)に対して単一細胞トランスクリプトーム解析(scRNA-seq)による比較解析を行い、多線毛細胞への分化の軌跡や細胞状態の変化を詳しく調査しました。
コントロール群(CCE1-iAEC)では、気道上皮前駆細胞からデューテロソーマル細胞状態を経て多線毛細胞へと分化する「正規のルート」が主流でした。一方でCCNO 遺伝子に病的バリアントを持つ群(PCD-iAEC)では、デューテロソーマル細胞を正常に通過できず、デューテロソーム関連遺伝子群を発現せずに多線毛細胞(MCC)へなろうとする「デューテロソーマル細胞バイパス経路」が出現していることが明らかになりました(Fig. 3)。この異常な経路を通った細胞(異常多線毛細胞:abMCC)は、線毛の構造遺伝子の発現が極めて低く、成熟した線毛を多数持つ多線毛細胞にはなり得ないことが示されました。
CCNOの機能低下は単に分化を止めるだけでなく、細胞に異常な分化経路を辿らせることで、非機能的な異常細胞を生成させてしまうことがわかりました。これは、CCNO 遺伝子の病的バリアントによる線毛機能不全症候群の病態が単なる多線毛細胞の欠乏ではなく、分化プロセスのエラーによって生じることを示唆しています。
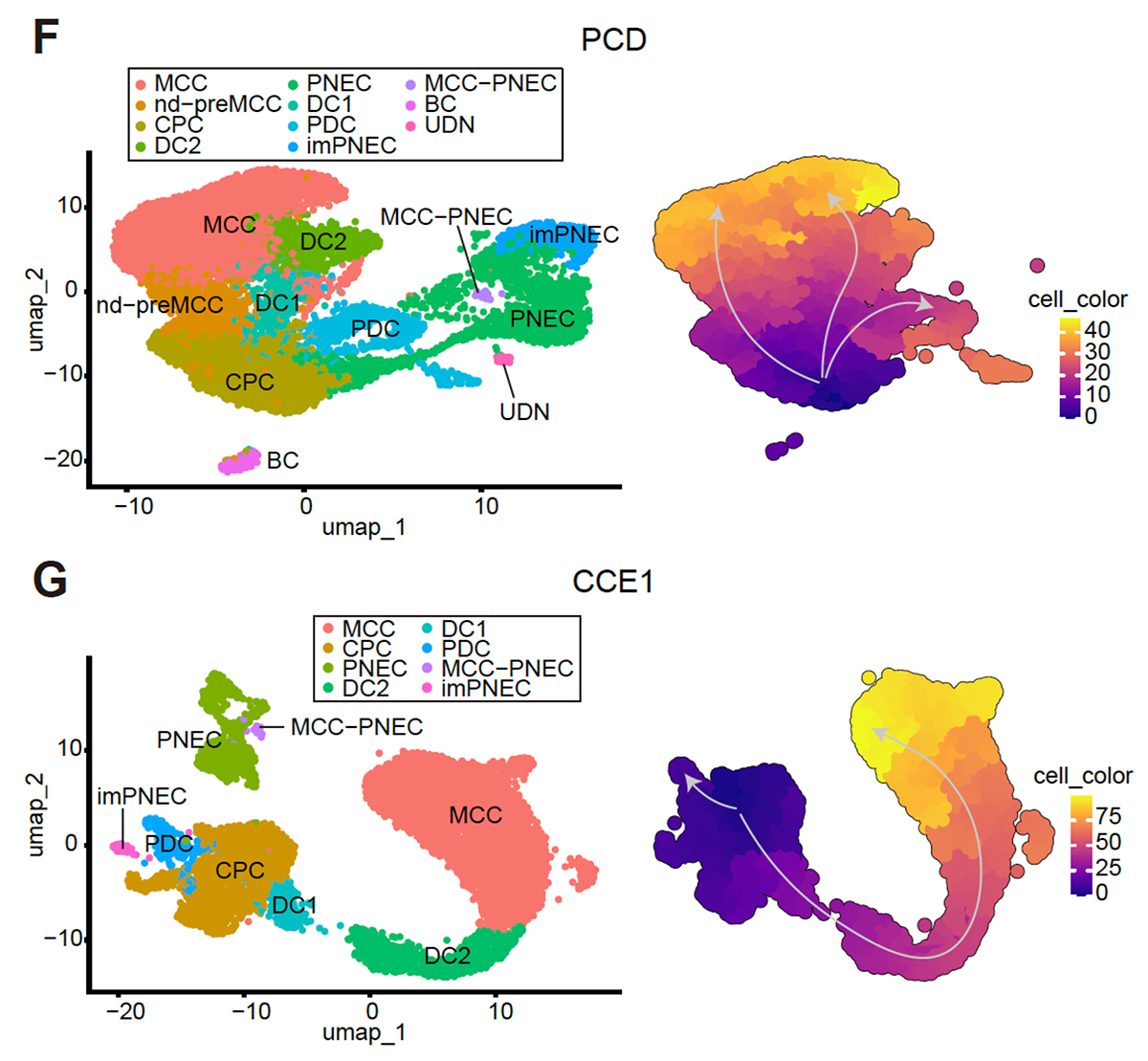
Fig. 3 PCD患者さん由来iPS細胞から分化させた気道上皮細胞(PCD-iAEC)とコントロールiPS細胞由来気道上皮細胞(CCE1-iAEC)のscRNA-seqに基づくUMAP解析・疑似時間解析の比較
PCD-iAECでは、CCE1-iAECでみられない「気道上皮前駆細胞(CPC)→デューテロソーム非依存性多線毛細胞前駆体(nd-preMCC)→多線毛細胞(MCC)」という異常な分化経路がみられた。
本研究では、ヒトiPS細胞を用い、多線毛細胞の前駆細胞であるデューテロソーマル細胞の表面マーカーCD36を同定しました。さらに、CCNOがデューテロソーマル細胞における中心小体増幅に必須であることや、その機能低下が異常な多線毛細胞の分化経路を誘発し、線毛機能不全症候群(PCD)を引き起こす病態を、ヒト細胞レベルで解明しました。
今後、このデューテロソーマル細胞解析プラットフォームを活用したPCDの治療薬スクリーニングや、他の線毛関連疾患の病態解明が期待されます。また、本知見は将来的な遺伝子治療や再生医療の実現に向けた重要な基盤となり、呼吸器難病の克服に向けた研究を前進させると期待できます。
- 論文名
Deuterosomal cells are the responsible lineage for multiciliogenesis in human airway differentiation - ジャーナル名
Stem Cell Reports - 著者
Haruka Yamaki1,2, Satoshi Konishi1*, Koji Tamai1, Naoyuki Sone1, Senye Takahashi1, Yifei Xu1,3,
Takahiro Tsuji2, Hiroaki Ozasa2, Takuya Yamamoto1,4,5, Toyohiro Hirai2, Kazuhiko Takeuchi3,6,
Shimpei Gotoh1*
*:責任著者 - 著者の所属機関
- 京都大学 iPS細胞研究所(CiRA)
- 京都大学大学院医学研究科 呼吸器内科学
- 三重大学大学院医学系研究科 耳鼻咽喉・頭頸部外科学
- 京都大学 高等研究院 ヒト生物学高等研究拠点(WPI-ASHBi)
- 理化学研究所 革新知能統合研究センター(AIP)iPS細胞連携医学的リスク回避チーム
- 松阪中央総合病院 耳鼻咽喉科
本研究は、下記機関より支援を受けて実施されました。
-
日本学術振興会 (JSPS) 科学研究費助成事業
(JP22H03077, JP23K24338, JP25K12809, JP25K02660) -
日本医療研究開発機構(AMED)
- 難治性疾患実用化研究事業
ヒトiPS細胞を用いた線毛機能不全症候群の新規診断法の開発と精密医療への応用- 再生・細胞医療・遺伝子治療実現加速化プログラム
次世代医療を目指した再生・細胞医療・遺伝子治療研究開発拠点- 再生医療等実用化研究事業
レポーターiPS細胞を用いた難治性呼吸器疾患に対する革新的創薬 - 公益財団法人 藤原記念財団
- 公益財団法人 内藤記念科学振興財団
- iPS細胞研究基金
注1)多線毛細胞
気道の上皮に存在し、細胞表面に「線毛」と呼ばれる数百本の細い毛を持つ細胞。この線毛がリズムよくそろって動くことで、気管支や肺に入ってきた病原体やゴミを粘液とともに体外へ運び出す役割を担う。
注2)デューテロソーマル細胞
多線毛細胞へと分化する途中で一時的に現れる、希少な前駆細胞。細胞内で「デューテロソーム」という非膜性の小器官を形成し、線毛の土台となる構造(基底小体)の前駆体である「中心小体」を大量に増やすための工場のような役割を果たす。
注3)線毛機能不全症候群(PCD)
遺伝子の病的な変化により、気道の線毛が正しく作られなかったり動かなかったりする遺伝性の病気。これにより、気管支炎、肺炎などの呼吸器感染症を幼少期から繰り返すようになり、長引く咳や痰の症状がみられる。
注4)中心小体
細胞内に存在する構造体の一つで、線毛が伸びる際の土台となる「基底小体」に変化する。通常の細胞には2個程度しかないが、多線毛細胞になるためには、これを短時間で200~300個程度にまで効率よく増やす必要がある。
注5)単一細胞トランスクリプトーム解析(scRNA-seq)
組織に含まれる膨大な数の細胞を一つひとつバラバラにし、それぞれの細胞内でどの遺伝子がどれくらい働いているかを網羅的に調べる手法。細胞ごとの個性を精密に捉えることができるため、病気の原因となる異常な細胞の特定などに威力を発揮する。
注6)CD36
細胞の表面に存在するタンパク質で、特定の種類の細胞を見分けるための「目印」になる。本研究では、このCD36がデューテロソーマル細胞に特異的に現れることを突き止め、生きた細胞を分離するための目印として活用した。























