
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年3月24日
受精卵の遺伝子改変を狙い通りに近づける新手法 ―AI予測で結果のばらつきを低減―
研究のポイント
- 遺伝子改変後に起こりやすい変化について、AI(機械学習)モデルによる予測とES細胞での事前検証を組み合わせ、
受精卵でのゲノム編集の結果を事前に見通す手順を確立 - マウス受精卵で狙った遺伝子を働かなくし、初代の個体で目的の表現型を効率的に確認できることを実証
- ゲノム編集動物の作製期間の短縮と結果の確実性の向上だけでなく、動物の使用数の抑制も期待
滋賀医科大学動物生命科学研究センターのKhanui Lkhagvadorj大学院生、岡村永一助教(研究当時)、依馬正次教授、筑波大学生命科学動物資源センターの水野聖哉教授、京都大学iPS細胞研究所のKnut Woltjen准教授らの研究グループは、受精卵の遺伝子改変で起こりやすい結果のばらつきを減らし、狙い通りの変化をより確実に導入する新しい方法を開発しました。
従来のゲノム編集の手法(CRISPR/Cas9※1等)では、DNAを切断した後の修復結果をコントロールすることが難しく、狙い通りの個体を得るために多くの時間と多数の動物を必要としていました。
本研究では、AIモデル「inDeiphi※2」を用いて、ゲノム編集を施した受精卵に「どのような変化が起こりやすいか」を事前に予測し、さらに、その予測結果を、培養細胞(ES細胞※3)を使って、事前に検証する手順を確立しました。これにより、受精卵で起こる変化を前もって見通すことが可能になり、初代の個体※4で目的の表現型の変化を効率的に確認できることを示しました。
この方法は、遺伝子改変動物の作製を迅速化し、結果の正確性を高めることが期待されます。また、狙い通りにならない個体を減らすことで、動物の使用数を抑えることにもつながります。さらに、次の世代を得るのに数年を要するサルなどの動物では、初代の個体で結果を確認できる意義は極めて大きいと考えられます。
本研究成果は、2026年3月23日付けで国際学術誌「Communications Biology」に掲載されました。
遺伝子を改変した動物は、病気の原因を調べたり、新しい治療法や薬の候補を評価したりするために必要不可欠です。近年は、受精卵の段階で遺伝子に変化を入れる「ゲノム編集」技術が広く使われるようになり、これまでより短い時間で研究用の動物を作れるようになってきました。
一方で、受精卵で遺伝子改変を行うと、同じ設計を使っても個体ごとに起こる変化が違ったり、1匹の体の中に複数の異なる変化が混ざったり(モザイク変異※5)して、狙った通りの結果にならないことがあります。その場合、「どの個体が目的に合っているか」を確かめるために多くの個体を作って調べる必要があり、時間が増えるだけでなく、動物の使用数も増えやすくなります。
さらに、次の世代を作って遺伝子の状態をそろえてから詳しく解析する進め方をとることも多くありますが、世代交代に時間がかかる動物では、研究開始までに長い期間が必要になります。特に、サルなど世代の長い動物では、目的の個体を得るまでの負担が大きく、研究を加速するためには「初代の個体で狙い通りの結果を得やすくする」工夫が強く求められていました。
こうした背景から、受精卵での遺伝子改変をより安定して行い、どのような結果が起こるかを前もって見通して、無駄の少ない実験計画につなげる方法の確立が課題となっていました。
本研究では、受精卵で遺伝子改変を行う前に、「どの設計なら狙い通りの変化が起こりやすいか」をできるだけ事前に見極めるための手順を組み立てました。
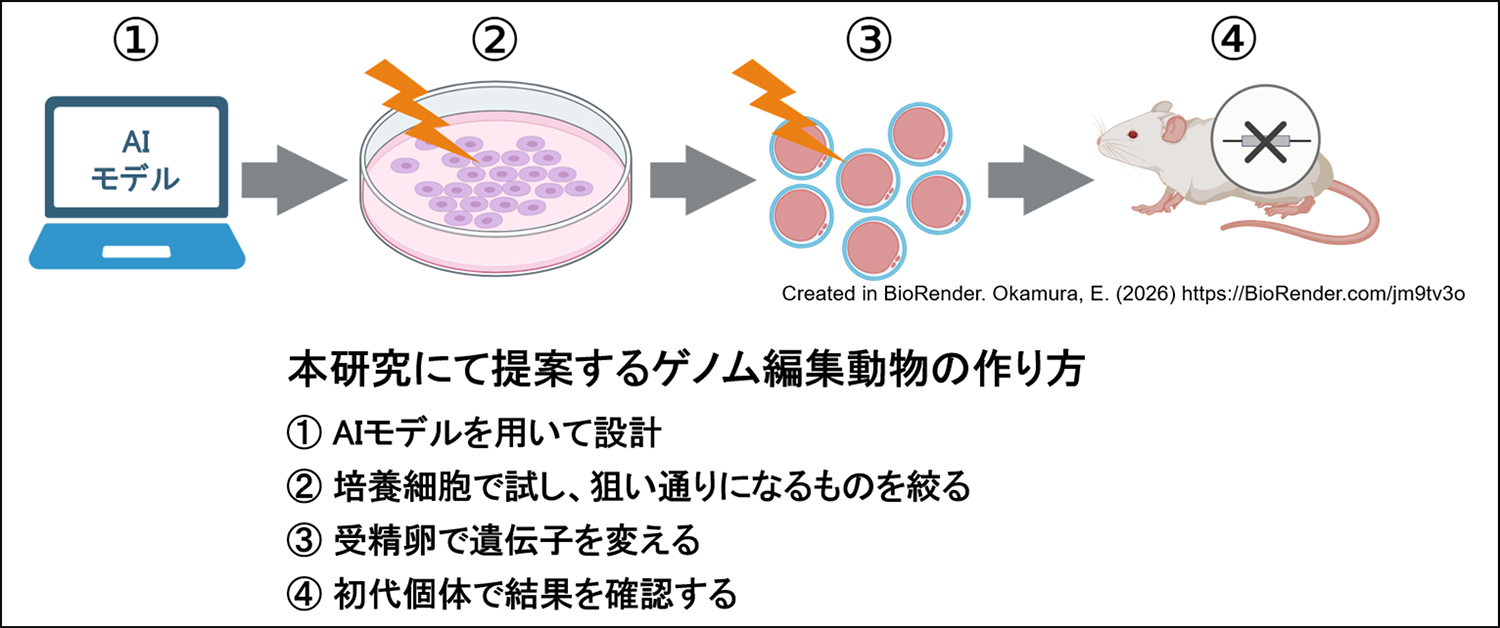
まず、AIモデルを用いて、遺伝子を切り替えるための設計候補について「改変後に起こりやすい変化」を予測し、狙った結果につながりやすい候補を選びました。次に、絞り込んだ候補を培養細胞で実際に試し、予測通りの変化が起こりやすいかどうかを確かめました。そのうえで、事前確認で有望と判断した設計を用いて、マウス受精卵で遺伝子改変を実施しました。
実際に、複数の遺伝子を標的とした実験で、狙い通りに遺伝子の働きを失わせる(ノックアウト※6)ことができ、初代の個体で期待される変化(表現型)を確認できることを示しました。
このように本研究は、受精卵での遺伝子改変を「やってみないと分からない」状態から一歩進め、事前の予測と確認に基づいて成功しやすい設計を選び、無駄を減らして実験を進めるための実用的な手順を提示したものです。
この方法により、遺伝子改変動物を作る作業が速くなり、狙い通りの結果を得られる確かさも高まると期待されます。また、狙い通りにならない個体を減らせるため、必要な動物の数を抑えることにもつながります。さらに、次の世代を作って確認する前に、初代の個体で結果を確かめやすくなることで、研究の進め方がよりスムーズになります。特に、次の世代を得るのに時間がかかるサルなどの動物では、初代の個体で結果を確認できる意義が大きく、研究の時間と負担を減らすことに役立つと考えられます。
- 論文名
Optimizing CRISPR Precision in Mouse Embryos via Microhomology-Mediated End Joining-Dominant Targeting - ジャーナル名
Communications Biology - 著者
Khanui Lkhagvadorj#, Eiichi Okamura#,*, Taito Taki, Hayate Suzuki, Akihiro Kuno, Yasushi Itoh, Seiya Mizuno, Knut Woltjen*, Masatsugu Ema*
#:共同筆頭著者
*:共同責任著者
本研究は、科学研究費助成事業(科研費)(課題番号:25K02195、24K18045、23H03860)および国立研究開発法人日本医療研究開発機構(AMED)(事業名:ワクチン開発のための世界トップレベル研究開発拠点の形成事業、研究開発課題名:霊長類モデルを用いたワクチン評価に関するサポート機関)の助成を受けて実施されました。
※1 CRISPR/Cas9(クリスパー/キャスナイン)
狙ったDNA配列を認識する「ガイドRNA (gRNA)」と、DNAを切断する酵素「Cas9」を組み合わせて、特定の遺伝子を改変できるゲノム編集技術。切断後に細胞の修復機構が働くことで、遺伝子の働きを失わせる(ノックアウトする)などの変化が生じる。
※2 inDelphi
2018年に報告された、CRISPR/Cas9などでDNAが切断された後、細胞の修復によって生じる欠失・挿入(インデル)の起こりやすさを、大規模データに基づく機械学習で予測するモデル。(MV Shen, Nature, 2018)
※3 ES細胞(胚性幹細胞)
受精卵が発生した胚盤胞から樹立され、さまざまな細胞に分化できる性質をもつ細胞。本研究では、受精卵で編集を行う前に、候補gRNAでどのような変異が起こりやすいかを事前に確かめる検証系として用いた。
※4 初代の個体
受精卵にゲノム編集を施して得られた「最初の世代」の個体。通常は次世代(F1)を作って遺伝子型を揃えることが多いが、初代個体で狙い通りの変異が得られれば、より迅速に解析できる。
※5 モザイク変異
同じ個体の中に、異なる遺伝子型の細胞が混在する状態。受精卵でゲノム編集を行うと、発生初期の複数の細胞分裂の段階で編集が起こりうるため、個体内で複数種類の変異が混じり、解析が難しくなることがある。
※6 ノックアウト
遺伝子の働きを失わせること。CRISPR/Cas9で遺伝子を切断し、修復の過程で欠失などの変異が入ることで、遺伝子機能が失われる状態を作る。























