
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年3月25日
ヒトiPS細胞由来の間葉系間質細胞(MSC)とそこから分泌される細胞外小胞は抗炎症・免疫調節能をもつ ー次世代の細胞療法や「EV療法」への応用に期待ー
ポイント
- ヒトiPS細胞から動物由来成分を用いずに誘導した間葉系間質細胞「XF-iMSC」が炎症性サイトカインの分泌を抑制する抗炎症効果をもつことを確認した。
- XF-iMSCから分泌される細胞外小胞「XF-iEv」が抗炎症効果に関わることを示した。
- XF-iMSCおよびXF-iEvは、T細胞の増殖や活性化を抑制する免疫調節能を示した。
- XF-iEvは、生体組織由来MSCの細胞外小胞と組成が一部異なり、神経・骨格筋再生に関連する成分が含まれていることを明らかにした。
池谷真 准教授(CiRA臨床応用研究部門、タケダ-CiRA共同研究プログラム(T-CiRA))、上谷大介 特命助教(CiRA同部門、T-CiRA(いずれも研究当時))および小茂池勇作 主任研究員(武田薬品工業株式会社、T-CiRA)らの共同研究グループは、ヒトiPS細胞から作製した間葉系間質細胞(MSC)注1)とその分泌物である細胞外小胞(EV)注2)の機能を詳細に解析しました。その結果、これらが炎症反応を抑制し、過剰な免疫反応を調節する優れた能力をもつことを実証しました。特に、細胞の分泌物であるエクソソームなどの細胞外小胞が単独でも高い治療効果をもつ可能性を示した点は、将来の「無細胞療法」への応用にも重要な知見となります。
本研究成果は、2026年2月26日に国際科学誌「Regenerative Therapy」にオンライン掲載されました。
間葉系間質細胞(MSC)は、骨、軟骨、脂肪などへ分化する能力に加えて、炎症を抑えたり免疫を調節したりする作用を示し、再生医療の有力な細胞源として期待されています。現在は主に骨髄や脂肪などの生体組織から採取されたMSCが利用されていますが、細胞提供者ごとの品質のバラつきや、採取できる細胞数が限られることが課題となっています。
これらの課題を解決するため、iPS細胞から誘導する間葉系間質細胞「iMSC」の研究が進んでいます。研究グループはこれまでに、動物由来成分を含まない「アニマルフリー(Xeno-Free; XF)」の条件下で、ヒトiPS細胞から神経堤細胞(NCC)注3)を経由してMSC(XF-iMSC)を効率よく誘導する方法を確立し、組織再生能力があることを報告しました(CiRAニュース 2022年9月15日、CiRAニュース 2024年10月7日)。しかし、このXF-iMSCがもつ抗炎症・免疫調節機能や細胞が分泌する細胞外小胞の効果については十分に解明されていませんでした。
1)ヒトiPS細胞由来XF-iMSCの特性評価
本研究では、ヒトiPS細胞からNCCを経由して誘導した間葉系間質細胞(MSC)であるXF-iMSCを解析しました。XF-iMSCは、MSCの指標である細胞表面タンパク質(CD44, CD73, CD105)を発現しており、さらに骨、軟骨、脂肪細胞への分化能を保持していることが確認されました(図1)。
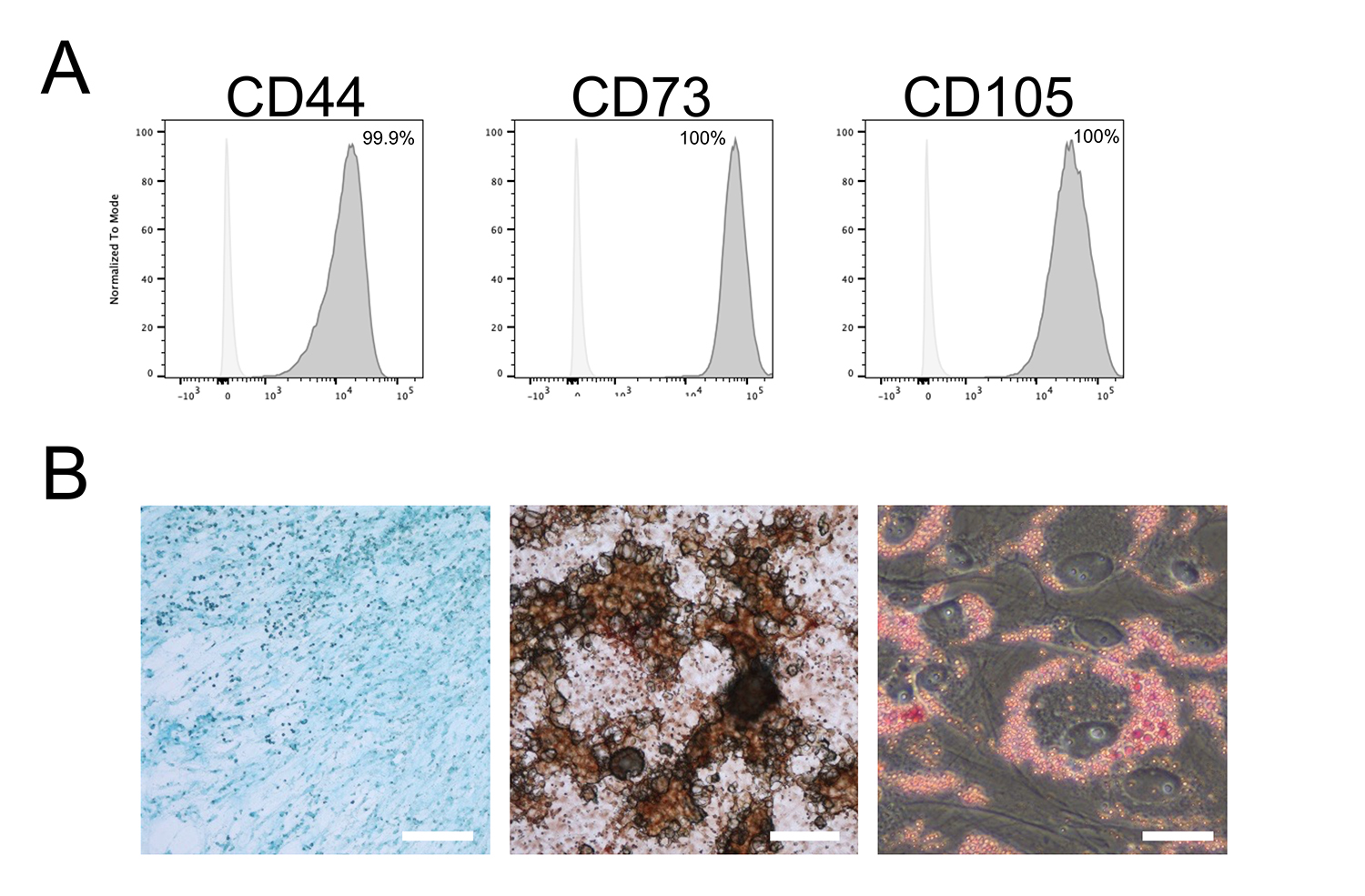
図1. XF-iMSCの特性評価
A:XF-iMSCはMSCに特徴的な細胞表面タンパク質が発現している。
B:XF-iMSCはMSCとしての軟骨(左:アルシアンブルー染色)、骨(中央:アリザリンレッド染色)、脂肪(右:オイルレッド染色)への分化能を示す。
2)XF-iMSCおよびXF-iEvによる抗炎症効果の検証
炎症を誘発する物質(LPS)で刺激したヒトおよびマウスの末梢血単核球(PBMC)注4)に対する、XF-iMSCと、XF-iMSCが分泌する細胞外小胞(XF-iEv)の作用を検証しました 。その結果、XF-iMSCおよびXF-iEvは、LPS刺激で誘発されるPBMCからの炎症性サイトカイン注5)(IL-6やTNF-α)の分泌を有意に抑制しました 。この抑制効果は、既存の生体組織(脂肪)由来MSC(hAC-MSC)やその細胞外小胞(hAC-iEv)と同等以上であることが示されました(図2)。
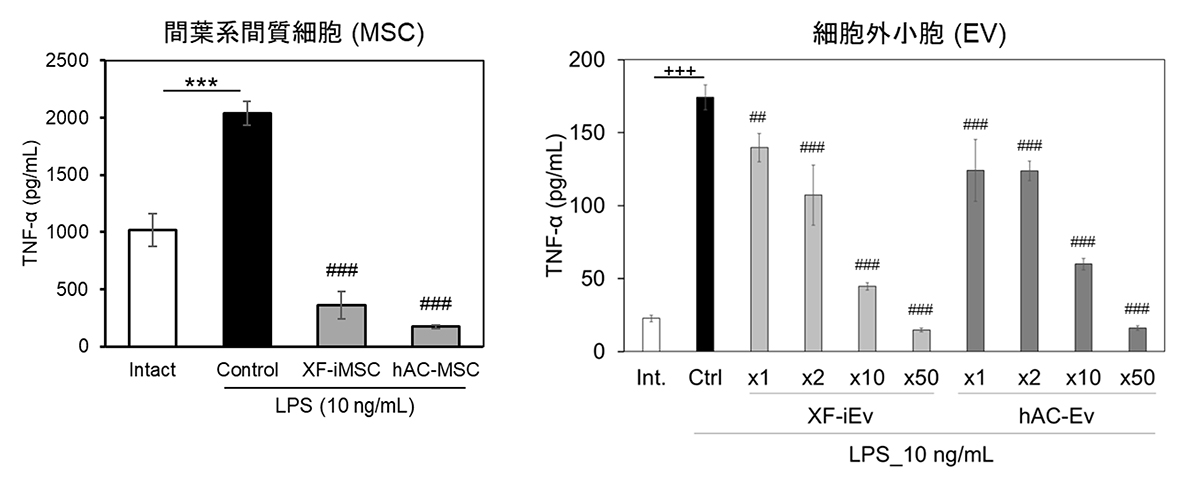
図2. 炎症性サイトカインの分泌抑制効果の検証
左:LPS刺激によって活性化されるマウスの末梢血単核球のTNFαの発現量が、XF-iMSCおよびhAC-MSCにより抑制される。
右:LPS刺激によって活性化されるマウスの末梢血単核球のTNFαの発現量が、XF-iEvおよびhAC-Evにより抑制される。
3)T細胞に対する免疫調節能の解析
次に、免疫反応の中核を担うT細胞の増殖に対する影響を調べました。XF-iMSCはT細胞の増殖を約80%抑制し、その能力は既存の組織由来MSCと同等でした(図3)。
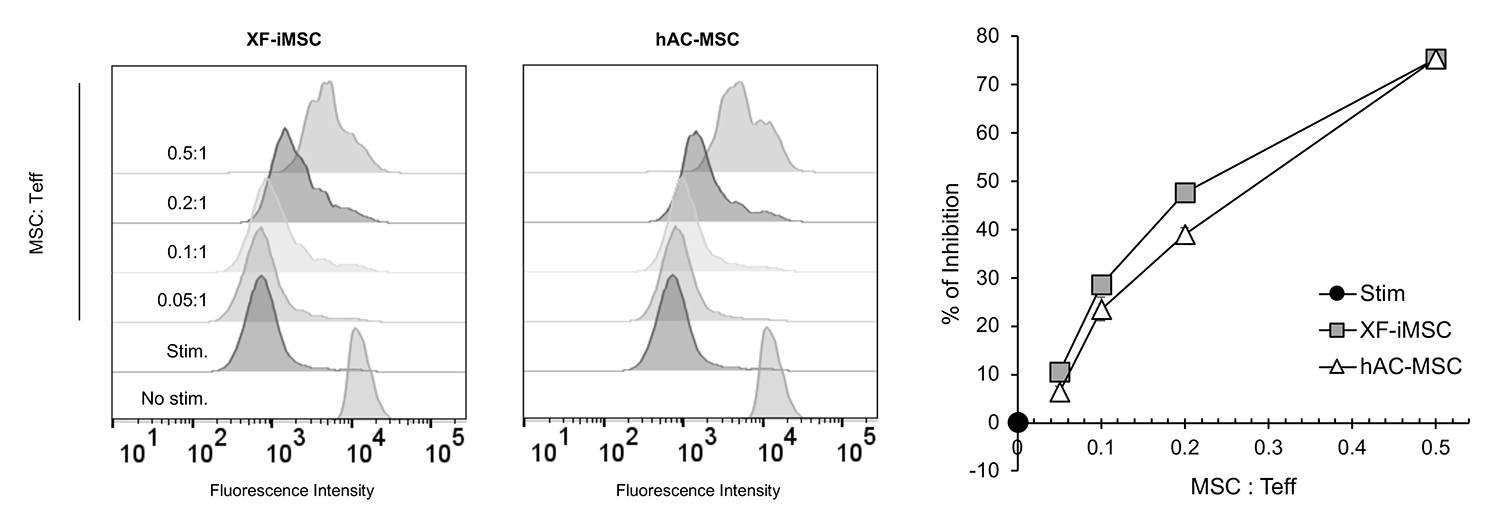
図3. T細胞増殖抑制のグラフ
ヒト末梢血単核球のT細胞受容体刺激によって誘導されるエフェクターT細胞(Teff)注6)の増殖をXF-iMSCが抑えるかどうかを検証した。
左、中:蛍光標識したヒト末梢血単核球とXF-iMSCまたは脂肪由来hAC-MSCを異なる比率で4日間共培養し、細胞増殖に応じて減弱する蛍光強度をフローサイトメトリーで測定した。
右:T細胞の増殖がどの程度抑えられたかを抑制率(%)で算出した。
4)細胞外小胞(XF-iEv)に含まれるタンパク質の網羅的解析
XF-iEvがもつ治療効果のメカニズムを探るため、プロテオーム解析(タンパク質の網羅的解析)を実施しました。XF-iEvからは1217種類のタンパク質が同定され、既存の組織由来MSCのEVには少ない、MidkineやPleiotrophinをはじめとした神経・骨格筋再生に関連する成分が含まれていることがわかりました。
本研究により、ヒトiPS細胞からNCCを経由して作製されたXF-iMSCおよびその細胞外小胞が、優れた抗炎症・免疫調節能をもつことが明らかになりました。アニマルフリーで安定供給が可能なこれらの細胞や小胞は、従来の組織由来MSCの自己免疫疾患や炎症性疾患への利用に代わる新しい治療手段として、治療への応用が期待されます。
- 論文名
Anti-inflammatory and immunomodulatory effects of human induced pluripotent stem cells-derived mesenchymal stem/stromal cells and their extracellular vesicles - ジャーナル名
Regenerative Therapy - 著者
Yusaku Komoike1,2, Daisuke Kamiya2,3,*, Haruka Sasaki-Ban1, Atsushi Matsuda1,2, Hirokazu Matsumoto1,2, Makoto Ikeya2,3,*
*:責任著者 - 著者の所属機関
- 武田薬品工業株式会社 T-CiRAディスカバリー&イノベーション
- タケダ-CiRA共同研究プログラム(T-CiRA)
- 京都大学iPS細胞研究所(CiRA)
本研究は、下記機関より支援を受けて実施されました。
- タケダ-CiRA共同研究プログラム(T-CiRA)
注1)間葉系間質細胞(Mesenchymal Stem/stromal Cell, MSC)
骨・軟骨・脂肪細胞などといった間葉系の細胞に分化する能力を持った間質(結合組織)の細胞。本報では、iPS細胞から作製したものをiMSC(iPSC-derived Mesenchymal Stem/stromal Cell)としている。
注2)細胞外小胞(EV)
細胞から分泌される直径40〜200nm程度の膜に包まれた微細な粒子。タンパク質や核酸を含み、細胞間の情報伝達を担う。
注3)神経堤細胞(NCC)
発生過程で一時的に現れる細胞で、神経系や骨、軟骨、MSCなど多様な細胞に分化する能力を持つ。
注4)末梢血単核球(PBMC)
血液中に含まれるリンパ球や単球などの単核細胞の総称。免疫反応の解析に広く用いられる。
注5)炎症性サイトカイン
細胞から分泌されるタンパク質の一種で、細胞間の情報伝達を担う「サイトカイン」のうち、炎症を促進するもの。サイトカインには炎症を抑制するものもある。
注6)エフェクターT細胞
T細胞は胸腺で作られたのち、自身が反応する抗原を認識し活性化するまで「ナイーブT細胞」として体内を循環(パトロール)する。ナイーブT細胞が特異的な抗原を認識することで活性化し、エフェクターT細胞となり活発に増殖し、さまざまな免疫反応を引き起こす。























