
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年3月31日
ヒトiPS細胞から後脳特異的な神経幹細胞を安定的に誘導・維持する手法を開発
―後脳の発達解明や神経変性疾患の病態解明・創薬研究への貢献に期待―
ポイント
- ヒトiPS細胞から後脳領域の特性を持つ神経幹細胞(hindbrain-like induced NSC; Hb-LiNSCs)を作製する新たな分化誘導法を確立した。
- この方法は、3種類の特定の低分子化合物の組み合わせにより、動物由来成分や成長因子bFGFを用いない条件で、簡便かつ安定的にHb-LiNSCを誘導・維持することが可能である。
- 誘導されたHb-LiNSCsは、1年間以上の長期培養後も、後脳としての領域特異性と分化能、正常な核型を維持することを示した。
- Hb-LiNSCsから分化した神経細胞は、機能的なネットワーク形成と電気信号の伝達が確認され、マウス脳内へ移植すると周囲の組織へ生着・分化することを示した。
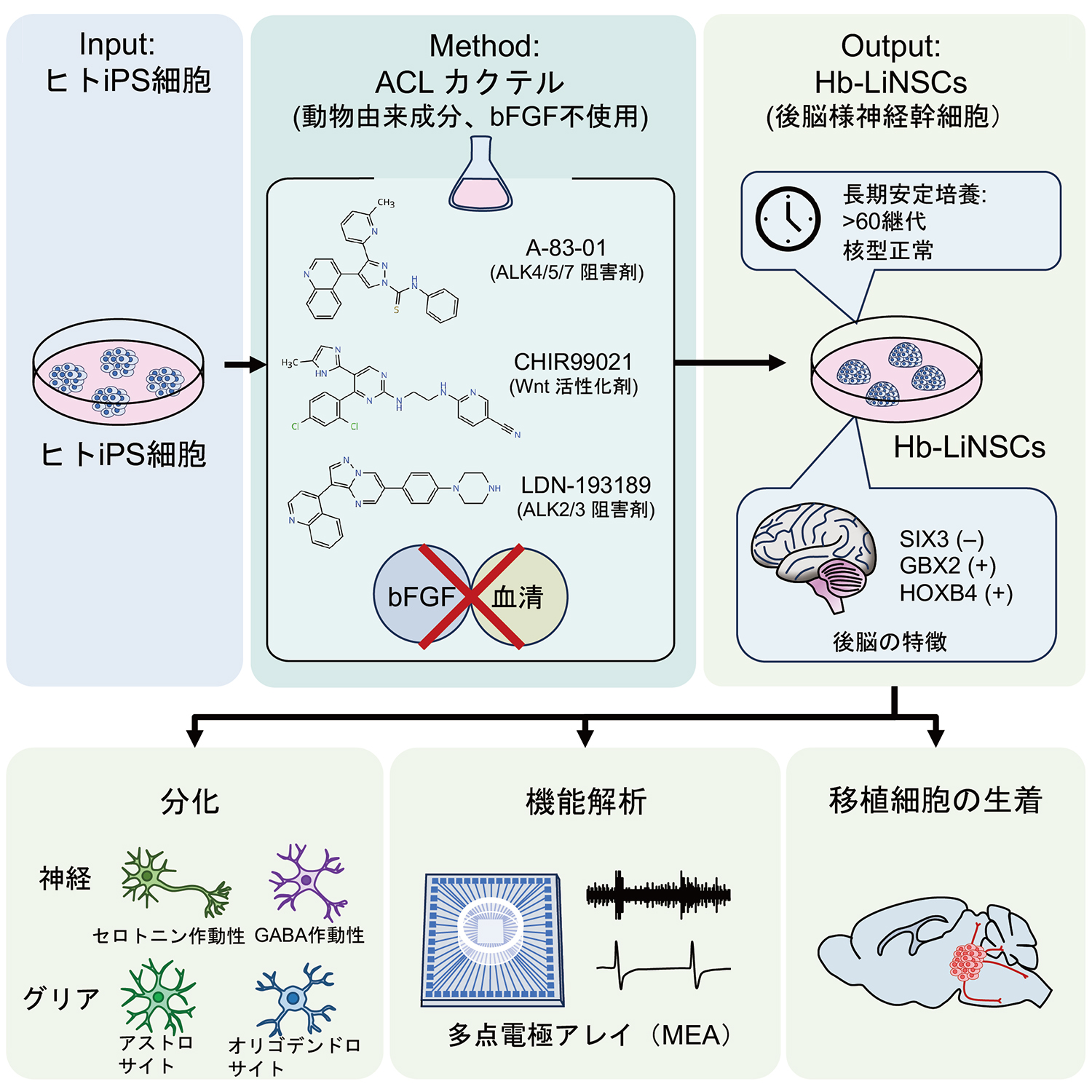
本研究の概要
池谷真 准教授(CiRA臨床応用研究部門)らの研究グループは、ヒトiPS細胞から後脳注1)の性質を持つ神経幹細胞注2)(後脳様神経幹細胞、Hb-LiNSCs)を、簡便かつ安定的に作製する新手法を開発しました。これまで、多能性幹細胞から後脳の神経幹細胞を誘導する方法は報告されていましたが誘導した神経幹細胞の特性を長期間にわたって維持し培養する方法は確立されていませんでした。本研究では、3種類の低分子化合物を組み合わせた「ACLカクテル注3)」を用いることで、後脳特異的なマーカーを発現する神経幹細胞の誘導に成功しました。さらに、開発した培養方法は、誘導後も1年間以上の長期間にわたって後脳領域の特性をもった神経幹細胞として増殖・分化能を維持できることを示しました。この手法は、脊髄小脳変性症や脳幹腫瘍などの後脳領域(橋(きょう)、小脳、延髄)に関連する神経疾患の病態解明や創薬研究において、信頼性の高いヒト細胞モデルを構築するための重要な基盤技術となります。
本研究成果は、2026年3月30日(米国東部時間)に国際科学誌「Cell Reports Methods」に掲載されました。
神経幹細胞は、神経細胞やグリア細胞へと分化する能力を持ち、神経疾患の疾患モデルや再生医療の研究に不可欠な細胞です。中枢神経系の発生では、前脳、中脳、後脳、脊髄など、その領域によって役割が異なり、それぞれの領域に応じた神経幹細胞が分化していきます(領域特異性注4))。後脳領域に相当する橋(きょう)、小脳、延髄は、呼吸や循環などの生命維持に関わる重要な部位ですが、患者さんから神経幹細胞を直接採取することは、組織損傷のリスクや倫理的な観点から極めて困難です。そのため、これまでにiPS細胞から後脳の神経幹細胞の誘導法の研究が進められ、開発されていましたが、一方で、その性質を維持したまま長期間培養する方法は開発されていませんでした。中間段階の細胞を長期間維持・拡大培養することが可能になれば、毎回iPS細胞から誘導する手間を省くことができるだけでなく、均質な細胞を必要なときに大量供給できるようになります。これにより、実験の再現性を高めることや、創薬研究での実用化に向けた薬剤スクリーニングなどの大規模な実験が可能となります。
1)ACLカクテルによる後脳様神経幹細胞(Hb-LiNSCs)の誘導
研究グループは、TGF-β注5)阻害剤(A-83-01)とWntシグナル注6)活性化剤(CHIR99021)とBMP注7)阻害剤(LDN-193189)をそれぞれ適切な濃度で組み合わせた「ACLカクテル」を開発しました。このカクテルを用いることで、ヒトiPS細胞から1週間で、ドーム状の形態をした後脳様神経幹細胞(Hb-LiNSCs)を効率よく誘導することに成功しました。この手法は動物由来成分や高価な成長因子(bFGF)を必要とせず、また複数の異なるヒトiPS細胞株で同様のHb-LiNSCsが誘導できるという高い再現性を示しました。(図1)
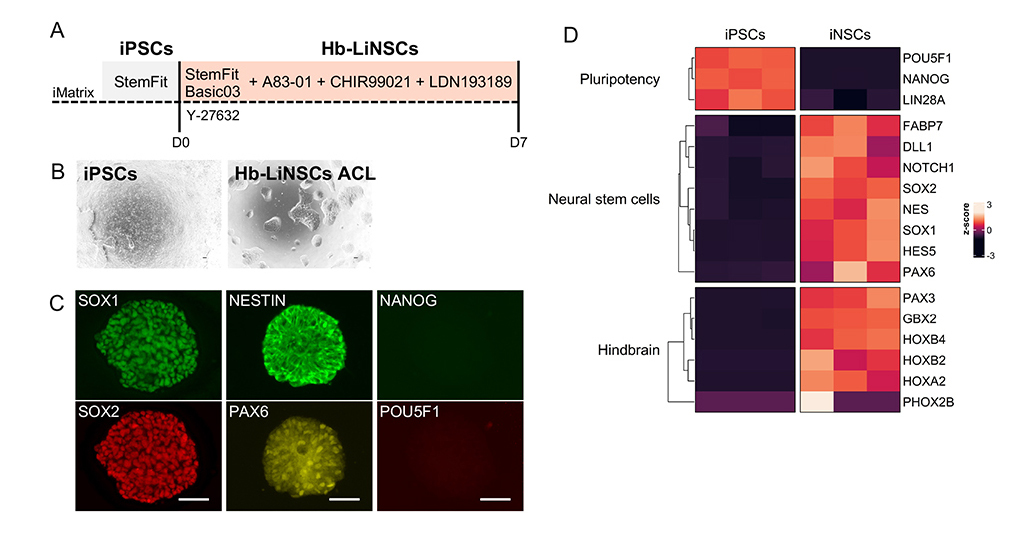
図1. Hb-LiNSCsの誘導
A:誘導法の模式図。
B:iPS細胞と誘導後のHb-LiNSCsの明視野画像。
C:各種神経幹細胞への分化の指標となる遺伝子(マーカー)の発現。神経幹細胞マーカー(SOX1, SOX2, NESTIN, PAX6)が陽性、多能性幹細胞マーカー(NANOG, POU5F1)が陰性。
D:ヒートマップによる遺伝子発現解析。誘導後の細胞は神経幹細胞マーカー(Neural stem cells)および後脳神経幹細胞マーカー(Hindbrain)を発現する。
2)1年間以上にわたる長期安定性の実証
Hb-LiNSCsを、誘導後も継続してACLカクテル存在下で一週間に一度の継代を行いながら培養し続けました。その結果、誘導した細胞が1年間以上(53継代)にわたって、後脳特異的な遺伝子(GBX2, HOXB4など)の発現と、正常な染色体核型を維持し続けることが分かりました(図2A,B)。また、継代初期(10回目まで)は脊髄の指標となる遺伝子(HOXB7やHOXB9)を同時に発現し、中期以降(20回目以降)は後脳神経幹細胞の遺伝子発現パターンを維持することが分かりました(図2C)。この結果は、単一細胞ごとの遺伝子発現パターンを解析するシングルセル解析でも確認されました(図2D)。
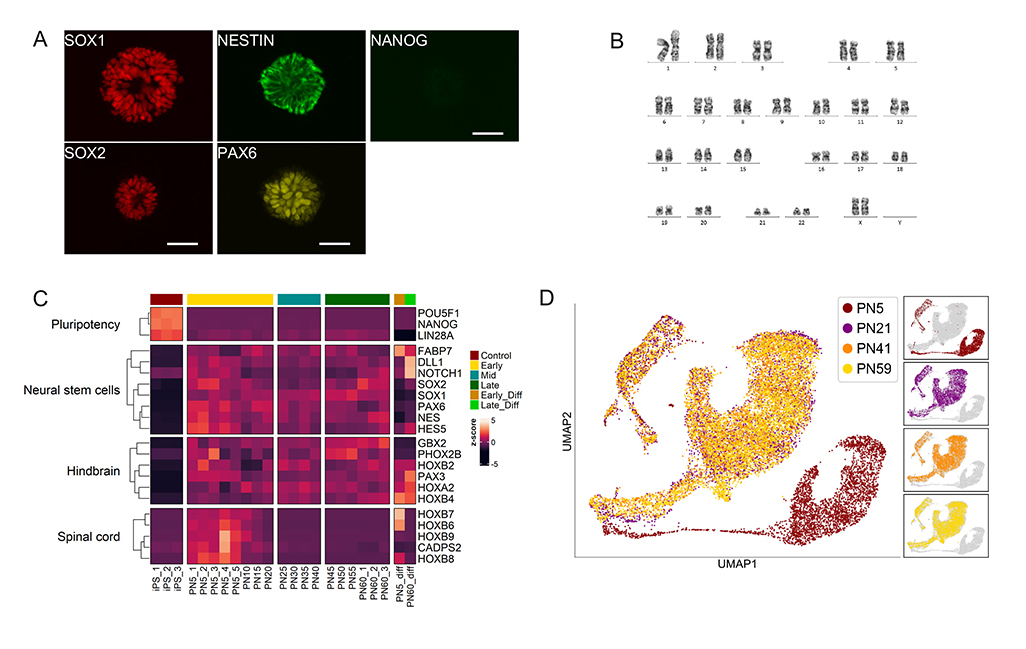
図2. 長期間継代培養後も細胞は後脳様の特徴を維持している
A:各種神経幹細胞マーカーの発現(60回継代後)。神経幹細胞マーカー(SOX1, SOX2, NESTIN, PAX6)が陽性、多能性幹細胞マーカー(NANOG)が陰性。
B:核型解析。長期培養後(53回継代後)も核型は正常。
C:ヒートマップによる遺伝子発現解析。各継代で、細胞は神経幹細胞マーカーおよび後脳神経幹細胞マーカーを発現するが、初期(10継代まで)は脊髄マーカーも発現する。
D:継代5, 21, 41, 59回目(PN5, 21, 41, 59)のHb-LiNSCsのシングルセル解析。継代21以降は同一の細胞集団により構成されていることがわかる。
3)多様な神経細胞への分化と機能評価
後脳様神経幹細胞の状態を維持するACLカクテルを除いた培地でHb-LiNSCsを培養したところ、各細胞の指標となる遺伝子TUBB3(神経細胞)、OLIG2(オリゴデンドロサイト注8))、GFAP(アストロサイト注9))、FEV、TPH2、SLC6A4(いずれもセロトニン作動性神経細胞注10))の発現が誘導され、Hb-LiNSCsから神経系の分化が進むことを確認しました(図3A,B,C)。電極を用いた解析(MEA解析注11))では、Hb-LiNSCsから分化した神経細胞が機能的なネットワークを形成し、電気信号をやり取りしていることが示唆されました(図3D)。また、マウスの後脳領域へHb-LiNSCsから分化した神経細胞の集合体(ニューロスフェア)を移植した実験でも、細胞が死滅することなく生着し、より成熟した神経細胞へと分化することを確認しました(図4)。
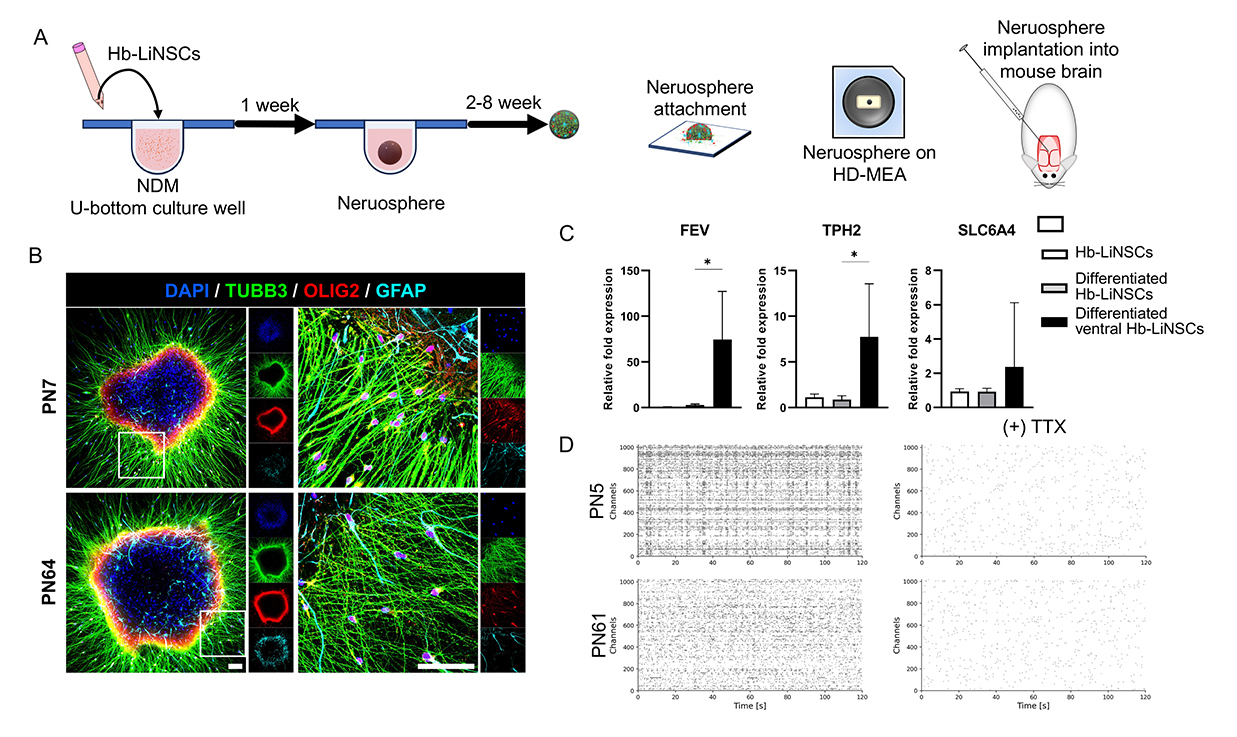
図3. in vitroでの神経分化
A:実施した実験の模式図。ACLカクテルを除いた培地で神経細胞を分化させ、神経細胞からなる3次元集合体のニューロスフェアの形成を誘導した。ニューロスフェアを培養皿に播種し、神経細胞への分化を行なった(図3B,C)。また、ニューロスフェアを高密度微小電極アレイシステム(HD-MEA)上に配置し、神経細胞の電気的活動を計測した(図3D)。さらに、ニューロスフェアをマウスの後脳領域に移植する実験も行った(図4)。
B:各種細胞のマーカーである、TUBB3(神経細胞)、OLIG2(オリゴデンドロサイト)、GFAP(アストロサイト)の遺伝子発現が誘導された。
C:ニューロスフェアにSHHシグナル注12)を活性化させる化合物(SAG)とFGF4を作用させたところ、セロトニン作動性神経マーカー(FEV, TPH2, SLC6A4)の発現が誘導された。
D:ニューロスフェアの電極アレイ解析。同調した神経の発火が観察され(左)、その発火は神経毒(テトロドトキシン、TTX)により消失した(右)。
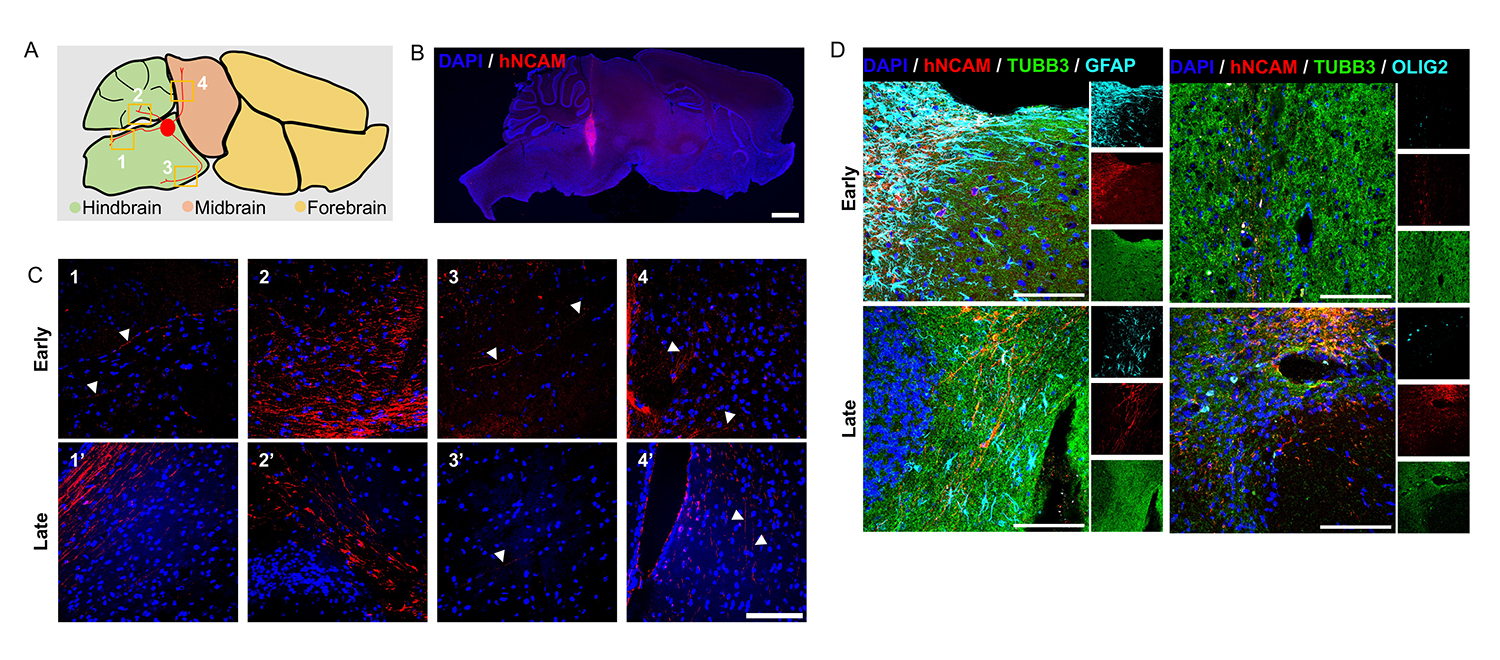
図4. in vivoでの神経分化
A:マウス脳への移植部位の模式図。後脳(Hindbrain)領域に移植した。
B:マウス脳の矢状断像。hNCAMで染色された細胞(図中赤色)が移植細胞。
C:移植したHb-LiNSCs由来ニューロスフェアの神経突起が、本来の投射先である脊髄小脳路 (1, 1')、小脳 (2, 2')、皮質脊髄路 (3, 3')、および中脳 (4, 4') 領域で、hNCAM陽性として観察された。1, 2, 3, 4が継代初期(継代7回)、1', 2', 3', 4' が継代後期(継代67回)のニューロスフェア移植体。
D:継代初期および後期ニューロスフェア移植体の両方で、各種細胞のマーカーである、TUBB3(神経細胞)、GFAP(アストロサイト)、OLIG2(オリゴデンドロサイト)を発現する細胞への分化が観察された。
本研究で確立されたヒトiPS細胞から後脳様神経幹細胞(Hb-LiNSCs)を分化誘導し維持培養できる手法により、ヒトの後脳神経系を再現できる安定した細胞の供給源が確保されました。Hb-LiNSCsを用いることで、これまで困難であった後脳特異的な疾患のメカニズム解明や、効率的な薬剤スクリーニングが進むことが期待されます。また、長期にわたって領域特異性を維持できるという知見は、他の脳領域の細胞作製における技術開発にも示唆を与えると期待されます。
- 論文名
Wnt activation and dual SMAD inhibition for induction and maintenance of hindbrain-like neural stem cell from hiPSCs - ジャーナル名
Cell Reports Methods - 著者
Ziadoon Al-Akashi1, Denise Zujur1, Nicholas Boyd-Gibbins1, Nathalie Eileen Wiguna1, Masato Nakagawa1, Tetsuhiro Kikuchi1, Asuka Morizane1,2, Jun Takahashi1, Makoto Ikeya1,*
*:責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 神戸市立医療センター中央市民病院 再生医療研究部
本研究は、下記の支援を受けて実施されました。
-
日本医療研究開発機構(AMED)
- 再生医療実現拠点ネットワークプログラム
「再生医療用iPS細胞ストック開発拠点」- 再生・細胞医療・遺伝子治療実現加速化プログラム
「次世代医療を目指した再生・細胞医療・遺伝子治療研究開発拠点」 - iPS細胞研究基金
- 日本学術振興会(JSPS)科学研究費助成事業(16H05447)
- 科学技術振興機構(JST)次世代研究者挑戦的研究プログラム(JPMJSP2110)
- 公益財団法人 大塚敏美育英奨学財団
注1)後脳
脳幹の一部(橋や延髄)および小脳を含む脳の領域。呼吸、循環、運動調節などの生命維持に不可欠な機能を担う。
注2)神経幹細胞
自己複製能(自分と同じ細胞を増やす能力)と、神経細胞やグリア細胞に分化する能力を併せ持つ細胞。英語では、Neural Stem Cells(NSCs)という。
注3)ACLカクテル
A-83-01(TGF-β阻害剤)、CHIR99021(Wnt活性化剤)、LDN-193189(BMP阻害剤)の3つの低分子化合物の組み合わせ。
注4)領域特異性(Regional identity)
発生の過程で、脳のどの場所になるかが決定される性質のこと。
注5)TGF-β
細胞の増殖や免疫機能の維持を制御する重要な細胞内の情報伝達(シグナル伝達)を担うタンパク質(サイトカイン)。
注6)Wntシグナル
Wntリガンドが受容体であるFrizzledを介して活性化する細胞内のシグナル伝達系。
注7)BMP
骨組織や軟骨の分化を誘導、促進するタンパク質。
注8)オリゴデンドロサイト
神経細胞の機能をサポートするグリア細胞(支持細胞)の一種。神経細胞から伸びる軸索に巻き付き、髄鞘(ずいしょう)を形成し、神経伝達の高速化にかかわる。
注9)アストロサイト
神経細胞の機能をサポートするグリア細胞(支持細胞)の一種。血管と神経細胞のあいだの栄養物質の輸送や血液脳関門の形成、神経細胞同士の情報伝達が起きるシナプスでの神経伝達物質の回収などを行い、脳内の環境を保つ。
注10)セロトニン作動性神経細胞
神経伝達物質「セロトニン」を放出して脳内の情報伝達を行う神経細胞。
注11)MEA(多点電極アレイ)解析
細胞の外側に配置した多数の電極により、神経細胞の電気的な活動(スパイク)を網羅的に計測する手法。
注12)SHHシグナル
SHHタンパク質が受容体に結合して活性化される細胞内のシグナル伝達系。























