
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年4月23日
人工胸腺オルガノイドによるヒトiPS細胞由来CD4⁺T細胞療法の開発と評価
ポイント
- ヘルパーT細胞による免疫細胞の活性化機能とキラーT細胞などでみられる細胞傷害機能の両方を併せ持つ、ヒトiPS細胞由来のCAR-CD4+T細胞(CAR-iCD4+T細胞)を作製した。
- ヒトiPS細胞由来CD8+T細胞(iCD8+T細胞)と比較して、iCD4+T細胞は高い増殖能とよりメモリー様の表現型を示した。
- 血液系腫瘍モデルにおいて、CAR-iCD4+T細胞の単独使用は、CAR-iCD8+T細胞単独あるいはCD4/CD8併用と比較して、より優れた治療効果を示した。
郭清怡 特定研究員(CiRA臨床応用研究部門(研究当時:大学院生))、金子新教授(CiRA同部門)らの研究グループは、人工胸腺オルガノイド(Artificial Thymic Organoid:ATO)注1)を用いて、ヒトiPS細胞から、ヘルパー機能注2)と細胞傷害(キラー)機能注3)の双方を兼ね備え、がんに対して長期にわたる持続的な免疫反応が期待できるCAR-CD4+T細胞を作製する手法を開発しました。
患者さん自身のT細胞に遺伝子改変を加え、がん細胞を特異的に攻撃する能力を持たせる「CAR-T療法注4)」は、高精度にがんを攻撃する治療法として注目されています。しかし、患者さんのT細胞は、がんの進行や治療の過程で「疲弊注5)」して攻撃力が落ちてしまい、CAR-T療法に利用してもがんを完治させることが難しいという課題がありました。さらに近年、がんに対する持続的な免疫反応を実現するためには、CD8を発現する(CD8+)細胞障害性T細胞による細胞障害(キラー)機能だけでなく、CD4+T細胞による免疫細胞の活性化を行うヘルパー機能が重要であることが明らかになってきています。
研究グループはこれまでに、iPS細胞への初期化によって、細胞増殖などの能力を若返らせたCD8+キラーT細胞(iCD8+T細胞)の作製と臨床応用に向けた技術改良に取り組んでいます。本研究では、がんに対する免疫細胞療法の効果をさらに高めることを目指し、人工胸腺オルガノイド(ATO)を用いてヒトiPS細胞からCD4+T細胞を作製し、がん細胞への免疫機能の解析を行いました。その結果、iPS細胞から作製したCD4+T細胞は、ヘルパーT細胞に特徴的なサイトカイン注6)などを発現し、他の免疫細胞の増殖を促進するヘルパー機能を持ち、がん細胞を直接攻撃する細胞傷害活性の持続、優れた増殖能、さらに疲弊しにくい特性が確認されました。これらの成果から、iPS細胞から作製するCD4+T細胞が免疫療法において高い治療効果を発揮する可能性が期待できると考えられます。
本研究成果は、2026年1月3日に科学誌「Inflammation and Regeneration」に掲載されました。
iPS細胞は、細胞培養により増殖し続け、大量に使えることから、免疫細胞療法のためのT細胞を製造するための細胞資源として注目されています。これまで、iPS細胞から分化させたCD4+T細胞の機能が未解明であったため、iPS細胞由来T細胞による治療法開発は、CD8+T細胞が中心となっていました。しかし、ヘルパー機能を持たないCD8+T細胞のみでは、治療効果の持続性や臨床応用の拡大に課題が残されていました。
近年、T細胞が作られる臓器「胸腺」を細胞・組織レベルで再現した「人工胸腺オルガノイド(Artificial Thymic Organoid:ATO)」と共培養することで、iPS細胞からCD4+T細胞を分化誘導することが可能となりました。生体内のCD4+T細胞は、周囲の環境に応じて他の免疫細胞を活性化または抑制させる複数種のT細胞へとさらに分化します。しかし、iPS細胞から人工胸腺オルガノイドによって誘導したCD4+T細胞の機能については十分に解明されていませんでした。
これまでは、iPS細胞から免疫抑制注7)機能をもつCD4+T細胞である制御性T細胞(iTreg)を作製する研究が主流でした。一方で、CD4+T細胞はがんに対する幅広い免疫応答に関わることが知られています。CD4+T細胞は、CD8+T細胞の機能を補助・増強するだけでなく、抗原提示細胞注8)の活性化を介して攻撃対象のより効率的な認識が可能となるエピトープ拡大注9)の誘導や、CD4+T細胞自ら直接的にがん細胞を攻撃する細胞障害機能を発揮する能力を発揮することが知られています。特に、炎症性かつ細胞傷害性を持つ1 型CD4+T細胞は、がんに対する免疫で重要な役割を果たします。こうした背景を踏まえ、iPS細胞由来CD4+T細胞の抗腫瘍機能を解明することで、より持続的かつ高い治療効果を発揮するがん免疫療法の実現が期待されます。
1)iPS細胞から作製したCD4⁺T細胞はヘルパー機能を持つ
本研究では、人工胸腺オルガノイド(ATO)との共培養により、ヒトiPS細胞からCD4⁺T細胞を分化誘導し(iCD4+T細胞)、遺伝子発現と機能特性を解析しました。
CD4+T細胞は、CD40Lの発現やIL-21およびIL-2などのサイトカイン分泌を介してヘルパー機能を発揮することが知られています。研究グループは、CD3刺激抗体(OKT3)によりiCD4+およびiCD8+T細胞(iPS細胞由来CD8+T細胞)を活性化したところ、iCD4+T細胞が末梢血中から採取した生体組織由来のCD4+T細胞と同程度にCD40Lを発現することを確認しました(図1A)。また、iCD4⁺T細胞のエフェクター注10)機能を評価するため、PMA/イオノマイシン刺激を与え、活性化を誘導させた結果、iCD4+T細胞はiCD8+T細胞と比較して高いIL-2産生能を示し、IL-21を特異的に発現していました(図1B)。
さらに、iCD4+T細胞のヘルパー機能を検証するため、CD4+T細胞とCD8+T細胞を1:1で共培養したところ、iCD4+T細胞がCD8+T細胞の増殖を促進することが明らかとなりました(図1C)。
以上の結果より、iCD4+T細胞がヘルパーT細胞としての基本的な特性と機能を持つことを確認しました。
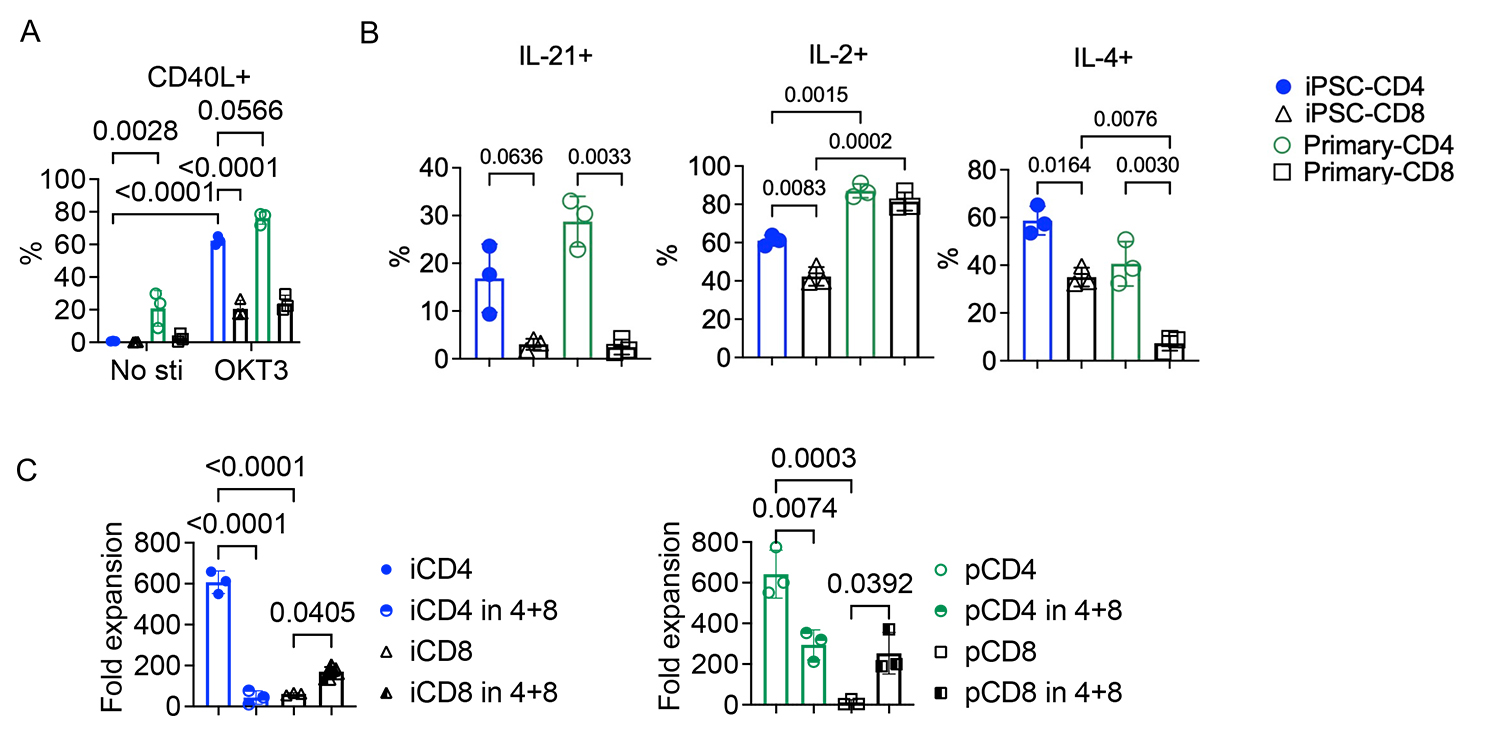
図1. iCD4+T細胞のヘルパー表現型および機能
A:iPSC-T細胞およ健常人由来T細胞を未刺激または固相化抗CD3抗体(OKT3)で24時間刺激し、フローサイトメトリーによりCD40Lの発現を解析した。
B:PMA/イオノマイシンによる4時間刺激後の、ヘルパー関連サイトカイン産生細胞の割合。
C:iPS細胞(i)および組織(p)由来の各T細胞(CD4+またはCD8+)を、単独培養、またはCD4+T細胞とCD8+T細胞を1:1の割合で混合培養して8日目の増殖倍率。
2)iCD4+T細胞は、長期間の持続的なCAR依存的細胞傷害活性を示す
次に、研究グループは、がん細胞を攻撃する能力を強化させるキメラ抗原受容体(CAR)遺伝子(CD19-4-1BB-CD3ζ)を導入したiPS細胞由来、組織由来T細胞を作製し、がん細胞株(NALM6:急性リンパ性白血病由来細胞株)との短期間の共培養により、細胞障害活性を評価しました(図2A)。その結果、iPS細胞由来と組織由来のCAR-T細胞のどちらでも、CD8+T細胞はCD4+T細胞よりも高い傷害活性を示しました(図2B)。
さらに、より長期間にわたって、がん細胞を3日おきに連続投与するCAR-T細胞との共培養において、細胞傷害活性を評価しました。その結果、初期段階においてiCD8+T細胞が高い活性を示す一方で、長期的には活性が低下しました。それに対して、iCD4+T細胞は、長期にわたる持続的な活性を示すことが明らかになりました(図2C-D)。
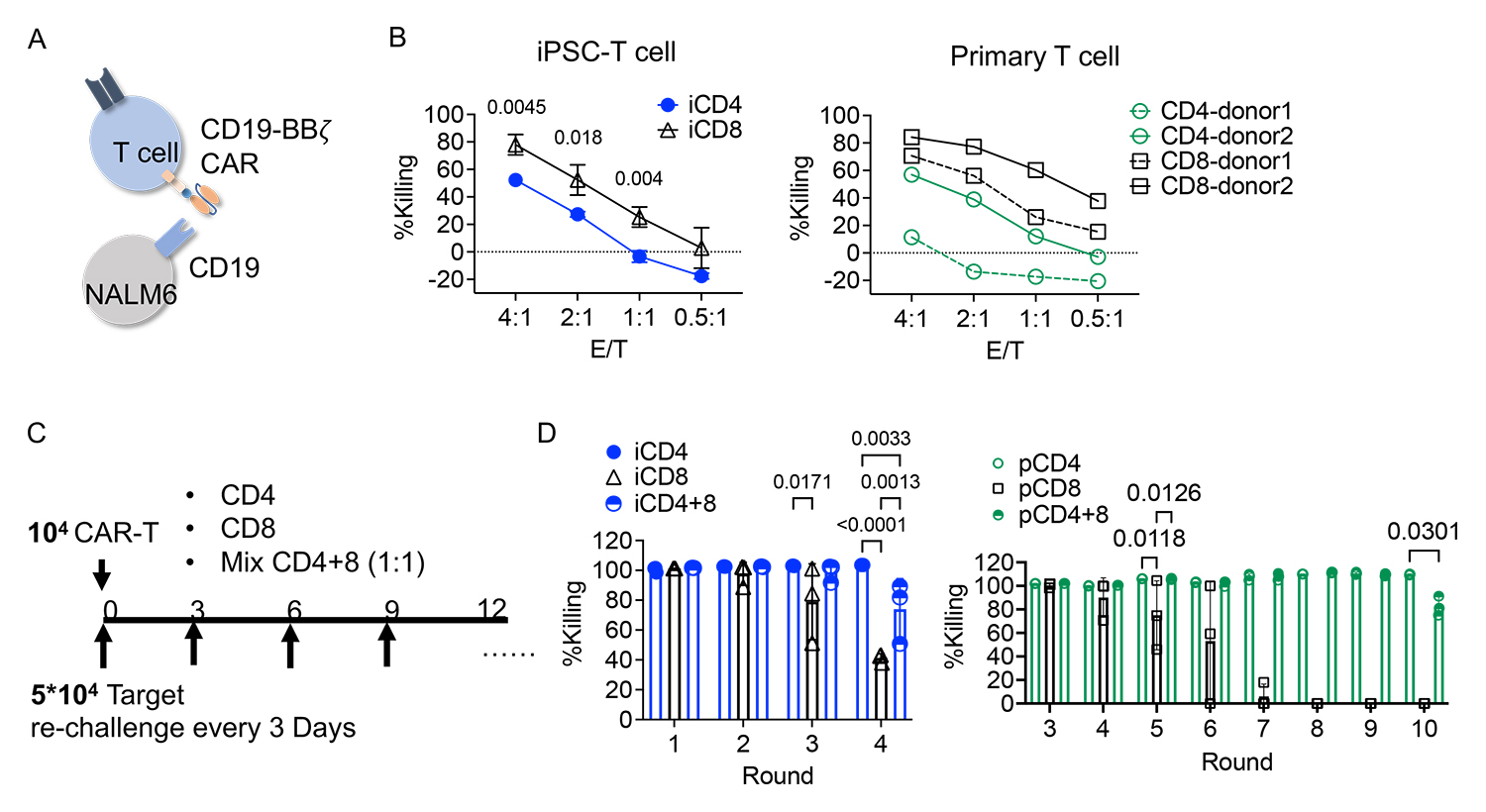
図2. iCD4+T細胞のCAR依存的な細胞障害活性
A:T細胞によるCAR(CD19-4-1BB-CD3ζ)依存的ながん細胞株(NALM6細胞)に対する細胞傷害の模式図。
B:NALM6細胞とiPS細胞(iPSC)由来または組織(Primary)由来のCAR-CD4+/CD8+T細胞とを各比率(T細胞:NALM6細胞=4:1、2:1、1:1、0.5:1)で3日間共培養した条件下でのNALM6細胞に対するCAR-CD4+/CD8+T細胞の殺傷効率。
C:3日間おきにNALM6細胞を追加する長期連続共培養実験の模式図。
D:Cの条件における、がん細胞株に対する各CAR-T細胞(iPS細胞/組織由来のCD4+/CD8+T細胞)による殺傷効率の3日おきの推移。CD4+およびCD8+T細胞を同時にがん細胞株と共培養した場合も、CD4+T細胞とがん細胞株の共培養による殺傷能力を上回る効果はみられなかった。
3)iCD4+T細胞は高い増殖能およびサイトカイン産生能を示す
T細胞の増殖とサイトカインを産生する能力は、がんを攻撃する能力と密接に関連しています。そこで、がん細胞に対する免疫応答過程におけるCAR-iCD4+/iCD8+T細胞数の経時的な変化を評価しました。その結果、CAR-iCD8+T細胞は、がん細胞を攻撃する細胞傷害過程が進行するのに伴って、細胞数が減少するのに対し、CAR-iCD4+T細胞では細胞数の顕著な増加が認められました(図3A)。さらに、がん細胞との共培養した培養液の上清に含まれるサイトカインの量を測定したところ、iCD4+T細胞はiCD8+T細胞と比較して、各種サイトカイン産生量が高いことが示されました(図3B)。この結果は、組織由来CAR-CD4+/CD8+T細胞においても、同様の傾向が認められました。
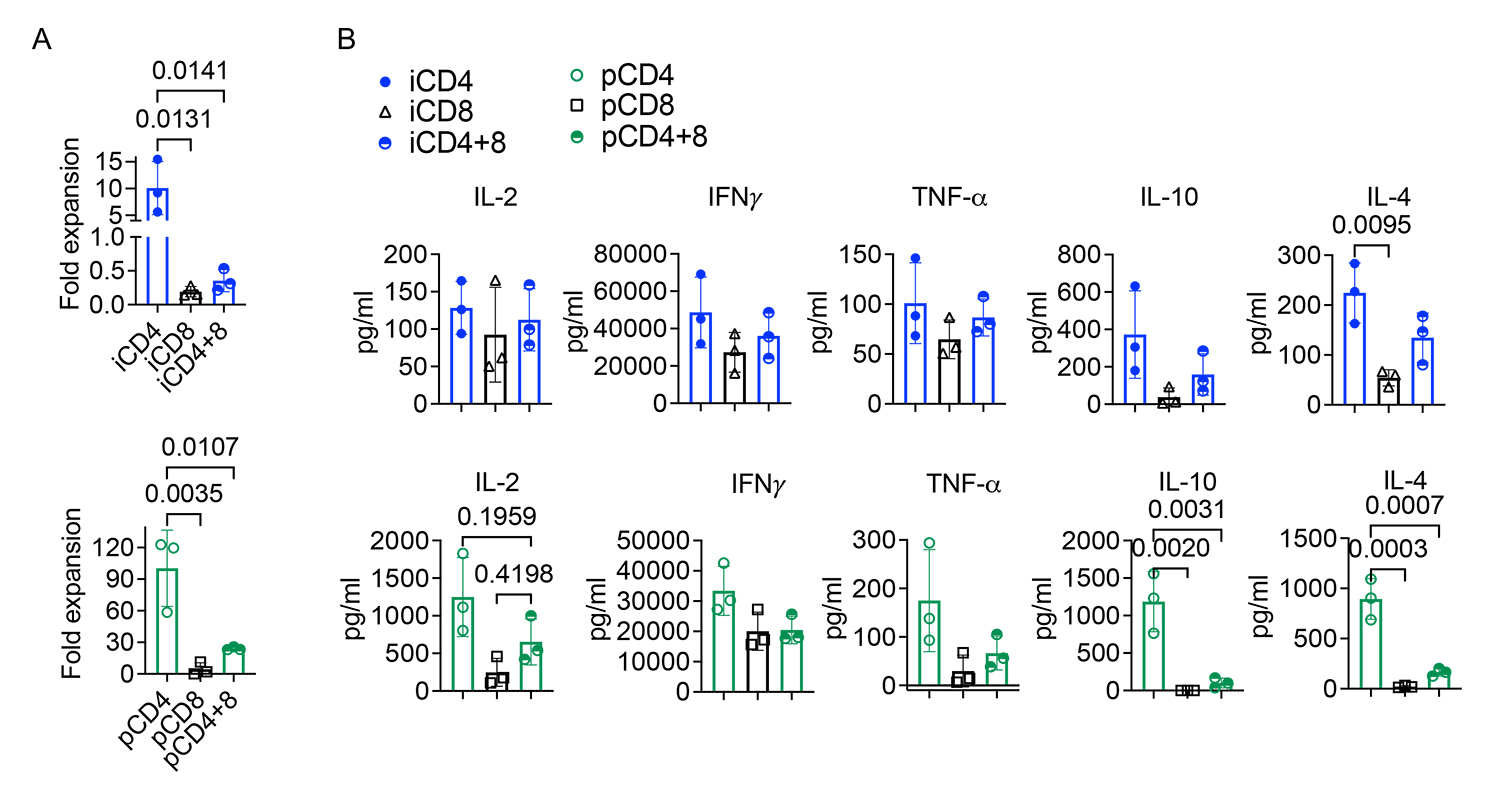
図3. iCD4+T細胞の増殖能およびサイトカイン産生能
A:4回にわたるがん細胞株(NAML6細胞)の連続投与におけるCAR-T細胞の増殖倍率。
B:NALM6細胞とCAR-T細胞の共培養後の培養液上清中のサイトカイン濃度。
4)iCD4+T細胞は、メモリーT細胞に似ており、疲弊しにくい特性を持つ
T細胞のエフェクターおよびメモリー状態への分化バイアスと細胞疲弊は、増殖能および持続性に大きく影響する。そこで、これまで確認した機能の差が分化バイアスや細胞疲弊に起因するものか評価するため、iCD4+/iCD8+T細胞におけるメモリー関連およびエフェクター関連マーカーの発現を解析しました。その結果、iCD4+T細胞ではメモリー関連マーカーの高発現が認められた一方、iCD8+T細胞はよりエフェクター様の表現型を示しました(図4A, B)。
さらに、iCD4+/iCD8+T細胞の疲弊耐性を評価するため、腫瘍細胞と連続共培養後に疲弊関連マーカー発現を測定したところ、iCD8+T細胞では繰り返し抗原刺激に伴い疲弊関連マーカーの発現上昇が認められたのに対し、多くのiCD4+T細胞は依然として未疲弊の表現型を維持していました。また、組織由来CD4+/CD8+T細胞においても、同様の傾向が認められました(図4C)。
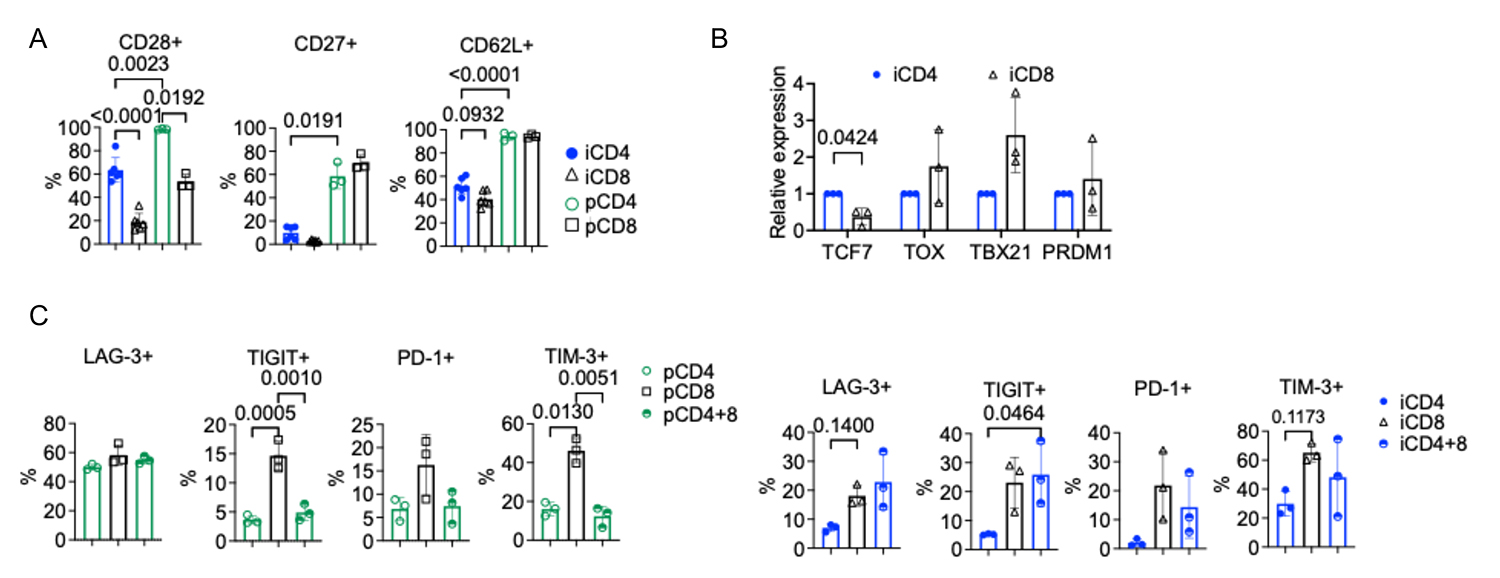
図4. iCD4+T細胞はメモリー関連マーカーを発現し、疲弊しにくい。
A:CD4+/CD8+T細胞においてCD28、CD27、CD62Lを発現する細胞の割合。
B:定量PCRにより評価した、iPS細胞由来CD4+およびCD8+T細胞におけるメモリー関連転写因子TCF7および疲弊関連転写因子TOX、TBX21、PRDM1の相対的mRNA発現量。
C:NALM6細胞を4回目にわたって連続投与する共培養におけるCAR-T細胞の疲弊マーカー(LAG-3、TIGIT、PD-1、TIM-3)の発現。
本研究は、iPS細胞由来CD4+T細胞がヘルパー機能と細胞傷害機能の双方を兼ね備え、組織由来CD4+T細胞と同様の機能を示すことを明らかにしました。iCD4+T細胞は、量産が可能であり、治療が必要なときにすぐに提供が可能なオフ・ザ・シェルフ型のCAR-T免疫療法を実現するための有望な細胞ソースです。今回、iCD4+T細胞の詳細な解析により、免疫応答の持続性や機能面での従来のiCAR-T療法の課題を克服する可能性が示唆されました。本研究では、ヒトiPS細胞と組織由来のT細胞を比較することで、同様の結果が得られたことから、T細胞の分化運命や持続性を規定する発生学的シグナルの解明に役立つことも同時に示しています。今後、マウス細胞との共培養を必要としない分化誘導などの開発などを進めることで、次世代免疫療法の合理的設計に向けた新たな展開を切り拓くことが期待されます。
- 論文名
Adaptive-like CAR-iPSC-CD4+ T cells outperform CD8+ counterparts in sustained ALL control - ジャーナル名
Inflammation and Regeneration - 著者
Qingyi Guo1, Chaoqi Zhang1,3, Bo Wang1, Shoichi Iriguchi1, Akihiro Ishikawa1, Atsutaka Minagawa1, Tomoko Ishii1, Yohei Kawai1, Shin Kaneko1,2,3,*
*:責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- シノビ・セラピューティクス株式会社
- 筑波大学トランスボーダー医学研究センター
本研究は、下記機関より支援を受けて実施されました。
- 日本学術振興会(JSPS)科学研究費助成事業(22H00586)
- 科学技術振興機構(JST)次世代研究者挑戦的研究プログラム(JPMJSP2110)
- シノビ・セラピューティクス株式会社
- iPS細胞研究基金
注1)人工胸腺オルガノイド(Artificial Thymic Organoid:ATO)
特定の分化状態の誘導や維持を補助するマウスのフィーダー細胞に、胸腺上皮細胞でT細胞分化に関わる遺伝子を導入し、3次元培養することで、胸腺の環境を模倣したオルガノイド。幹細胞からT細胞への分化および成熟過程を体外で再現するための細胞培養系。
注2)ヘルパー機能
CD4+T細胞が樹状細胞などからの抗原提示を受けて、サイトカインなどの分泌を介して、他の免疫細胞の免疫反応を制御する機能。
注3)細胞障害(キラー)機能
CD8+T細胞やNK細胞などの免疫細胞が、ウイルス感染細胞やがん細胞を特異的に認識し、直接的に殺傷・排除する機能。
注4)CAR-T療法
キメラ抗原受容体(Chimeric Antigen Receptor:CAR)を遺伝子導入したT細胞で、特定の抗原を認識してがん細胞などを攻撃するよう人工的に改変された免疫細胞療法。
注5)疲弊
慢性的な抗原刺激などによりT細胞の機能が低下した状態を指し、増殖能やサイトカイン産生能、細胞傷害活性が減弱する現象。
注6)サイトカイン
細胞間の情報伝達を担う低分子タンパク質であり、細胞の増殖、分化、活性化などを調節する情報(シグナル)を細胞内へと伝える(シグナル伝達)分子。特に免疫細胞が分泌するサイトカインとして、IL-2やIL-21など、さまざまなインターロイキン(Interleukin:IL)が存在する。
注7)免疫抑制
免疫応答が低下または制御されている状態を指し、腫瘍微小環境や制御性T細胞などにより免疫機能が抑えられる現象である。
注8)抗原提示細胞
抗原を取り込み、分解し、その断片を主要組織適合遺伝子複合体(MHC)上に提示してT細胞を活性化する細胞であり、樹状細胞、マクロファージ、B細胞などが含まれる。
注9)エピトープ拡大
免疫応答の進行に伴い、最初に認識された抗原部位(エピトープ)だけでなく、異なる部位に対しても反応が広がる現象である。
注10)エフェクター
特異的な抗原刺激を受けていないナイーブT細胞から、抗原刺激後に活性化し、免疫応答を担う機能を備えたT細胞の状態。エフェクターT細胞は即時的な免疫応答を担い、そのうちの一部はメモリーT細胞となり、長期間生存して再感染時に迅速に応答する役割をもつ。























