
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年5月1日
NAT1はクロマチン制御因子の選択的翻訳を介して成体腸管幹細胞の恒常性と分化を支える
ポイント
- 翻訳開始因子eIF4G2(別名NAT1)を失うと、腸管幹細胞の維持と分泌系細胞の成熟が損なわれ、腸上皮は胎児様/再生様状態へ移行した。
- eIF4G2欠損により、クロマチン制御因子の翻訳が選択的に低下し、ヒストンアセチル化低下と腸管幹細胞関連制御領域におけるクロマチン状態の選択的再編成が生じた。
- この変化は炎症や統合的ストレス応答が主因ではなく、翻訳制御とエピゲノム制御の連携が成体組織アイデンティティを支えることを示した。
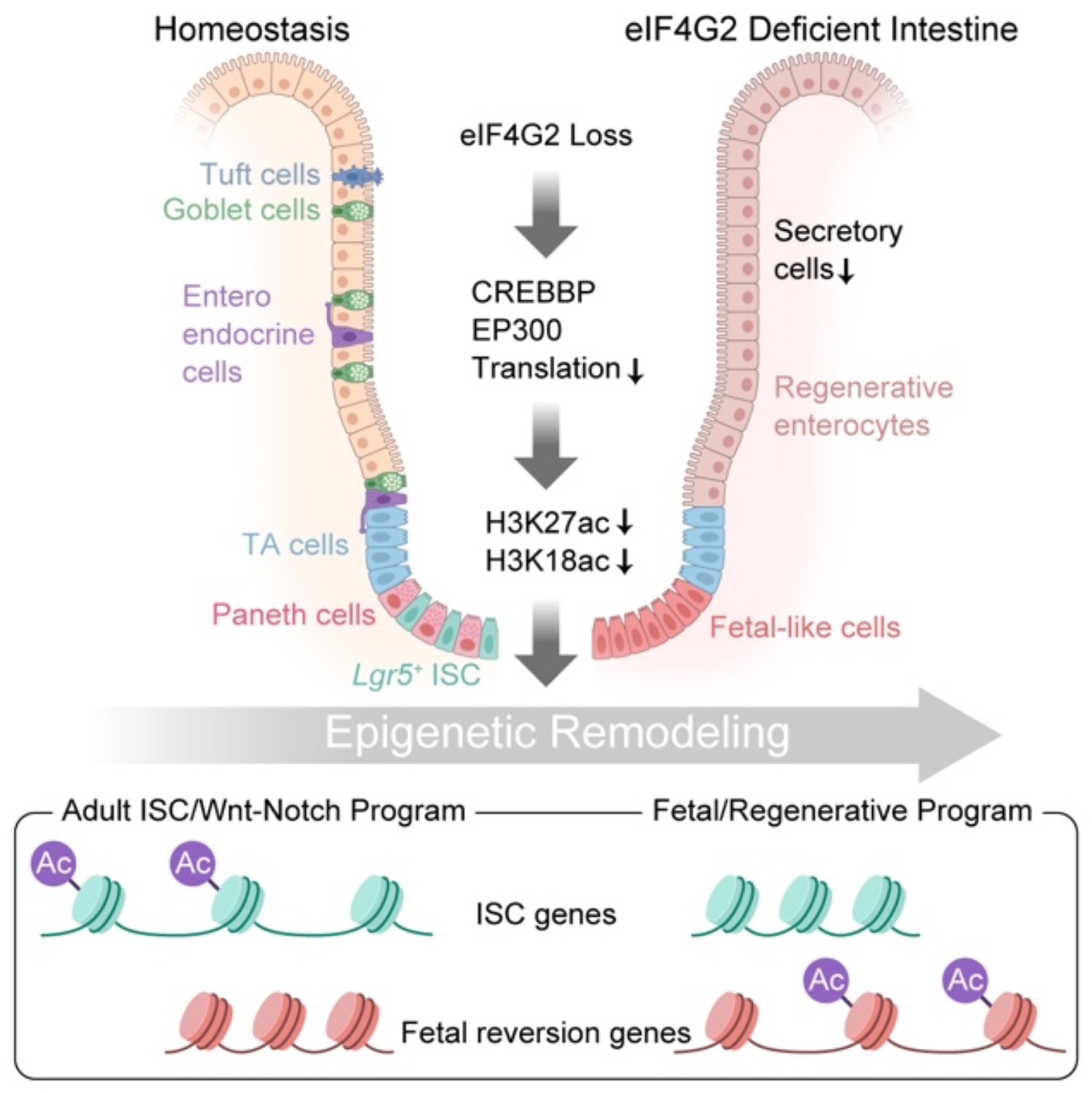
図1. 本研究の概要
國富晴子研究員(グラッドストーン研究所)、山中伸弥教授(グラッドストーン研究所・京都大学CiRA未来生命科学開拓部門)らは、非古典的翻訳開始因子eIF4G2注1)が成体小腸において腸管幹細胞(Intestinal stem cell, ISC)注2) のアイデンティティ維持と分化制御に重要な役割を果たすことを明らかにしました。
研究グループは、誘導性Eif4g2欠損マウスと小腸オルガノイドを用いて解析を行い、eIF4G2を失うとLgr5陽性腸管幹細胞プログラムおよび分泌系細胞の成熟プログラムが崩れる一方、腸絨毛構造自体は比較的保たれ、上皮全体は胎児様/再生様状態へ移行することを見いだしました。さらに、リボソームプロファイリング注3)、シングルセルマルチオーム解析(single-nucleus multiome解析)注4)、CUT&Tag解析から、この現象の背景にはCREBBP/EP300を含むクロマチン制御因子注5)群の選択的翻訳低下と、それに続くヒストンアセチル化低下および腸管幹細胞関連制御領域のクロマチン状態の選択的再編成があることを示しました。
本研究は、翻訳開始因子が単なる"ハウスキーピング因子"ではなく、特定mRNA群の翻訳を選択的に支えることで、成体組織の細胞状態とアイデンティティを安定化することを示した成果であり、腸上皮恒常性、タンパク翻訳制御とエピゲノム制御をつなぐ新しい視点を提供します。
この研究成果は2026年5月1日に「Cell Stem Cell」で公開されました。
小腸上皮は、Lgr5陽性腸管幹細胞によって活発に細胞が入れ替わる、再生能力の高い組織です。この恒常性維持には、幹細胞の自己複製と各細胞系譜への適切な分化が精密に制御される必要があります。一方、腸上皮が障害を受けると、一時的に胎児様の再生プログラムが誘導されることが知られており、その過程にはYAP/TAZ-TEAD経路が関与します。
eIF4G2(別名NAT1)は、非古典的な翻訳開始因子として知られ、構造の複雑な5′UTR(Untranslated region)やuORF(Upstream Open Reading Frame)をもつ一部mRNAの翻訳に関与することが示唆されてきました。しかし、全身ノックアウトが胚性致死となるため、成体組織の恒常性維持における生理的役割は十分に分かっていませんでした。そこで本研究では、成体期にeIF4G2を欠損させる誘導型モデルを作製し、成体腸上皮でeIF4G2が果たす役割を解析しました。
1)eIF4G2欠損は成体腸上皮を胎児様/再生様状態へ移行させる
誘導型Eif4g2欠損マウスおよび小腸オルガノイドの解析から、eIF4G2を失うとLgr5陽性腸管幹細胞の維持と分泌系細胞の成熟が損なわれる一方で、腸絨毛構造自体は比較的保たれることが分かりました。腸上皮特異的Eif4g2欠損モデルでは、欠損誘導から3か月経過後にも、腸管幹細胞およびパネート細胞(Paneth)の減少と胎児様/再生様状態が持続していました。これは、eIF4G2欠損で見られる状態変化が、急性障害後の一過性再生応答ではなく、長期に安定化した代替的上皮状態であることを示します。
RNAシーケンス解析およびシングルセルマルチオーム解析(single-nucleus multiome解析、RNAおよびATAC)により、eIF4G2欠損上皮では通常の腸管幹細胞プログラムが弱まり、代わって胎児様/再生様シグネチャーおよびYAP標的遺伝子群が上昇していました。これらの結果は、eIF4G2欠損によって成体腸上皮が本来の恒常性維持状態から離れ、再生様の代替的状態へ移行することを示しています。
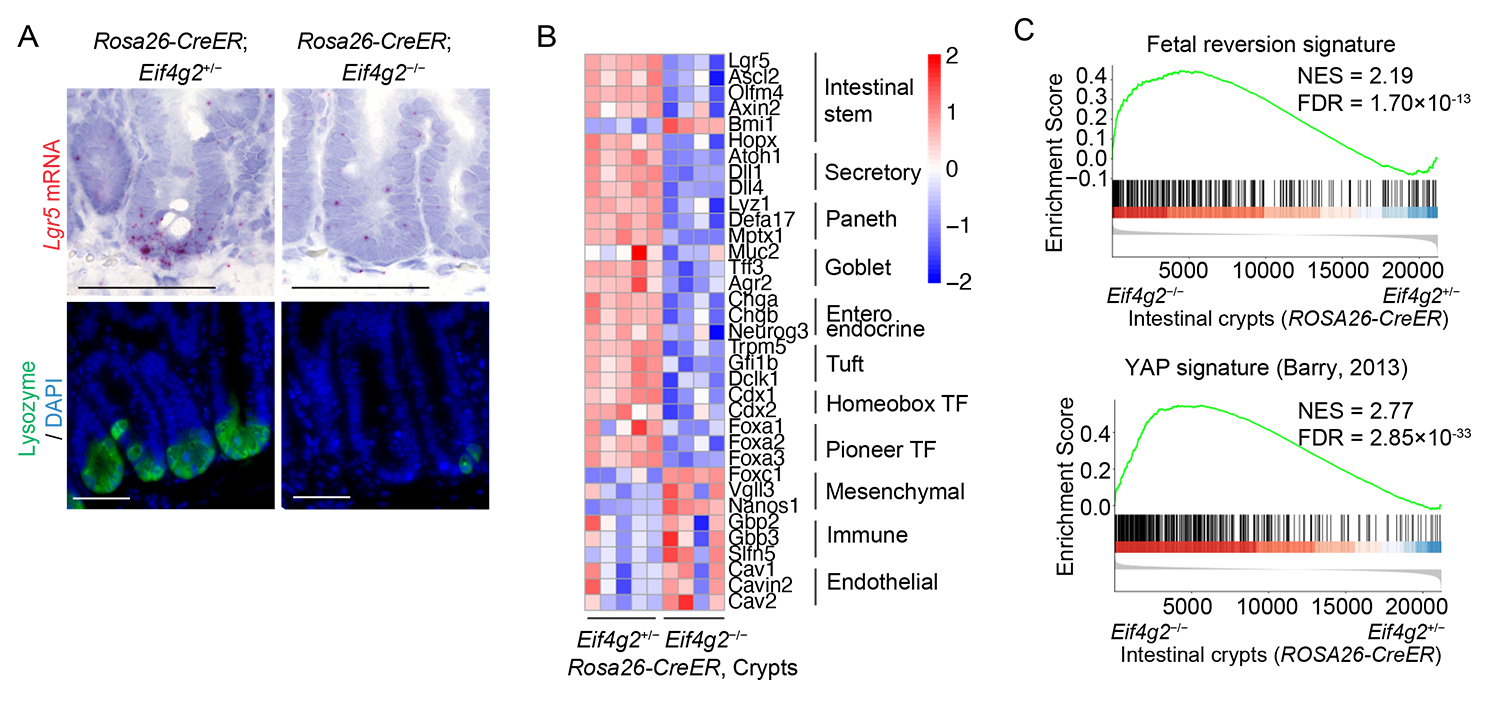
図2. eIF4G2欠損小腸における表現型
A:eIF4G2欠損上皮ではLgr5陽性腸管幹細胞およびライソゾーム陽性パネート細胞が減少する。
B:ヒートマップによる遺伝子発現解析。eIF4G2欠損腸上皮細胞では腸管幹細胞および分泌細胞のマーカー遺伝子発現が低下する。
C:遺伝子セットエンリッチメント解析結果。eIF4G2欠損腸上皮細胞では胎児様シグネチャおよびYAP標的遺伝子群が上昇する。
2)eIF4G2欠損は、クロマチン制御因子の翻訳低下とクロマチン再編成を起こす
小腸オルガノイドの解析では、eIF4G2欠損時にも細胞全体のタンパク質合成量は低下していませんでした。一方、リボソームプロファイリングではCREBBPやEP300を含むクロマチン制御因子群で翻訳効率が選択的に低下していました。これに対応して、CREBBP/EP300タンパク質量と、それらの活性を反映するヒストンアセチル化修飾H3K18ac、H3K27acが低下していました。さらにCUT&Tag解析とATAC解析から、こうした分子変化は全ゲノムで一様に起こるのではなく、腸管幹細胞やWnt-Notchシグナルに関連する制御領域ではクロマチンアクセシビリティが低下し、胎児様/再生様・YAP/TAZ-TEAD関連領域で相対的に上昇することが分かりました。加えて、CREBBP/EP300阻害剤A-485は、eIF4G2欠損と同様の形態変化や遺伝子発現変化を再現し、この経路の関与を支持しました。
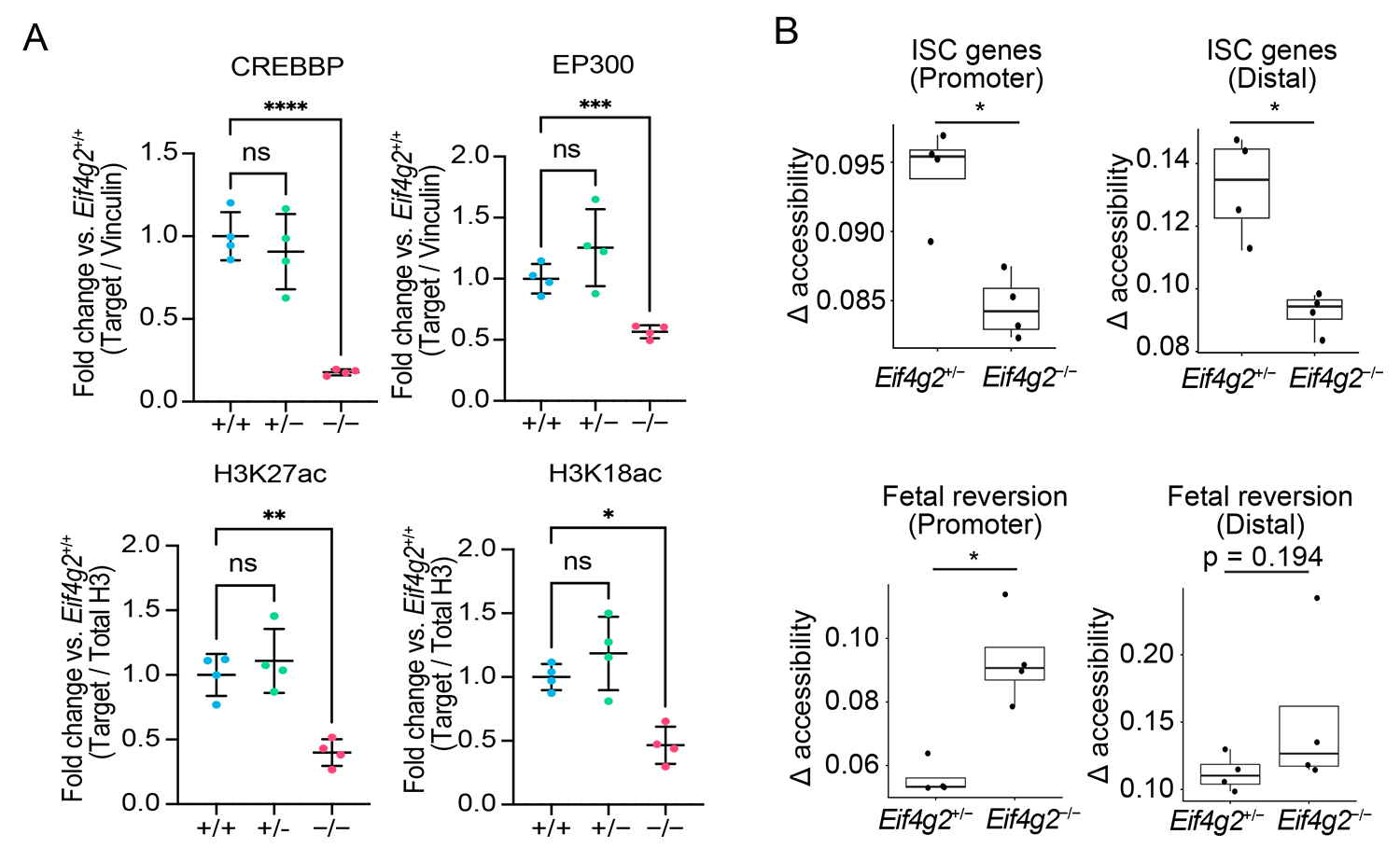
図3. eIF4G2欠損によるタンパク翻訳とエピゲノムの変化
A:eIF4G2欠損によりCREBBPとEP300のタンパク翻訳効率が低下し、それに伴いH3K27ac・H3K18acも低下する。
B:クロマチンアクセシビリティ(ATAC解析)では腸管幹細胞に関連する制御領域の低下と胎児様シグネチャ関連領域での上昇を認める。
3)eIF4G2による翻訳制御への依存性は、腸上皮の成熟段階によって異なる
胎児腸管スフェロイドでは、eIF4G2欠損によりCREBBP/EP300低下やヒストンアセチル化低下といった成体オルガノイドと共通の生化学的変化が生じたにもかかわらず、長期生存と増殖能は保たれていました。さらに、クロマチン変化の方向性は成体と概ね共通していた一方で、影響を受ける制御領域の機能的な重要性は異なっていました。これらの結果は、eIF4G2による翻訳バッファリングがとりわけ成体腸上皮アイデンティティの維持に重要であり、同じ腸上皮でも発生・成熟段階によってその依存性が異なることを示しています。
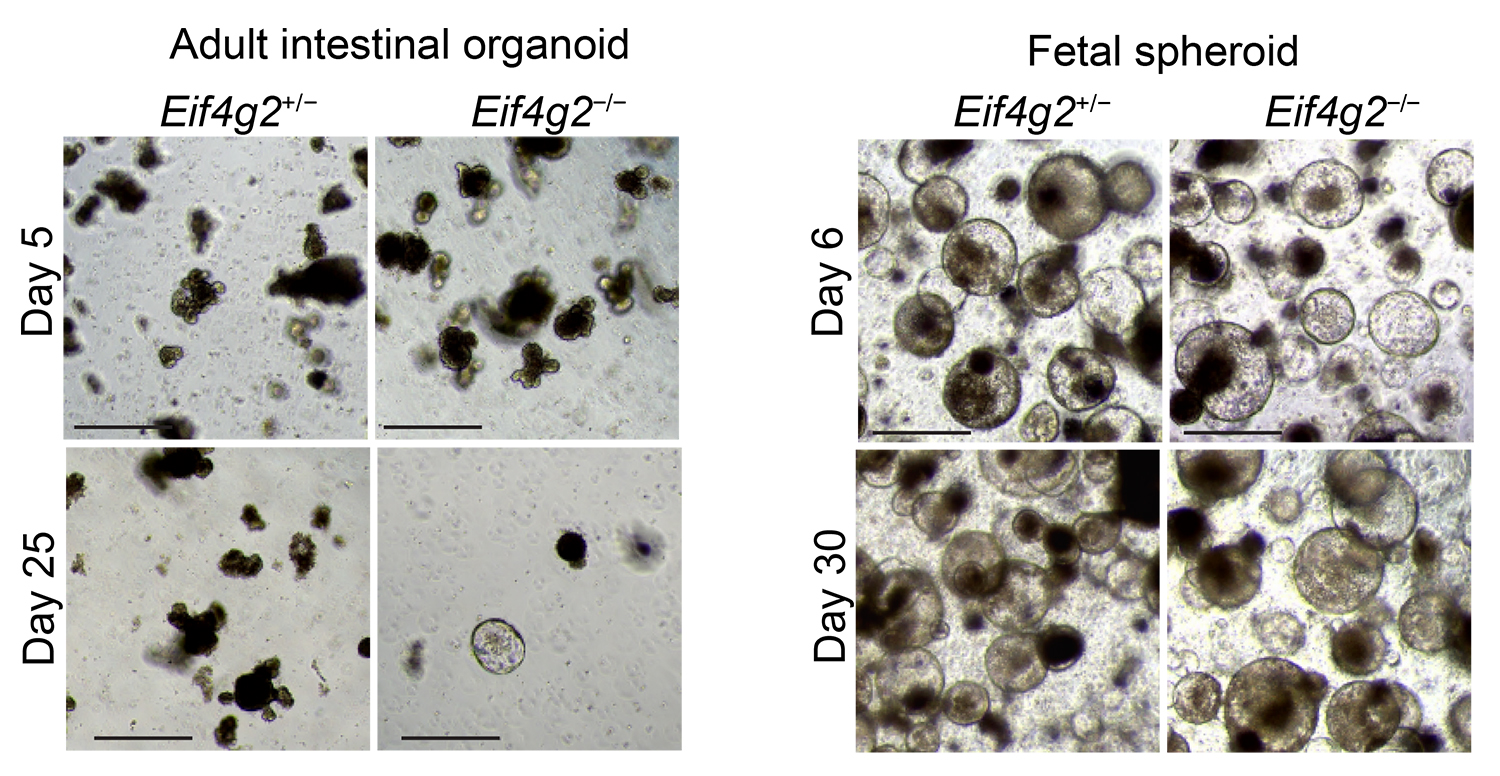
図4. eIF4G2欠損成体腸上皮オルガノイドと胎児腸管スフェロイドの比較
成体腸上皮オルガノイド(左)では細胞の生存・増殖がeIF4G2に依存するのに比べ、胎児腸管
スフェロイド(右)はeIF4G2欠損による影響が少ない。
本研究は、eIF4G2が成体小腸において、CREBBP/EP300をはじめとする用量感受性の高いクロマチン制御因子の翻訳を支える"翻訳バッファー"として機能し、そのことによって成体腸管幹細胞の維持・分化プログラムを安定化していることを示しました。eIF4G2が失われると、腸管幹細胞関連制御領域のクロマチンアクセシビリティが選択的に弱まり、成体上皮は胎児様/再生様状態へ移行します。
この成果は、翻訳開始因子が単なる一律に働く翻訳装置ではなく、特定のmRNA群の翻訳を選択的かつ精密に制御することで、細胞運命や組織恒常性、さらに幹細胞性の維持に深く関与し得ることを示す重要な例です。今後、再生医療や腸上皮障害、慢性的な再生状態の理解に新たな視点を与えるとともに、翻訳制御を介した幹細胞性維持の仕組みや、翻訳制御とエピゲノム制御が連携して成体組織アイデンティティを支える仕組みの解明につながることが期待されます。
今後の課題としては、まず、CREBBP/EP300以外のeIF4G2依存的翻訳標的にも焦点を当て、成体腸上皮の恒常性維持や細胞状態制御に関わる分子ネットワークをより広く理解することが挙げられます。また、eIF4G2の機能や必須性が他の臓器や他の幹細胞系でも共通するのかを明らかにすることで、翻訳バッファリングによる組織アイデンティティ維持という仕組みの一般性を検証していく必要があります。
- 論文名
eIF4G2-Mediated Selective Translation of Chromatin Regulators Safeguards Adult Intestinal Stem Cell Identity and Differentiation - ジャーナル名
Cell Stem Cell - 著者
Haruko Kunitomi1*, Aye Myat Khaine1, Radia Jamee1, Vanessa Arreola1, Mariselle Lancero1, Amba Raychaudhuri1, Samuel Perli1, Yoshiko Sato2, Mio Iwasaki2, Pedro Ruivo3, Kiichiro Tomoda1,2, Mari Mito4, Yuichi Shichino4,5, Shintaro Iwasaki4,6, Shinya Yamanaka1,2*
*:責任著者 - 著者の所属機関
- グラッドストーン心血管疾患研究所、グラッドストーン研究所
- 京都大学iPS細胞研究所(CiRA)
- カリフォルニア大学デービス校
- 理化学研究所
- 筑波大学医学医療系
- 東京大学大学院新領域創成科学研究科
本研究は、下記機関より支援を受けて実施されました。
-
日本医療研究開発機構(AMED)
- 再生医療実現拠点ネットワークプログラム
「再生医療用iPS細胞ストック開発拠点(JP21bm0104001)」- 革新的先端研究開発支援事業
「神経変性疾患におけるアグリゲーションと翻訳の陰陽(JP20gm1410001)」
「非膜性オルガネラによるRNA時空間制御を介したDNA損傷応答(JP23gm6910005)」 - 日本学術振興会(JSPS)科学研究費
- iPS細胞研究基金
- 理化学研究所
- 京都大学 On-site Laboratory
- 三木谷浩史 氏
- Marc Benioff 氏
- L. K. Whittier Foundation
- Roddenberry Foundation
- Gladstone Institutes
注1)eIF4G2(NAT1/p97/DAP5)
標準的な翻訳開始因子eIF4G1のアイソフォーム。典型的な「キャップ依存的翻訳」を促進するeIF4G1とは異なり、ストレス条件下や特定のmRNAに対して選択的に翻訳を誘導する役割を持つ。
注2)腸管幹細胞(Intestinal stem cell, ISC)
小腸の隠窩(クリプト)底部に存在する、腸上皮の全ての細胞を供給する幹細胞。Lgr5陽性細胞は通常時に活発に分裂している。
注3)リボソームプロファイリング
細胞内でリボソームが結合している mRNA 断片(リボソームフットプリント)を網羅的にシーケンシングする手法。転写量(RNA-seq)ではなく、実際にどれだけタンパク質が作られようとしているか(翻訳効率)を定量できる。
注4)シングルセルマルチオーム解析(single-nucleus multiome解析)
同一の単一核から、遺伝子発現(RNA-seq)とクロマチンアクセシビリティ(ATAC-seq)の情報を同時に取得する技術。細胞ごとの不均一性を考慮しながら、エピジェネティックな状態と転写の関係を解析できる。
注5)クロマチン制御因子
ヒストン修飾酵素やクロマチン再構成複合体など、DNAのパッケージング状態を変化させて遺伝子発現を調節するタンパク質群。























