
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年5月2日
膵臓のストレス応答因子「CXCL13」を特定 ―慢性炎症とがん進行を制御する新メカニズムを解明―
ポイント
- 膵臓へのストレスや加齢によりタンパク質「CXCL13」が誘導されることを発見。
- CXCL13が免疫細胞を集め、慢性炎症を引き起こすことで、膵がんの発症や進行を促進する仕組みを特定。
- 今回見出したストレス応答経路を制御することで、膵がんや慢性膵炎の治療法開発が期待される。
吉田昌弘 研究員(CiRA未来生命科学開拓部門、京都大学医学研究科)、川口義弥 教授(CiRA未来生命科学開拓部門)らは、膵臓においてストレスや加齢によって誘導されるタンパク質「CXCL13注1)」が、組織の慢性炎症を引き起こし、膵がん(膵管腺がん)の進行を加速させるメカニズムを解明しました。
膵がん注2)は非常に予後が悪い難治性がんの一つであり、慢性的な炎症注3)がその発症や進行に深く関わっていることが知られています。しかし、加齢や外的ストレスがどのようにして膵臓内に炎症環境を作り出し、がん化を促すのか、その具体的な分子メカニズムは十分に解明されていませんでした。
研究グループは、膵腺房細胞がミトコンドリアや代謝のストレスに応答してケモカイン「CXCL13」を放出することを発見しました。この反応は、ストレスを受けた細胞のアポトーシス抵抗性とPD-L1の一時的な発現により免疫系から排除されるのを防ぎつつ、周囲の健康な細胞のHippo-YAP経路注4)を活性化して増殖を促し組織を修復する「保護的な役割」を果たします。しかし、加齢やがん変異によってこのシグナルが慢性化すると、持続的な炎症やがんの悪性化を引き起こす「共通のストレス応答軸(CXCL13-YAP-PD-L1軸)」として機能することが明らかになりました。マウスモデルおよびヒト臨床検体を用いた解析の結果、このCXCL13がB細胞を中心とした免疫細胞を異常に集積させ、炎症性微小環境注5)を形成することで、正常な膵組織の維持(恒常性注6))が困難となり、がんの悪性化を強力に後押しすることを突き止めました。さらに、このストレス応答経路を制御することで、膵がんの進行を抑制できる可能性も示唆されました。
本研究の結果は、加齢やストレスが膵臓に及ぼす悪影響を分子レベルで統合的に理解する一助となるものです。この知見は、膵がんや慢性膵炎といった難治性疾患に対する、これまでにない予防法や治療戦略の開発につながるプラットフォームとなることが期待されます。
この研究成果は2026年5月2日に「Science Advances」で公開されました。
膵管腺がん(PDAC)は、現代医学において最も予後が悪いがんの一つであり、早期発見が困難なだけでなく、既存の治療法に対する抵抗性も極めて高いことが大きな課題となっています。このがんの発症や進行には、喫煙や糖尿病といった生活習慣に加え、「加齢」と「慢性的な炎症」が重要なリスク因子であることが長年の研究から示唆されてきました。
特に、消化酵素を分泌する膵臓の外分泌系組織は、急性膵炎などの強いストレスや加齢に伴う組織の変化が生じると、内部の微小環境が劇的に変化します。この変化により、がん細胞が生存・増殖しやすい「炎症性の土壌」が形成されると考えられてきました。しかし、こうした多種多様なストレスが、どのような分子メカニズムを介して膵臓の恒常性を破壊し、持続的な炎症やがん化を引き起こすのか、その具体的なプロセスは十分に解明されていませんでした。
そこで研究グループは、細胞間の情報伝達を担うタンパク質である「ケモカイン注7)」に着目しました。なかでも、特定の免疫細胞を誘導する働きを持つ「CXCL13」が、膵臓のストレス応答において中心的な役割を果たしているのではないかという仮説を立て、検証を行いました。本研究は、老化と炎症、そしてがんという、一見異なる現象を一つの「共通したストレス応答経路」として統合的に理解し、難治性疾患の根源に迫ることを目指しました。
1)ストレスや加齢によるCXCL13の誘導
研究グループはまず、「ストレスを受けた膵臓の細胞で起きていること」を調べるため、遺伝子欠損マウスやストレスを引き起こす薬剤を投与したマウス、老化マウスを使用しました。
膵臓の維持に不可欠な遺伝子(Pdx1注8))を特定の時期に欠損させたマウス(Pdx1 cKO)を作製し、細胞に人為的なストレスを与えました。Pdx1を欠損させた細胞で特異的にCXCL13が強く発現していることを確認しました。(Fig.1)
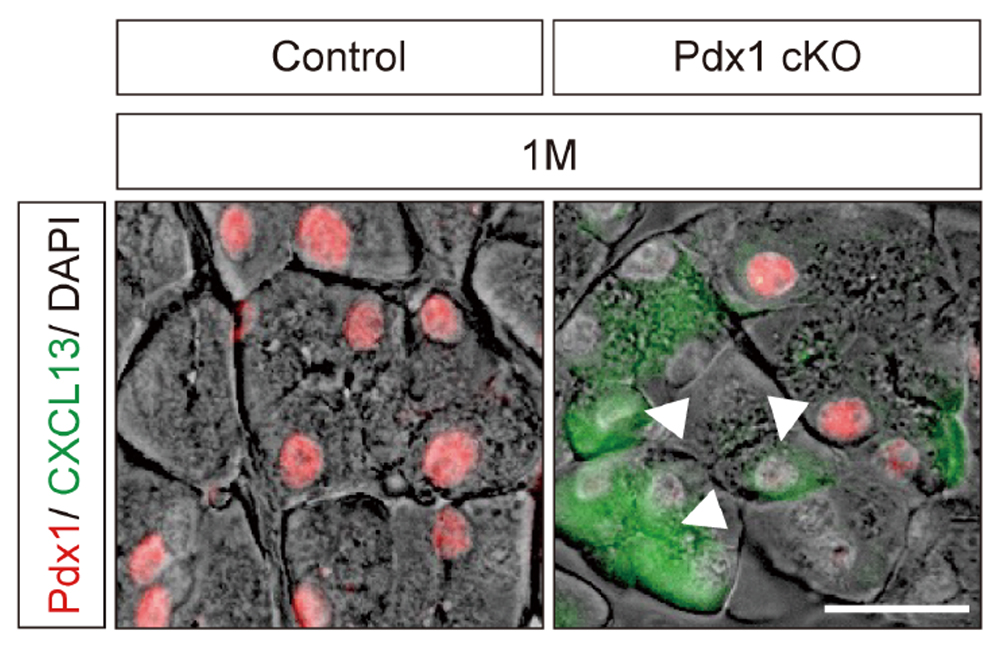
Fig.1 マウス膵臓の細胞を免疫染色した結果
さらに、細胞ストレスを生じさせる薬剤を投与したマウスや生後20ヶ月以上の高齢マウスの膵臓を解析しました。その両者の膵臓でも、若い正常マウスには見られないCXCL13や老化マーカー(p21など)の上昇が確認されました。
以上の結果から、膵臓の細胞は、ストレスや老化に直面すると「生存のための信号」としてCXCL13を出し始めることがわかりました。このCXCL13の放出はミトコンドリアの機能不全や代謝ストレスによってトリガーされていました。若い正常な組織では、この反応は一過性です。CXCL13が周囲の細胞のHippo-YAP経路を介して増殖を促すとともに、自らに対する抗アポトーシス作用に加えてPD-L1を発現することで、組織修復が完了するまでの間、免疫細胞による攻撃を一時的に回避して生き残るという、巧みな自己保護メカニズムが働いていました。
2)CXCL13による免疫細胞の集積と慢性炎症
次に、放出されたCXCL13が与える影響を調べるため、高齢マウスの膵臓の中で細胞の動きを追跡しました。高齢マウスではp21陽性の老化した細胞や、CD45陽性の免疫細胞の集積が見られました。しかし、CXCL13の働きを阻害する「抗CXCL13抗体」をマウスに投与すると老化細胞が減少し、免疫細胞の異常な集積が抑えられました(Fig.2)。また、加齢に伴う膵臓の脂肪化が改善されました。
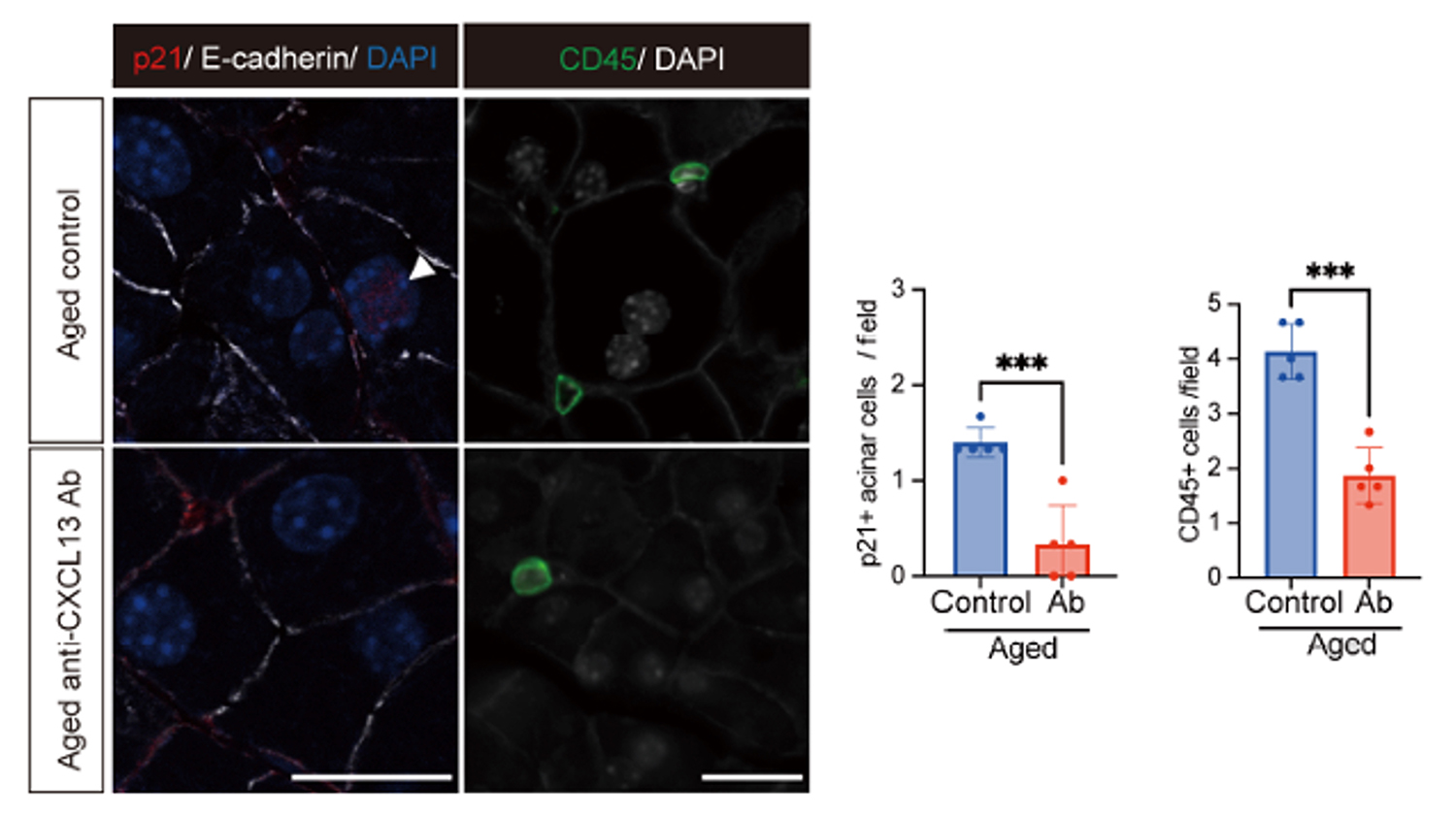
Fig.2 CXCL13の働きを抑制することが免疫細胞に与える影響
以上の結果から、老化細胞自身が放出するCXCL13がきっかけとなり、老化細胞の蓄積と組織の慢性炎症が起こることが示されました。
3)膵がんの進行加速と治療標的としての検証
最後に、「このメカニズムががんにどう関わるか」を検証するため、がんを発症するマウス(EKPマウス)を使用しました。がんモデルマウスにPdx1欠損ストレスを組み合わせ、がんの成長速度を比較しました。
ストレス(Pdx1欠損)があるマウスやストレスを引き起こす薬剤を投与したマウスでは、がんのサイズが劇的に大きく、線維化(がん特有の硬い組織)も進んでいました。(Fig.3)
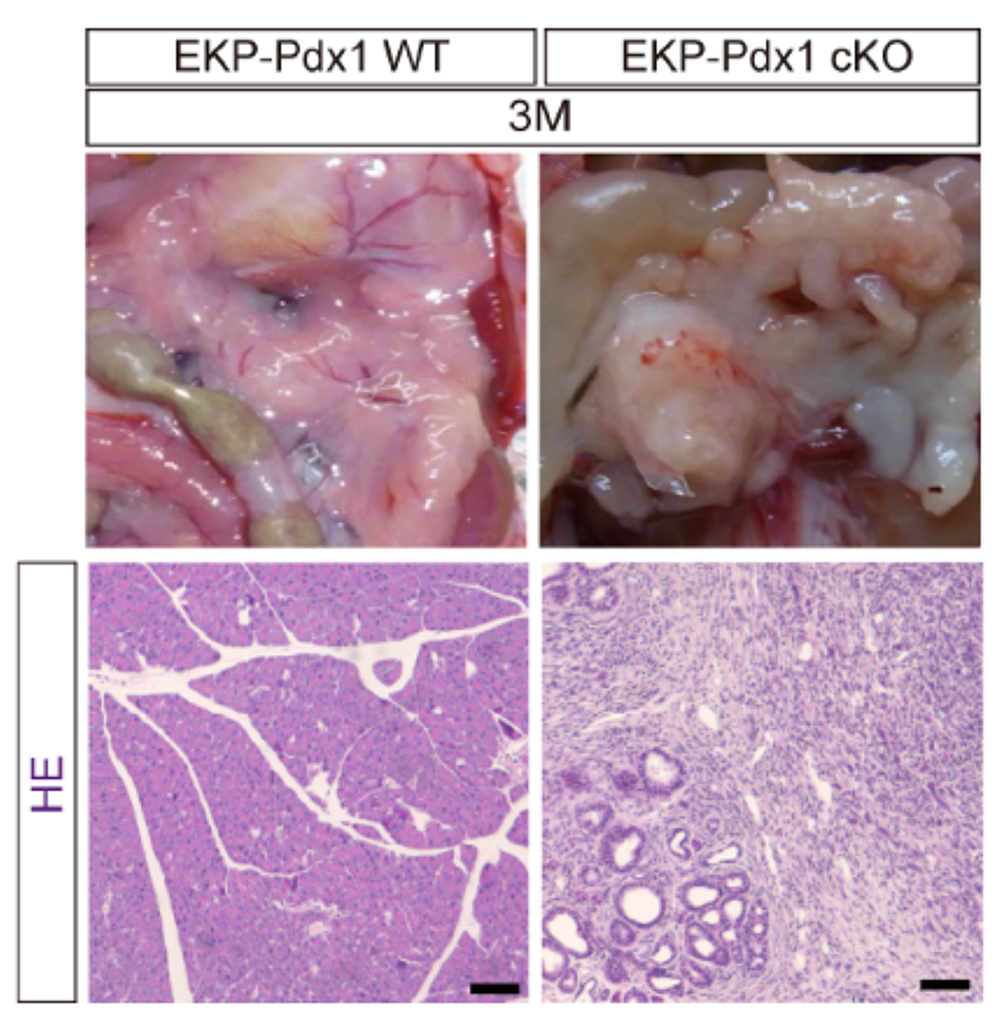
Fig.3 Pdx欠損によるがんの成長促進
その際、ストレスを受けたがん細胞は一過性ではなく持続的にCXCL13を産生しており、この長期的なシグナルはストレスがん細胞を保護するだけでなく、周囲の非がん細胞のYAP活性化を介した増殖刺激に加えて前がん病変に変化させるという予想外の非細胞自律的な形質転換を引き起こしました。そこで、がんが進行し始めたマウスに対し、抗CXCL13抗体や、Hippo-YAP経路阻害剤(super-TDU)を投与すると、がんの進行がほぼ完全にブロックされました。 細胞の増殖が抑えられ、周囲細胞の前がん病変化や組織の線維化も劇的に減少しました。(Fig.4)
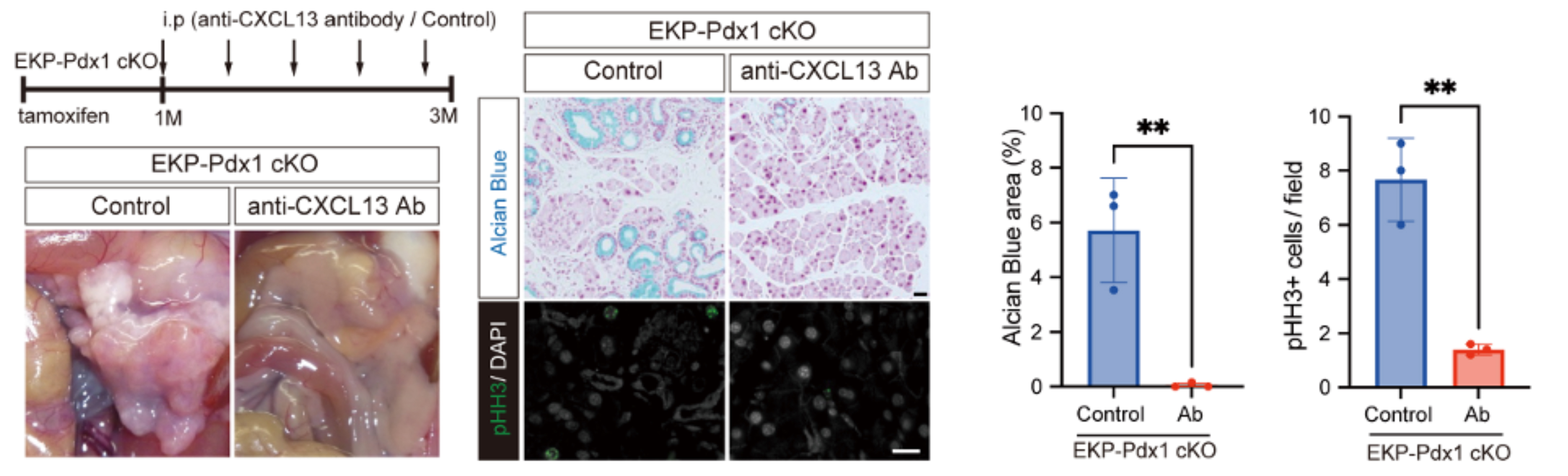
Fig.4 抗CXCL抗体によるがん進行の抑制
以上の結果からCXCL13を阻害することが、膵がんの進行を止めるための極めて有望な治療戦略になることが証明されました。元来、抗がん剤投与や放射線照射が細胞ストレスを引き起こすことを考え合わせると、CXCL13を引き金とした反応が膵がんの治療抵抗性の本質である可能性が高いと考えられます。
本研究では、加齢や外的ストレスにより膵臓で誘導されるケモカインCXCL13が、免疫細胞の異常な集積を介して慢性炎症を引き起こし、膵がんの進行を促進する新たな分子メカニズムを明らかにしました。また、CXCL13や関連するストレス応答経路を制御することで、がんの進行や慢性炎症・線維化を抑制できる可能性も示されました。本成果は、同一のシグナルが短期間であれば修復的に働き、長期間にわたると有害になることを示すことで、組織恒常性・老化・癌という異なる現象を共通のストレス応答機構で理解する新たな概念を提示するとともに、膵がんや慢性膵炎に対する新規治療戦略の開発につながることが期待されます。
- 論文名
Stress-induced CXCL13 regulates pancreatic exocrine homeostasis, age-related chronic inflammation, and cancer progression. A unified stress-response axis in the pancreas - ジャーナル名
Science Advances - 著者
Masahiro Yoshida1,2, Kenichiro Furuyama1,2, Keisuke Sumide3, Masashi Horiguchi1,2, Ahmed I. Abo-Ahmed2,4, Hirofumi Shibata2, Akito Tanaka2, Ahmed M. Rashwan2,5, Toshihiko Masui1,2, Cantas Alev6, Takuya Yamamoto2,6,7, Yasuhiro Yamada8, Shin Kaneko3, Shuh Narumiya9,10, David Tuveson11, Shinji Uemoto12, Etsuro Hatano1, Yoshiya Kawaguchi2* - 著者の所属機関
- 京都大学大学院医学研究科 外科学講座 肝胆膵・移植外科学分野
- 京都大学 iPS細胞研究所(CiRA)未来生命科学開拓部門
- 京都大学 iPS細胞研究所(CiRA)増殖分化機構研究部門
- ベンハ大学 獣医学部 解剖学・発生学講座
- ダマンフール大学 獣医学部 解剖学・発生学講座
- 京都大学 高等研究院 ヒト生物学高等研究拠点(ASHBi)
- 理化学研究所 革新知能統合研究センター(AIP) iPS細胞連携医学的リスク回避チーム
- 東京大学大学院医学系研究科 分子病理学講座
- 京都大学大学院医学研究科 創薬医学講座
- 神戸医療産業都市推進機構
- コールド・スプリング・ハーバー研究所
- 滋賀医科大学
本研究は、下記機関より支援を受けて実施されました。
- 日本学術振興会(JSPS) 科学研究費(18H05384, 24K22142, 25K02715)
注1)CXCL13
免疫細胞を特定の場所へ呼び寄せる「ケモカイン」と呼ばれるタンパク質の一種。本研究では、膵臓がストレスや加齢を受けた際にCXCL13が誘導され、慢性炎症や膵がんの進行を促す中心的な因子であることが示された。
注2)膵がん(膵管腺がん)
膵臓の外分泌組織から発生するがん。進行が早く、治療抵抗性で予後が不良な難治性がんとして知られる。
注3)慢性炎症
長期間にわたって持続する炎症状態。組織の機能低下や、がんの発症・進行を促進する要因となる。
注4)Hippo-YAP経路
細胞の増殖や生存を制御するシグナル伝達経路。がんの発症や進行に関与することが知られている。
注5)炎症性微小環境
組織の局所において、免疫細胞や炎症性分子が集積した状態。がん細胞が生存・増殖しやすい環境を形成する。
注6)恒常性(ホメオスタシス)
外的な変化があっても、組織や体の状態を一定に保とうとする仕組み。
注7)ケモカイン
免疫細胞の移動を制御する情報伝達分子の総称。炎症や免疫応答の調節に重要な役割を果たす。
注8)Pdx1
膵臓の発生や維持に必須な転写因子。Pdx1の機能低下は、膵臓の細胞に強いミトコンドリアストレスを与える。























