
ニュース・イベント
News & Events
ニュース・イベント
News & Events
ニュース
News
2026年5月15日
ナノファイバーによるヒト髄鞘形成モデルの構築と定量化
ー 生体模倣システム(MPS)としての新規ヒト細胞評価系 ー
ポイント
- ヒトiPS細胞由来のオリゴデンドロサイトとナノファイバーを組み合わせ、神経軸索を包み込む「髄鞘形成」の初期過程を試験管内で再現する新モデルを構築しました。
- 髄鞘特異的な分子(Claudin-11)を指標とすることで、これまで困難だったヒト細胞による「髄鞘化」プロセスの定量的な評価手法を確立しました。
- 本評価系は、多発性硬化症などの神経難病の病態解明や創薬研究に加え、老化に伴う脳機能低下の抑制に向けた研究基盤としての活用が期待されます。
森田賢受託研究員(京都大学iPS細胞研究所(CiRA)、理化学研究所(理研)バイオリソース研究センターiPS創薬基盤開発チーム客員研究員、サントリーウエルネス株式会社生命科学研究所研究員(現:サントリーグローバルイノベーションセンター株式会社研究員))、近藤孝之特定拠点講師(CiRA、理研同チーム客員研究員)、井上治久教授(CiRA、理研同チームディレクターおよび革新知能統合研究センターiPS細胞連携医学的リスク回避チーム客員主管研究員)らの共同研究チームは、ヒト人工多能性幹細胞(iPS細胞)注1)から分化誘導したオリゴデンドロサイト注2)という細胞を用いて、この細胞が神経細胞から細長く伸びる軸索注3)を包み込む初期過程を再現するモデルを構築し、その過程を定量的に評価する方法を確立しました。
オリゴデンドロサイトは中枢神経系で軸索を包み込み、髄鞘注4)と呼ばれる構造を形成します。髄鞘は神経信号の効率的な伝達に重要な役割を果たしており、その機能不全は神経疾患、老化に伴う変化などに関与しています。本研究で確立したモデルと評価方法は、オリゴデンドロサイトが関与する疾患の研究や脳の老化の研究、AI解析に資する均質なデータセット取得基盤への応用が期待されます。
本研究では、軸索構造を模倣したナノファイバーと、ヒトiPS細胞からオリゴデンドロサイトを効率よく作製する技術を組み合わせることで、オリゴデンドロサイトが軸索模倣構造を包み込む過程を再現するモデルを構築しました。さらに、髄鞘特異的な接着分子であるClaudin-11注5)の発現を指標として、髄鞘形成の初期過程を定量的に評価する方法を確立しました。この方法を用いることによって、白質を障害する、あるいは髄鞘形成を促進する化合物の評価ができることが明らかになりました。
本研究は、2026年5月14日(米国東部時間)に科学雑誌『Stem Cell Reports』にオンライン掲載されました。
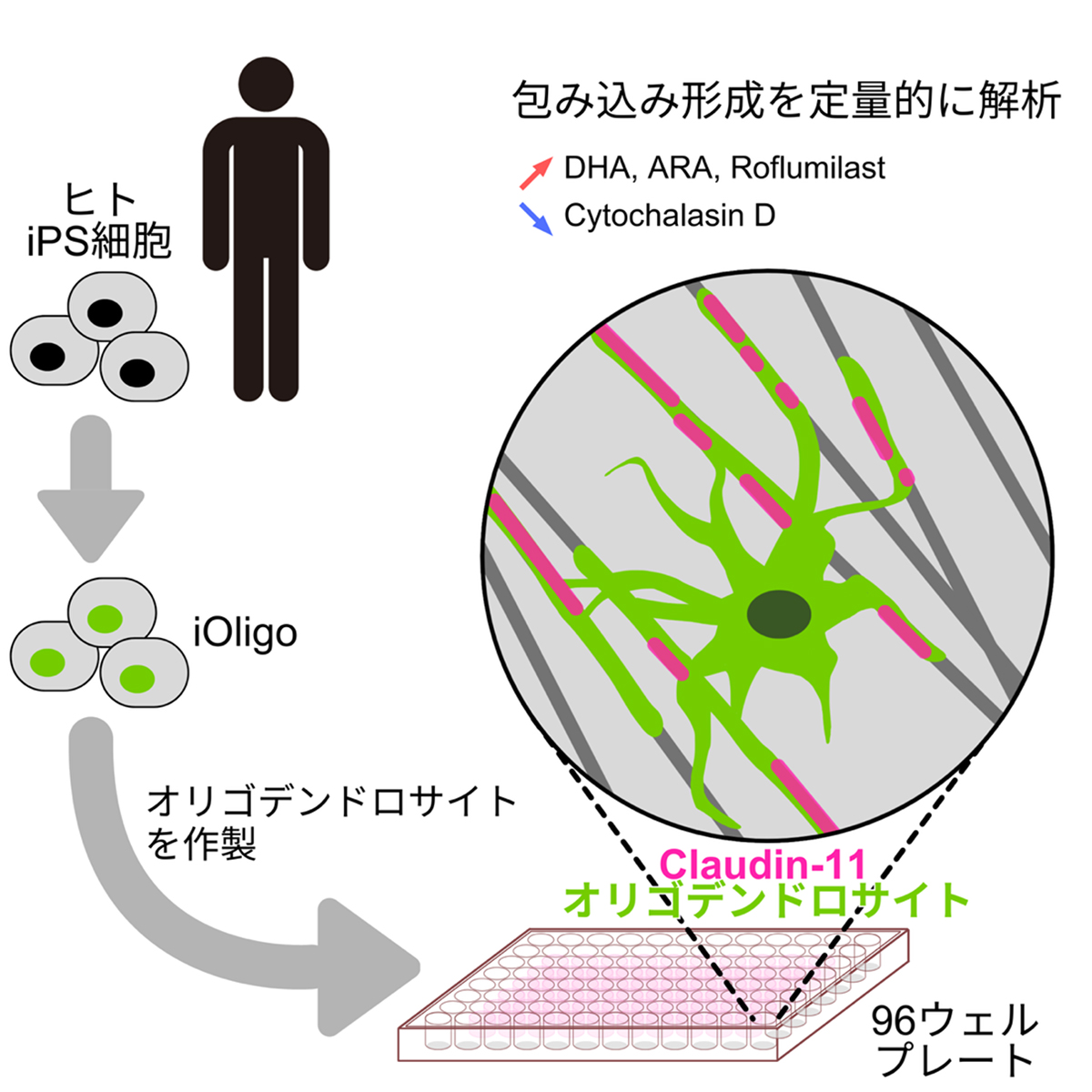
本研究の概要
オリゴデンドロサイトは中枢神経系のグリア細胞注6)の一種であり、神経細胞の軸索を包み込む髄鞘を形成します。髄鞘は電気信号の伝導速度を高める役割を担い、脳機能の維持に重要な役割を果たしています。また中枢神経組織のうち、髄鞘を持つ軸索(有髄神経線維)が多く集まる部位は髄鞘に含まれる脂質によって白く見え、白質と呼ばれます。オリゴデンドロサイトの機能不全は、多発性硬化症注7)などの神経疾患や老化に伴う白質変化とも関連することが知られています。
これまでオリゴデンドロサイトの研究は、主にマウスなどのモデル動物で行われてきました。しかし、ヒトと他の動物では白質構造や遺伝子発現、発達のタイミングなどに大きな違いがあることが報告されています。そのため、ヒトオリゴデンドロサイトを用いた研究モデルの構築がヒトに関する研究では重要とされています。
近年、ヒトiPS細胞から神経細胞やグリア細胞を作製する技術が発展してきましたが、ヒトオリゴデンドロサイトの機能につながる軸索を包み込む過程を定量的に評価できるモデルは限られていました。また、これまでのモデルでは、複数種類の細胞を混合した複雑な共培養系や長期間培養を用いることで生理的環境の再現が試みられてきましたが、解析の再現性や定量性をさらに高める新たな実験系が求められてきました。
共同研究チームはまず、ヒトiPS細胞においてオリゴデンドロサイト分化を制御する転写因子注8)(Sox10、Olig2、Nkx6.2)の発現を誘導することで、短期間でオリゴデンドロサイトへ分化させる方法を確立しました(図1)。この方法により、オリゴデンドロサイトを効率よく得ることが可能となりました。
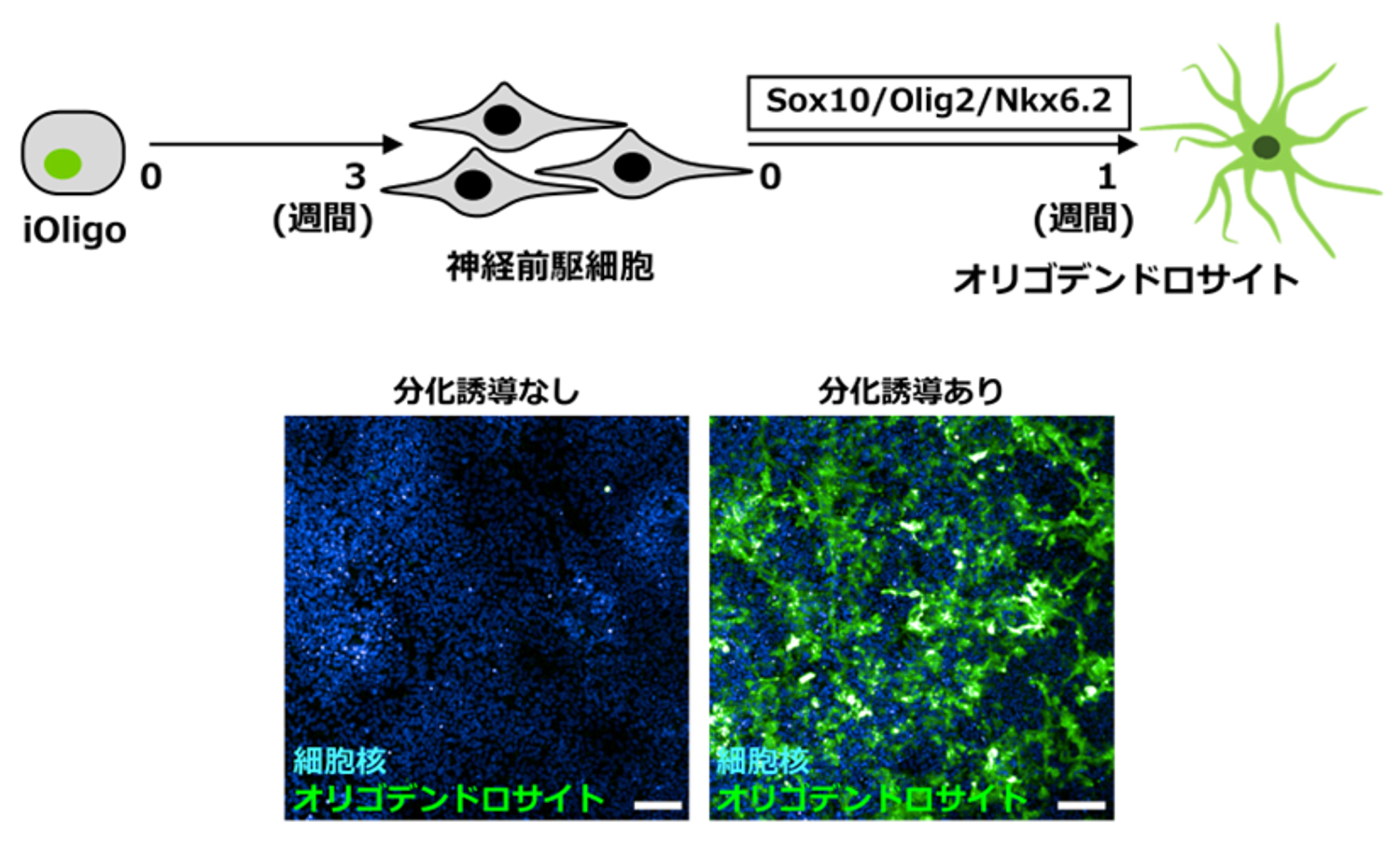
図1 ヒトiPS細胞由来オリゴデンドロサイトの作製
上:培養系の概要。iOligoから作製した神経前駆細胞に対して1週間、転写因子の発現を誘導し、オリゴデンドロサイトを作製した。iOligoとは、転写因子(Sox10、Olig2、Nkx6.2)を発現誘導できるように改変したiPS細胞。
下:細胞核(青)、オリゴデンドロサイト(緑)にそれぞれ特異的なマーカーで染色した画像。スケールバーは100マイクロメートル(μm、1μmは1,000分の1mm)。
次に、軸索構造を模倣した直径約0.7マイクロメートル(μm、1μmは1,000分の1mm)のナノファイバー上でオリゴデンドロサイトを培養すると、細胞突起がファイバーに沿って伸長し、ファイバーを包み込むような形態を示すことが観察されました(図2)。
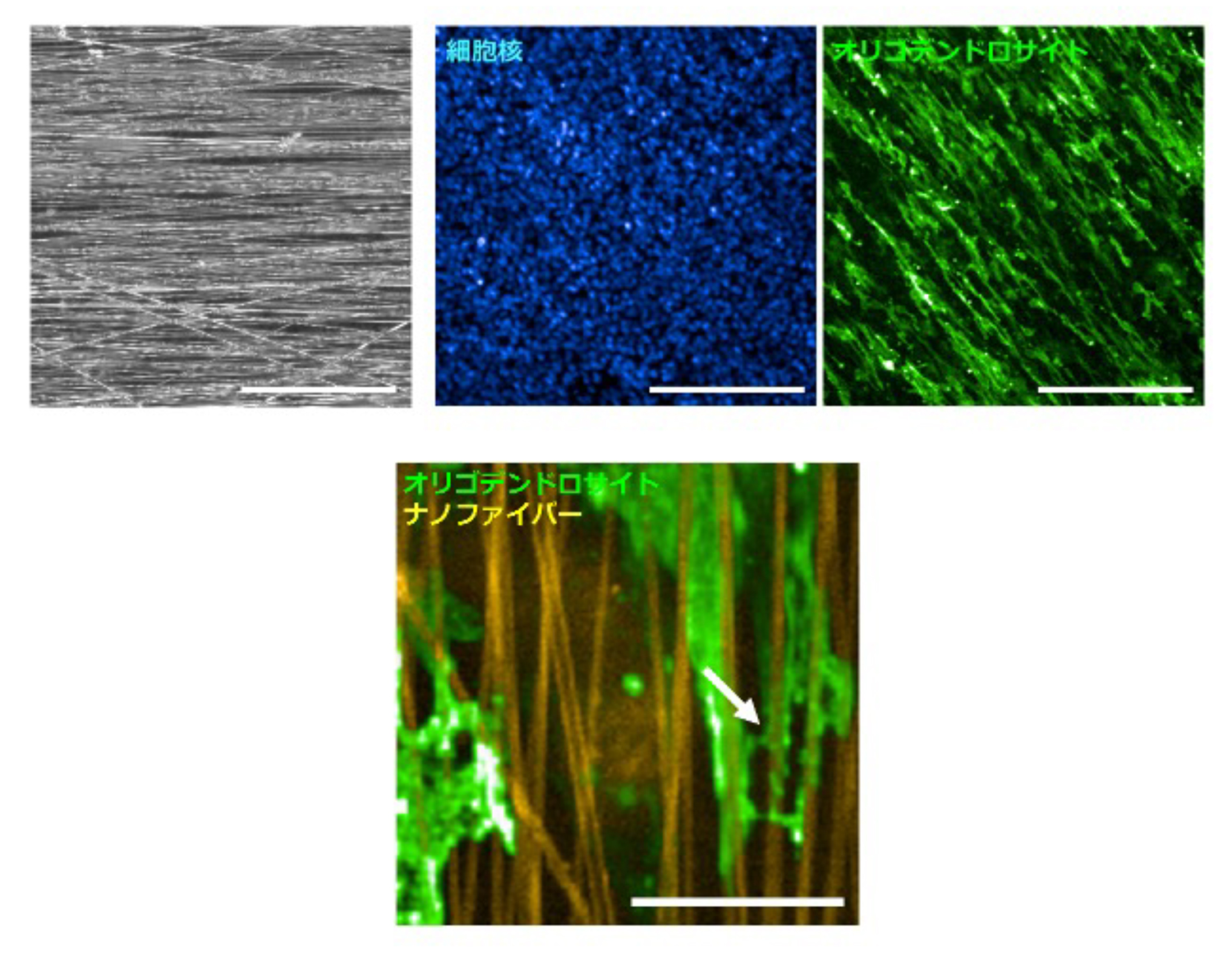
図2 オリゴデンドロサイトの突起伸長とナノファイバーを包み込む過程
(髄鞘形成過程)
上:左から、使用したナノファイバー(明視野画像)、ナノファイバー上で培養した細胞の細胞核(青)、オリゴデンドロサイト(緑)を示す画像。スケールバーは200μm。
下:オリゴデンドロサイト(緑)の突起が伸長し、ナノファイバーを被覆する構造が観察された(白矢印)。黄色はナノファイバーを示す。スケールバーは20μm。
RNAシーケンス解析(次世代シーケンサーを用いて遺伝子発現を網羅的に解析する手法)を用いて、ナノファイバー上で培養したオリゴデンドロサイトの遺伝子発現の変化を明らかにしました。通常の2次元培養と比較して、ナノファイバー上で培養したオリゴデンドロサイトは細胞外マトリックス注9)の形成、脂質代謝、細胞接着に関わる遺伝子群の発現が増加していることが分かりました。一方で、突起伸長に関わる遺伝子群の発現は低下していました(図3)。これらの結果は、ナノファイバー環境においてオリゴデンドロサイトは軸索を包み込む状態へと変化していることを示唆しています。
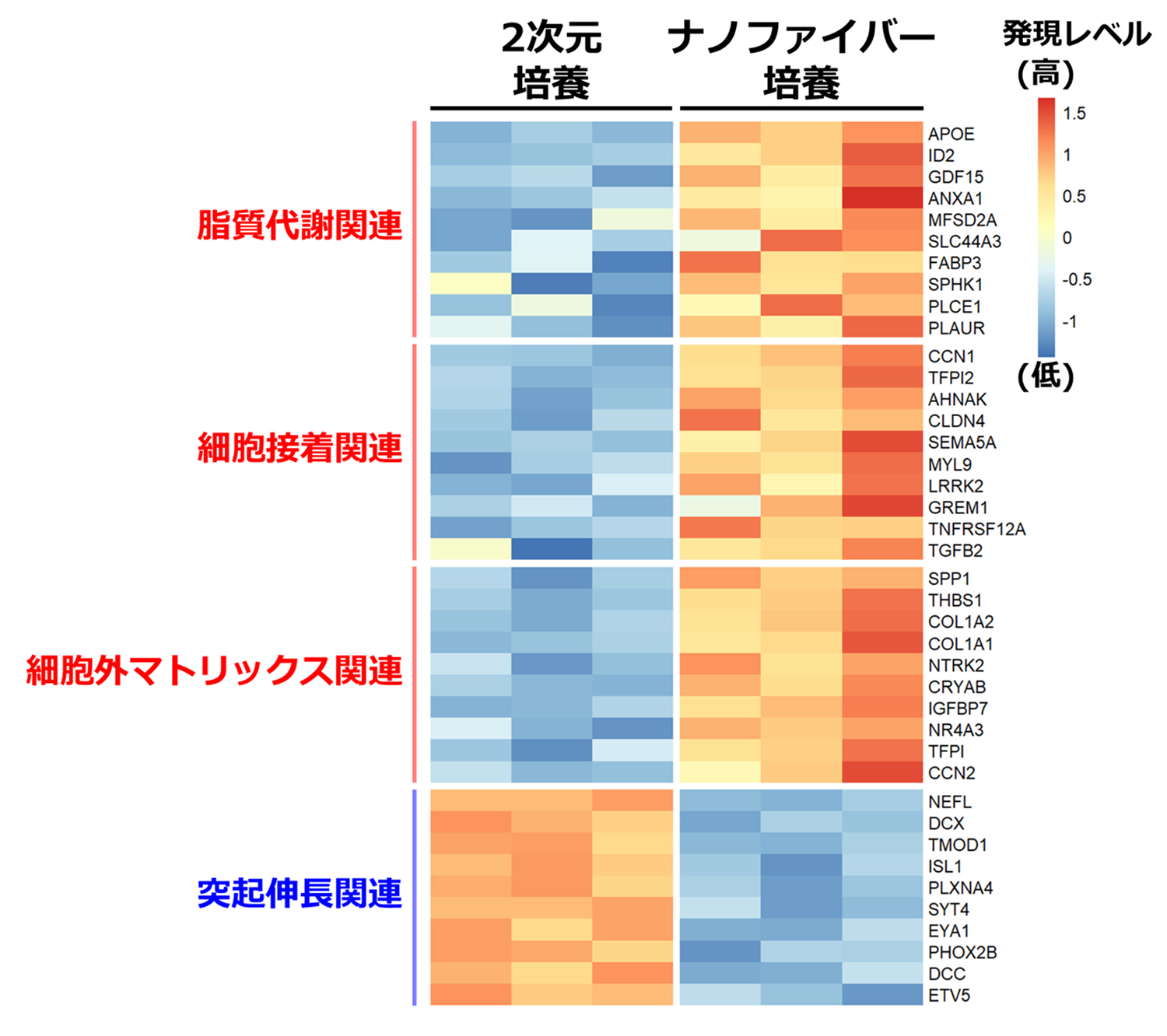
図3 髄鞘形成初期過程に関連する遺伝子発現の変化
2次元培養と比較して、ナノファイバー上で培養したオリゴデンドロサイトは細胞外マトリックス、脂質代謝、細胞接着に関わる遺伝子発現が増加していた。一方で、突起伸長に関わる遺伝子発現が低下していた。
さらに共同研究チームは、ナノファイバーに沿って発現している髄鞘特異的な接着分子であるClaudin-11の発現を指標とすることで、オリゴデンドロサイトによる包み込み構造を定量的に評価できる方法を確立しました。この評価系の有用性を検証するため、髄鞘の形成に作用することが知られている化合物を用いて解析を行いました。その結果、髄鞘形成を促進することが知られている化合物ではClaudin-11の発現が増加し、髄鞘形成を障害することが知られている化合物ではその発現が低下しました(図4)。これらの結果により、本方法によりオリゴデンドロサイトの髄鞘形成過程に対する化合物の作用を評価できることが示されました。
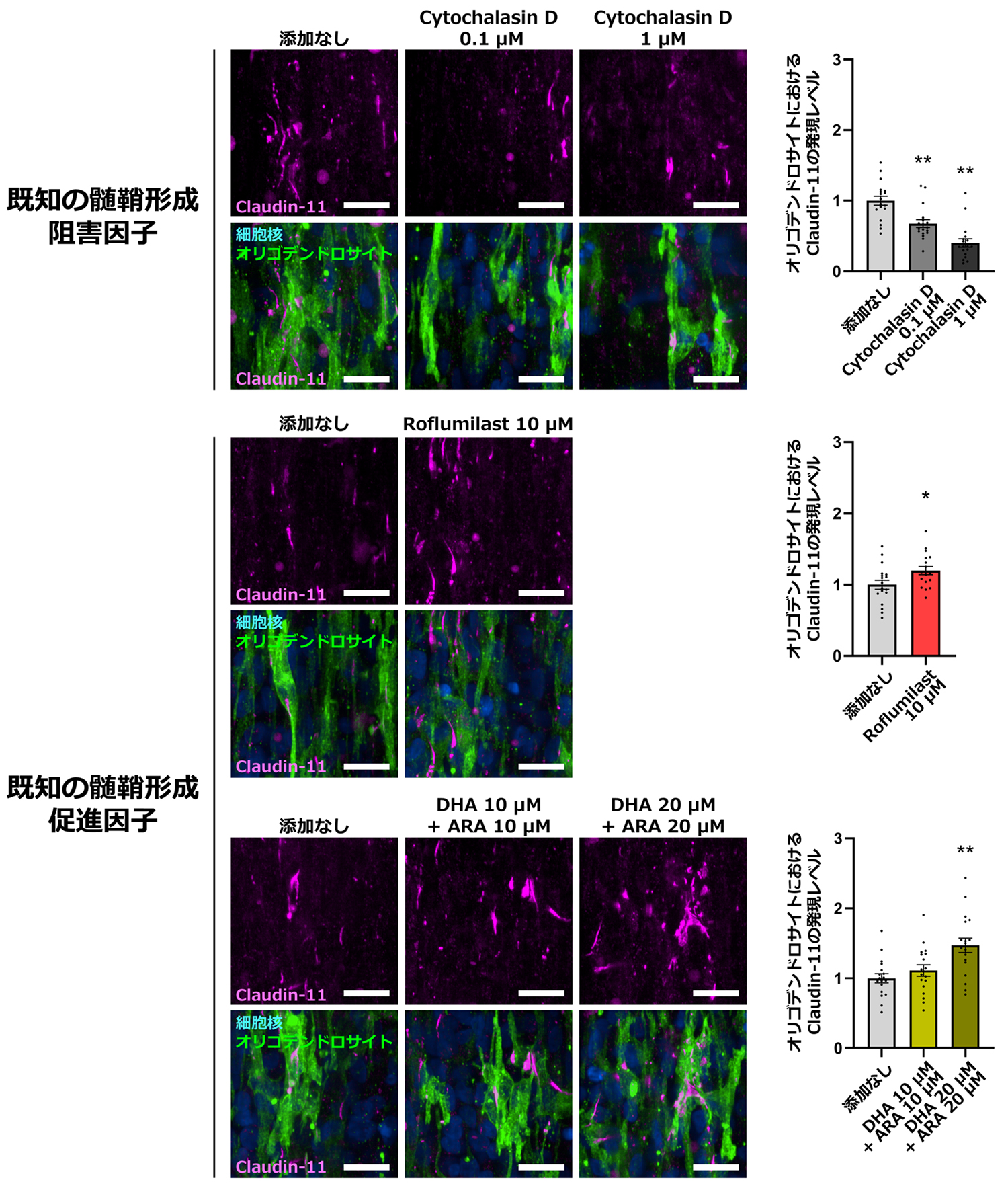
図4 Claudin-11を指標とした化合物応答の定量評価
既知の化合物を添加し、Claudin-11を指標とした定量評価を実施した。スケールバーは20μm。DHAはドコサヘキサエン酸、ARAはアラキドン酸を表す。「*」は統計的に有意な変化であることを示す。μM(マイクロモーラー)は溶液中の濃度を示す単位で、非常に薄い濃度を表す。
上:既知の髄鞘形成阻害因子(Cytochalasin D)を添加した結果、Claudin-11のシグナルが低下した。
中:既知の髄鞘形成促進因子(Roflumilast)を添加した結果、Claudin-11のシグナルが増加した。
下:既知の髄鞘形成促進因子(DHA、ARA)を添加した結果、Claudin-11のシグナルが増加した。
本研究で確立された評価系は、ヒトオリゴデンドロサイトによる軸索の包み込みを定量的に解析できる新たな方法です。今後、この方法を用いることで、オリゴデンドロサイトの機能不全が関与する神経疾患や老化に伴う白質変化の研究が進むことが期待されます。また、髄鞘形成を促進する化合物の探索や、薬剤による白質障害の評価など、薬剤の有効性評価ならびに安全性評価への応用も期待されます。さらに、本技術は、白質生物学の研究および初期ミエリン形成を調節する化合物の評価に向けた新たなツールとなり、生体模倣システム(MPS)注10)の観点からも重要な意義を有します。今後、患者さん由来iPS細胞から分化誘導した神経細胞との共培養などにより、より生理的な環境に近いモデルの構築につながる可能性があります。
- 論文名
Nanofiber-based platform for quantitative analysis of human oligodendrocyte ensheathment with pharmacological perturbations - ジャーナル名
Stem Cell Reports - 著者
Satoshi Morita1,2,3, Takayuki Kondo1,2,4, Keiko Imamura1,2,4, Yukako Sagara2, Kayoko Tsukita1, Hisanori Tokuda3, Yoshihisa Kaneda3, Takayuki Izumo3, Yoshihiro Nakao3, Haruhisa Inoue1,2,4,*
*:責任著者 - 著者の所属機関
- 京都大学iPS細胞研究所(CiRA)
- 理化学研究所 バイオリソース研究センターiPS創薬基盤開発チーム
- サントリーウエルネス株式会社生命科学研究所
- 理化学研究所 革新知能統合研究センターiPS細胞連携医学的リスク回避チーム
本研究は、下記機関より支援を受けて実施されました。
-
日本医療研究開発機構(AMED)
- 再生・細胞医療・遺伝子治療実現加速化プログラム
「次世代医療を目指した再生・細胞医療・遺伝子治療研究開発拠点」
「レジストリ連携による神経変性疾患iPS細胞コホートの構築と整備」
「脳細胞ヒト化による神経病態と免疫応答解析の基盤技術開発」- 認知症研究開発事業
「病的バリアントを有する遺伝性認知症を対象としたコホート構築による病態解明、
バイオマーカー開発、治験促進」- 脳神経科学統合プログラム
「認知症保護的バリアントの機能解明に基づく治療の研究開発」 - 日本学術振興会(JSPS)科学研究費助成事業(JP23K06927)
- 厚生労働省科学研究費補助金 難治性疾患政策研究事業(JPMH24FC1008)
など
また、本研究には理研バイオリソース研究センターから提供されたバイオリソース(ヒトiPS細胞株HPS1748、HPS4290、HPS5652)が使用されました。
注1)人工多能性幹細胞(iPS細胞)
血液や皮膚の細胞にOct3、Sox2、Klf4遺伝子などを導入することで人工的に作製される。培養皿内で無限に増やすことができ、かつ、多様な種類の体細胞に分化させることができる。
注2)オリゴデンドロサイト
中枢神経系に存在するグリア細胞(注6参照)の一種で、神経細胞の軸索(注3参照)を包み込む髄鞘(注4参照)を形成する細胞。
注3)軸索
神経細胞から伸びる細長い突起で、電気信号を遠くの細胞へ伝える役割を持つ。オリゴデンドロサイトによって形成される髄鞘が軸索の周囲を覆い、信号伝達の速度が高められる。
注4)髄鞘
神経細胞の軸索を取り囲む脂質とタンパク質から成る多層構造。電気信号の伝導効率を高める絶縁体のような役割を果たす。中枢神経系では主にオリゴデンドロサイトによって形成される。
注5)Claudin-11
髄鞘に特異的に発現する接着分子で、髄鞘構造の形成や安定化に関与することが知られている。
注6)グリア細胞
神経細胞を支え、神経機能を維持する細胞群の総称。神経細胞の保護や栄養供給、神経伝達の調節など多様な役割を担う。オリゴデンドロサイト、アストロサイト、ミクログリアなどが含まれる。
注7)多発性硬化症
中枢神経系の髄鞘が障害される自己免疫性疾患。髄鞘が破壊され、視覚障害や運動障害などさまざまな症状が生じる。
注8)転写因子
DNAに結合して特定の遺伝子の発現を調節するタンパク質。細胞の分化や発生過程に重要な役割を果たし、特定の転写因子を発現させることで細胞の性質を変化させることができる。
注9)細胞外マトリックス
細胞の周囲に存在するタンパク質や多糖類などから成る構造体。細胞を支える足場として働く他、細胞の接着や移動、分化などの細胞機能を調節する役割を持つ。
注10)生体模倣システム(MPS:Microphysiological Systems)
生体組織や臓器の微小な環境に近づけた細胞培養環境を用いて、薬物の効果や安全性を評価する技術。























