もっと知るiPS細胞
For the Public
もっと知るiPS細胞
For the Public
患者さん向け情報
For patients and their families
疾患研究について
2021年1月現在の関連情報を元に回答しています。
京都大学では、患者さんの細胞を用いてiPS細胞を作製しているのですか?
はい、行っております。2008年6月に京都大学医の倫理委員会は、患者さんの細胞を用いた疾患特異的iPS細胞に関する研究計画を承認しました。
この研究計画に基づき、デュシエンヌ型筋ジストロフィー、筋萎縮性側索硬化症(ALS)、ファンコーニ貧血など様々な患者さんから体細胞をご提供いただき、iPS細胞の樹立を実施しています。
その後も必要に応じて患者さんの細胞からiPS細胞を作製し、一部の細胞についてはより多くの研究者に利用して頂くため、理化学研究所バイオリソースセンターを通じて研究者への配布を行っています。
患者さんの体細胞から作製されたiPS細胞を用いて、どのような研究をするのですか?
患者さん由来のiPS細胞を患部の細胞や組織等に分化誘導し、その患者さんの病気の状態を再現させることにより、病気の原因やメカニズムの解明を進めています。 また、患部細胞を用いて薬剤の効果、副作用や毒性検査を実施する方法の開発も進んでいます。このような研究により、新しい薬や治療法の開発を進めています
京都大学以外の研究機関でも、患者さんの細胞からiPS細胞を樹立し、研究を行っているのですか?
国内外の研究機関で患者さんのご協力を得て、疾患特異的iPS細胞に関する研究を実施しています。
日本国内では、iPS細胞に関する公的プロジェクトが実施されており、その参加研究機関が様々な研究に取り組んでいます。
【主要な公的プロジェクトのサイト】
2つ下の「iPS細胞研究の最新情報を知りたいのですが、どうすればいいのですか?」をご参照ください。
患者さんを対象としたシンポジウムなどは開催しないのですか?
患者さんと直接お話する機会は大変、貴重であると考えています。 CiRA主催のシンポジウムやサイエンス・カフェなど、患者さんからのご要望等を伺い、CiRAから研究の進捗状況をご説明する機会を設けております。 イベントが決まり次第、イベントカレンダーのページでご案内致します。
iPS細胞研究の最新情報を知りたいのですが、どうすればいいのですか?
CiRAにおける研究情報は、このホームページの研究成果についてのページやシンポジウム等でお知らせする予定です。
京都大学以外の研究機関のホームページやiPS細胞をはじめとした幹細胞や再生医療・細胞医療についての研究情報を掲載しているホームページがありますので、そのようなサイトから情報を入手できます。
【iPS細胞研究等に関する情報サイト】
研究プロジェクトなどについて:
患者さん向け:
<以下は過去のもの(参考掲載)>
臨床研究・治験について
2022年7月現在の関連情報を元に回答しています。
CiRAでの臨床研究または治験の計画は、どうなっているのですか?
京都大学医学部附属病院等と協力して、再生医療(細胞移植治療)や薬の開発で、いくつかの臨床研究または治験に取り組んでいます。 臨床研究または治験を開始することになりましたら、ホームページ等でお知らせします。
再生医療/細胞移植治療に関するプロジェクト:
薬の開発に関するプロジェクト:
参考情報:
iPS細胞を用いた再生医療(細胞移植治療)の臨床研究または治験に参加したいのですが、どうすればいいのですか?
CiRAでの臨床研究または治験が開始されることになりましたら、ホームページ等を通じてお知らせする予定です。CiRA以外での研究等については以下のページも御覧ください。
iPS細胞やその他の幹細胞を用いた治療を行っている医療機関をインターネットで見かけました。安全性の問題はないのでしょうか?
iPS細胞をつかった治療法は未だ研究の段階であり、現段階でiPS細胞を用いて治療を行っている医療機関はありません。 日本においては、ES細胞(胚性幹細胞:embryonic stem cell)に関しても、ES細胞を用いて治療を行っている医療機関はありません。
一方、iPS細胞やES細胞のように、身体を構成するさまざまな細胞へと分化する幹細胞ではなく、体の中に存在する幹細胞(体性幹細胞)を用いた新しい治療法の開発も進んでいます。
一部のインターネットサイトや出版物において、難病と呼ばれる幾つかの疾患から、生活習慣病と呼ばれる一般的な疾患に至るまで、読者が治療効果を期待するような言葉を使い、 体性幹細胞と称するものを用いて注射・点滴などを行う医療機関が国内外に見られます。 これらの行為は論文などによる治療効果や安全性の根拠に乏しいなど疑問点も少なくなく、安全性確保や患者保護に関する情報についてもほとんど開示されていません。 そのため、日本再生医療学会は不適切な幹細胞治療に関して注意を呼び掛けています。 幹細胞治療の受診を検討される際には、その治療が科学的根拠にもとづいて安全性が確認されており、公的機関による承認を得ているかの確認をされることをお勧めします。
また、国際幹細胞学会が、幹細胞および幹細胞治療についてよくある質問に対する回答を記載した「幹細胞治療について患者ハンドブック」を作製しており、WebサイトからPDFをダウンロードできます。 このハンドブックには、幹細胞治療を検討する際に最低限確認すべき項目があげられていますので、ご参照ください。
国内では、「再生医療等の安全性の確保等に関する法律」が2013年11月に成立し、幹細胞を用いた治療を担保する法整備が進んでいます。
iPS細胞を用いた細胞移植治療はいつ実現するのですか?
iPS細胞の安全性、治療効果が確認されたら、患者さんのご協力を得て、臨床研究または治験を進めます。世界で初めてiPS細胞を利用した再生医療の臨床研究として、2014年9月に加齢黄斑変性の患者さんへのiPS細胞由来の細胞移植手術が行われました。その後、他の疾患についても臨床研究や治験が順次開始されています。 しかし、一般の方々に広く細胞移植治療を提供していくには、企業などによる細胞の大量調製技術の確立、各地病院での治療展開が必要です。
従いまして、現時点では、医療応用が可能になる時期を明確にお答えすることは難しい状況です。一日も早く新しい治療法を患者さんに届けることを目指して日々研究を推進してまいります。
パーキンソン病の治験について
2025年4月現在の関連情報を元に回答しています。
このページで「治験」とは、京都大学医学部附属病院において実施されている「iPS細胞由来ドパミン神経前駆細胞を用いたパーキンソン病治療に関する医師主導治験」のことを指します。
治験では、どのような症状の患者さんが対象になりますか?
パーキンソン病と診断されている方のうち、以下のような方が対象となります。
・薬物治療では症状のコントロールが十分に得られない。
・同意取得時の年齢が50才以上70才未満である。
・抗パーキンソン病薬によるオンとオフが認められる。
・オフ時のHoehn&Yahr重症度分類がStageⅢ以上である。
・オン時のHoehn&Yahr重症度分類がStageⅢ以下である。
・L-ドパ投与によく反応する。
なお、本治験に関する患者さんの募集は終了しています。
治験には何人くらいが参加するのですか?
公募にて7名の患者さんにご協力いただき、募集を終了しました。
治験参加をご希望の患者さんは、どの病院で実施されるのですか?
京都大学医学部附属病院で実施されます。
細胞移植のための入院期間はどれくらいですか?
約1ヶ月の予定です。
細胞移植後の観察期間はどれくらいですか?
その間、通院や入院が必要ですか?
細胞移植後、2年間の経過観察を行います。術後しばらくは1ヵ月ごと、その後2ヶ月ごとに京大病院に通院していただく必要があります。その間に5回、入院による検査を予定しております。また、治験終了後も引き続き経過観察が必要です。
手術や経過観察の際の入院期間は?
細胞移植手術の際の入院期間は約1ヶ月を見込んでいます。経過観察の際は約1週間の予定です。
治験に参加する際の費用は、誰が負担するのですか?
現在服用されているパーキンソン病のお薬や検査の費用などは通常の保険の対象となり、患者さんの自己負担が一部発生します。また、通院にかかる交通費は患者さんにご負担いただきます。ただし、移植用の細胞をつくる費用、細胞移植手術の費用、保険診療として認められていない検査等に関する費用は研究費で負担します。
治験に参加したいのですが、どの様に申し込めば良いでしょうか?
本治験に関する患者さんの参加募集は終了しています。
どのような手術をするのでしょうか?
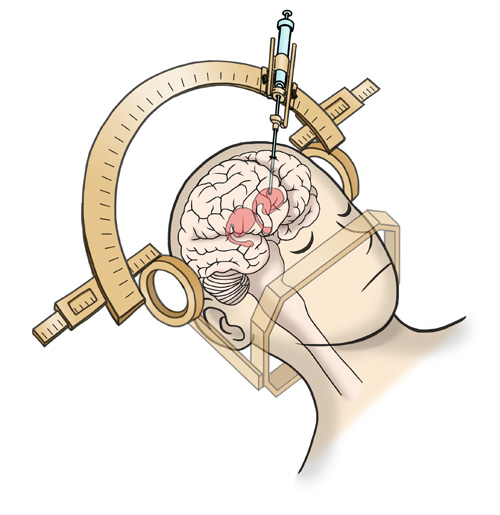
iPS細胞から分化誘導したドパミン神経前駆細胞(3例目まで計約500万個、4例目以降約1000万個)を、定位脳手術により、患者さんの脳の線条体(左右両側)に移植します。
現在、手術療法の主流である脳深部刺激療法(DBS手術)に置き換わる治療法となるのですか?
また、DBS手術と併用できる治療になるのですか?
治療法として、選択肢の一つが増えるというように捉えています。 今回の治験ではDBS手術を受けられた方は対象外となりますが、将来的には併用も可能であると考えています。
いつ頃一般的に治療を受けられるようになるのですか?
治験の結果次第であり、現時点では不明です。
実用化した場合、その際には保険適用になるのですか?
保険適用になることを目指します。
治験の進捗状況を教えて下さい。
2018年に開始した本治験につきまして、2021年には予定していた7例すべての患者さんの手術を終了し、2023年末をもって細胞移植後の経過観察期間も無事終了しました。
2025年4月には結果をまとめた論文がNature 誌に掲載されました。
ALSの治験について
2022年4月15日現在の関連情報を元に回答しています。
CiRAのボスチニブを用いた筋萎縮性側索硬化症(ALS)の治験に関するQ&Aです。
CiRAが関与しているALS治験には、どのようなものがありますか?
井上治久教授のグループが中心となり、ボスチニブを用いた医師主導治験の第1相治験を2019年3月から2021年9月まで実施しました。2022年4月に第2相治験を開始しました。
「筋萎縮性側索硬化症(ALS)患者を対象としたボスチニブ第1相試験」
「筋萎縮性側索硬化症(ALS)患者を対象としたボスチニブ第2相試験」
第2相試験の対象となるのはどのような患者さんですか?
第2相治験には何人くらいが参加するのですか?
全ての治験実施機関の合計で25人を予定しています。
第2相治験の期間はどのくらいですか?
1人の患者さんにつき、治験薬投与前の観察期間12週間、移行期間1週間、治験薬投与期間24週間とその後の経過観察期間4週間の合計41週間です。
すべての患者さんの観察期間が終了するのは2024年頃を予定しています。
通院や入院は必要ですか?
治験薬の投与が開始してから原則として約1週間は入院での経過観察が必要です。
それ以外の期間は定期的な外来通院が必要です。
第2相治験に参加する際の費用は、誰が負担するのですか?
治験薬は治験薬提供者(ファイザー社)から無償で提供されます。また、保険診療下での受診および検査の費用が必要になります。
一方、現在服用されているお薬や検査の費用などは通常の保険の対象となり、患者さんの自己負担が一部発生します。入院期間の費用についても、通常の入院と同様に、患者さんの医療保険が適応され自己負担が一部発生します。
アルツハイマー病の治験について
2022年6月30日現在の関連情報を元に回答しています。
このページで「治験」とは、2020年6月5日より開始している「プレセニリン1遺伝子変異アルツハイマー病に対するTW-012R(ブロモクリプチン)の安全性と有効性を検討する二重盲検比較試験及び非盲検継続投与試験」のことを指します。
- 家族性アルツハイマー病患者さんを対象とした医師主導治験(結果速報)(2022年6月30日)
治験では、どのような症状の患者さんが対象になりますか?
家族性アルツハイマー病と診断されている方のうち、一定の条件を満たす方を対象としています。
詳しくは以下のページをごらんください。
治験には何人くらいが参加するのですか?
全ての治験実施機関の合計で10名程度を予定しています。
治験の期間はどのくらいですか?
参加者の通院の期間として、1年程度を予定しています。
通院や入院は必要ですか?
ほとんどの観察日は外来にて行います。
一部1泊2日の入院を予定していますが、担当医と相談の上で変更することもあります。
治験に参加する際の費用は、誰が負担するのですか?
本治験は、京都大学発ベンチャーであるタイムセラ株式会社より支援を受けて実施されます。治験薬は東和薬品株式会社から無償で提供されます。また、治験の一環として保険診療としては認められていない検査等を行う場合、費用は研究費で負担します。
それ以外の医療費には健康保険が適用され、自己負担分をお支払いいただきます。
卵巣がんの治験について
2022年7月13日現在の関連情報を元に回答しています。
このページで「治験」とは、2021年4月12日より開始している「GPC3発現手術不能進行再発卵巣明細胞癌で腹膜播種を有する患者を対象とした、抗GPC3-CAR発現iPS細胞由来ILC/NK細胞を腹腔内投与することの安全性及び忍容性を検討する第I相臨床試験」 のことを指します。
治験では、どのような患者さんが対象になりますか?
GPC3発現手術不能進行再発卵巣明細胞癌で腹膜播種を有する患者さんが対象になります。
治験には何人くらい参加するのですか?
6人から18人の患者さんにご協力いただく予定です。
治験に参加したいのですが、どのような手続きが必要ですか?
治験に参加する場合、通院や入院は必要ですか?
細胞移植を行う際に1ヶ月程度の入院が必要です。また退院後も、6ヶ月ごとを目処に通院など、追跡調査にご協力いただきます。
治験に参加する際にかかる費用は、誰が負担するのですか?
現在服用されているお薬や検査の費用などは通常の保険の対象となり、患者さんの自己負担が一部発生します。治験参加のために通院にかかる交通費は患者さんにご負担いただきます。
移植用の細胞をつくる費用、細胞移植手術の費用は研究費で負担します。
治験の進捗状況を教えてください。
2021年9月に1例目の細胞移植を実施しています。
現在もご協力いただける患者さんを募集中です。