
ニュースレター
Newsletter
ニュースレター
Newsletter

Focus
2025年2月20日
iPS細胞を使った治療困難な肺疾患への挑戦

間質性肺炎(肺線維症)など治療が難しい肺疾患は、進行すると人工呼吸器や肺移植に頼らざるを得ません。「日本肺および心肺移植研究会」によると、2023年には日本では年間228名の患者さんが肺移植待機リストに登録された一方で、実際に手術を受けられたのは年間127名にとどまりました。移植までの平均待機期間は約2年半と長く、この間に病状が悪化し、命の危険にさらされるケースも少なくありません。ドナー不足は日本だけでなく世界的な問題でもあります。
こうした現状を変えるため、CiRAの後藤慎平教授は、iPS細胞を活用して、肺の病気のメカニズムの解明、創薬研究、そして再生医療研究を行っています。後藤教授に研究の進捗や今後の展望についてお話を聞きました。

後藤 慎平 教授
肺の研究者になったきっかけを教えてください。
京都大学医学部を卒業後、研修医として病院に勤務していたのですが、その病院には呼吸器疾患の患者さんが多く、特に私たちがよく診ていたのは肺が固くなって縮んでいく間質性肺炎の患者さんでした。治療手段が限られる中で病状がどんどん悪化していくのを見るうちに、現代の医療の限界を感じました。そういう患者さんのことがずっと忘れられなくて、研究の力で治療困難な肺の疾患を治せないかと考えるようになりました。
それで、京都大学大学院医学研究科に入学して呼吸器に関する基礎研究から始めることにしました。もともと学部時代から基礎研究の面白さを感じていましたし、基礎的なところから研究をすることで何か新しい治療法を見つけられるんじゃないかという期待もありました。
研究を始めた当初はどのような状況でしたか?
私が大学院に入ったころは、山中伸弥教授がiPS細胞の論文を発表して3年ほど経った時でした。しかし当時は、肺の再生医療研究は世界でもまだ進んでいない未開拓の分野でしたから、すぐにiPS細胞を使って肺の細胞を作って再生医療の研究ができるという段階ではありませんでした。そこで、CiRAに協力してもらい、まずはiPS細胞の培養方法や分化誘導の技術を習うことから始めました。その後もCiRAの先生方にiPS細胞から肺細胞への分化方法についての相談を重ね、ようやくiPS細胞から肺のもとになる細胞を効率よく作れるようになりました。
その後、iPS細胞由来の肺のもとになる細胞を使って肺胞オルガノイド(肺のミニ臓器)も作れるようになったという論文を世界に先駆けて出すことができました。自分たちの力だけでは到底できなかったことなので、CiRAにはとても感謝しています。
肺胞オルガノイドを使ってどのような研究をしているのでしょうか?
肺胞というのは肺の中の組織で、酸素を取り込んで二酸化炭素を排出する場所です。肺の中には、3億個程度の肺胞があり全身への酸素供給を支えています。肺胞は、1型肺胞上皮細胞と2型肺胞上皮細胞で構成されています。2型肺胞上皮細胞は平べったい1型肺胞上皮細胞に分化したり、肺サーファクタントという肺の膨らみやすい状態を維持する物質を分泌したりしています。
私たちはiPS細胞を使って、これらの組織と機能をすべて兼ね備えた肺胞オルガノイド(図1)を効率よく作ることに成功しました。この技術を使って間質性肺炎の患者さんから作製したiPS細胞由来の肺胞オルガノイドを作り、病気のメカニズムを観察することができました。また、この肺胞オルガノイドに間質性肺炎を発症させる薬剤を投与することで、培養皿の中で間質性肺炎を再現することもできました。この病態モデルを使って、治療薬候補の探索を行っています。
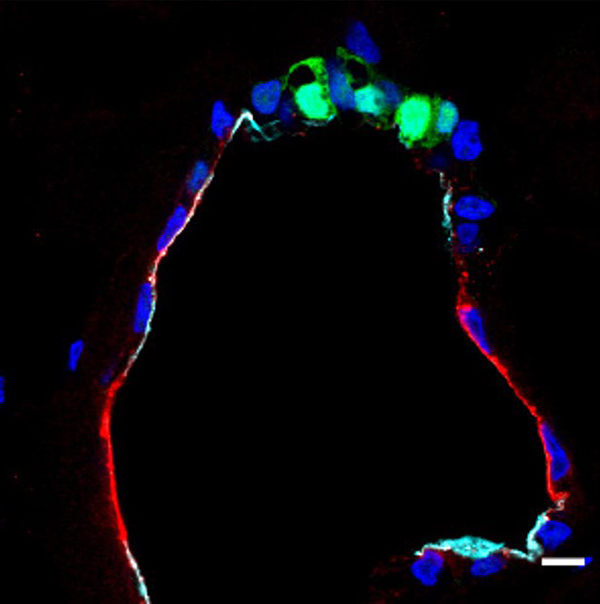
図1:iPS細胞から作製した肺胞オルガノイドの断面
緑色は丸い形をした2型肺胞上皮細胞、赤色は平べったく分化した1型肺胞上皮細胞を示す。オルガノイドの内側の黒い空間は肺サーファクタントなどの分泌物質が充満している。
新型コロナウイルスに関する研究も行っているとお伺いしました。
特殊加工したプレートを使って、肺胞オルガノイドと気道オルガノイド(図2)を「2.5次元」に培養できる技術を開発しました(図3)。通常、これらのオルガノイドは3次元で作製するのですが、培養に用いるゼリー状の物質に包まれた状態となり、調べたい新型コロナウイルスをオルガノイドに感染させることができません。オルガノイドを「2.5次元」培養すると、肺胞あるいは気道オルガノイドの一部が培地側に顔を出した状態になり、その出ている部分に簡単にウイルスを感染させることができるのです。
この技術を使って、新型コロナウイルスを肺の細胞に感染させる実験をCiRAの高山和雄講師と共同研究で行いました。この研究で、新型コロナウイルスは2型肺胞上皮細胞にはよく感染するということや、気道オルガノイドにも広く感染すること、ただし、変異株によって感染の仕方が違うということがわかってきました。パンデミックの時に問題になったデルタ株は、肺胞オルガノイドにも気道オルガノイドにもかなり強く感染することや、オミクロン株では感染力はだいぶ落ちることもわかりました。今後、新しいウイルスが出てきてメカニズムを知りたいときにも、この技術は使えると思います。
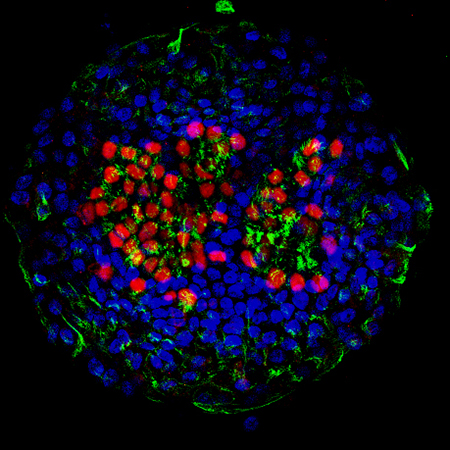
図2:iPS細胞から作製した気道オルガノイド
中央の赤色に染まった部分は線毛細胞の核を示し、赤色周辺の濃い緑色に染まった部分は線毛を示す。
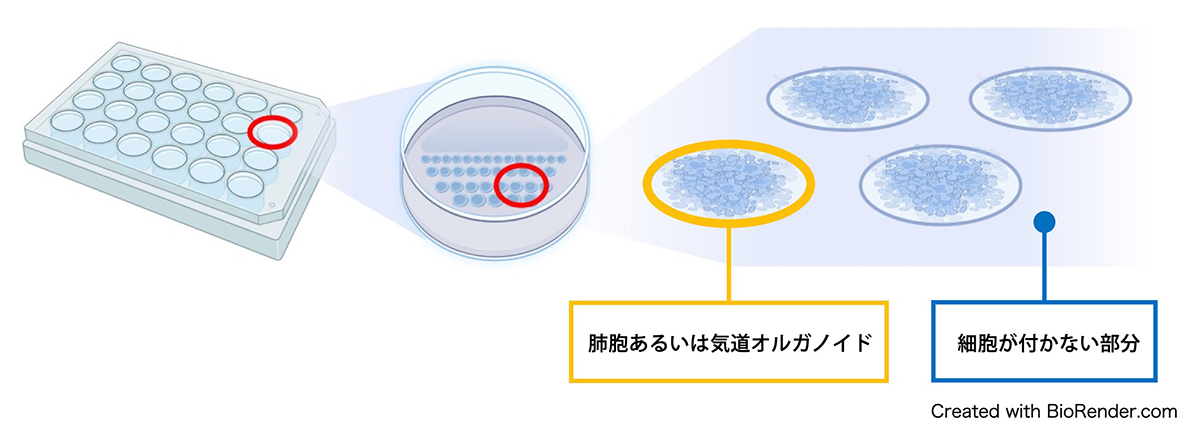
図3:「2.5次元」培養のイメージ
その他に、どのような肺の疾患の研究をしているのですか?
気道には線毛という動く毛がたくさん生えた細胞があり、ウイルスや細菌、異物などを肺まで届かないように守っています。粘液がとらえた異物を痰として喉まで運んでいるのが線毛の役割です。その線毛が動かなくなる病気についても研究しています。
線毛機能不全症候群という、咳や痰が続き、肺炎などを繰り返す指定難病がありまして、診断が一筋縄ではいかないうえに、治せる薬もありません。病気の診断をするために、患者さんの線毛細胞を取ってきて何度も調べるのも患者さんにとっては負担です。そこで、患者さんから血液をいただいてiPS細胞を作製し、患者さんの線毛細胞を作りだすことで病気を再現できるようになりました。病気の原因になる遺伝子を証明できるようになったので、治療薬の候補を探す研究も進めています。
このように病気を再現できるようになったのも、iPS細胞から線毛細胞を含む気道オルガノイドを作れるようになったことが成果として大きかったと思います。ただ、培養方法にはこれでもまだ限界があり、培養皿上で単純に気道オルガノイドを作製しただけでは、線毛の方向が揃わないことが昔からの問題でした。線毛細胞は生体内で同じ方向にそろって線毛を動かすことで異物を除去しています。線毛細胞同士の線毛の動きをそろえるにはどうしたらよいか、私たちはその課題にも取り組み、京都大学大学院工学研究科の先生との共同研究で気道の機能を再現した「気道チップ」を作ることができました(図4)。
このチップにiPS細胞から作製した気道上皮細胞を乗せて培養するんですけども、培地が流れる構造になっており、そこで細胞を培養すると線毛細胞がお互いに協調しあって、流れを止めても一定の方向に線毛が動くようになります。こうやって線毛細胞同士を協調させた状態をチップ上で再現できるようになりました。
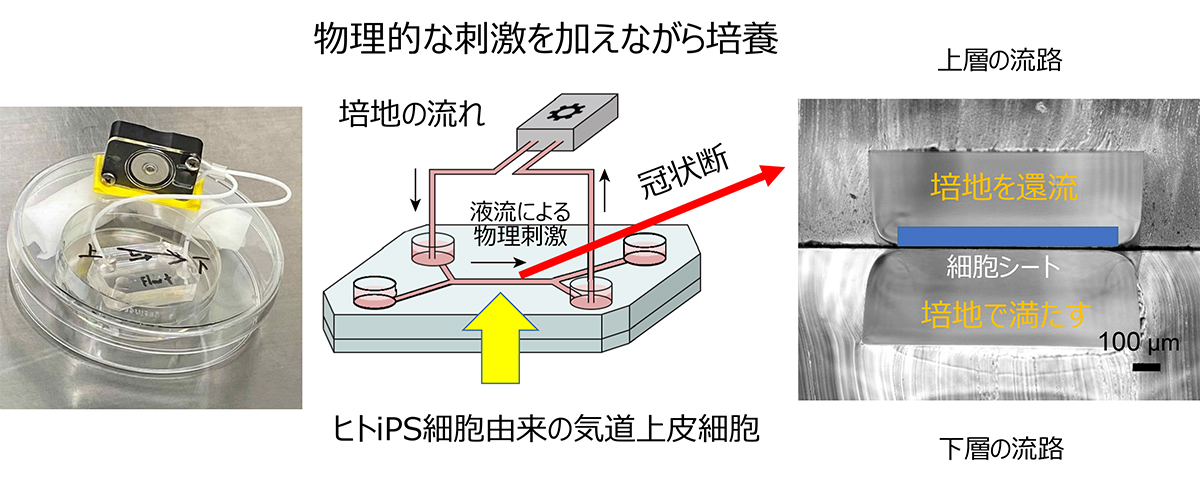
図4:「気道チップ」の仕組み
今後の目標は何ですか?
私たちはiPS細胞を使って肺の薬を見つける研究と肺を再生させる研究の二本立てでやっています。まずは肺の疾患に役立つ薬を見つけたいっていうのがありますね。そして、その少し先には細胞を使って肺の再生ができればと思っています。
現在、iPS細胞を使って肺を再生するための研究も進めており、ヒトiPS細胞から肺のもとになる細胞を作って、マウスの肺に移植して、きちんと生着して肺の機能を果たしているかを調べています。この技術が人にも応用できたらと考えています。
あとは個別化医療の研究も進めたいです。同じ病気でも人によって病状は異なりますよね。ですので、例えば、こういう病状の患者さんにはこの薬を使うとすごく効果があるとか、一人一人の患者さんにあった治療をしたいと考えています。
やっぱりiPS細胞の強みは、患者さん由来の細胞が利用できたり、患者さんの遺伝子に着目した研究ができたりと、個別化医療につなげやすいところだと思います。たとえ患者さんの数が少ない疾患だとしても、その患者さんにとってすごく効く薬が見つかると、肺移植を待っている間のリスクの高い状況を減らせるのではないかと思っています。
もともと研究をスタートした理由が、治せない肺の病気を治せるようにしたいということだったので、iPS細胞から作った肺の細胞を使って臨床応用までつなげることが一番大事だと思っています。そして、私の最終目標はiPS細胞を使って「肺を創る」です。その目標の実現に向けて、日々努力を続けています。
-
プロフィール: 後藤 慎平 教授
京都府出身。京都大学医学部を卒業後、呼吸器内科での研修医・医員を経て、京都大学大学院医学研究科修了(医学博士)。同大学附属病院特定助教、同大学大学院医学研究科特定准教授などを経て、2022年よりCiRA教授。趣味は何かにチャレンジすること。 -
取材・執筆した人:三宅 陽子
京都大学iPS細胞研究所(CiRA) 国際広報室 サイエンスコミュニケーター























